1-Brombutan – Wikipedia
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 1-Brombutan | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C4H9Br | |||||||||||||||
| Kurzbeschreibung | farblose bis gelbliche Flüssigkeit mit charakteristischem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 137,03 g·mol−1 | |||||||||||||||
| Aggregatzustand | flüssig[1] | |||||||||||||||
| Dichte | 1,28 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt | 102 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Brechungsindex | 1,4399 (20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
1-Brombutan ist eine chemische Verbindung aus der Gruppe der aliphatischen, gesättigten Halogenkohlenwasserstoffe und gehört zur Gruppe der Butylbromide.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]1-Brombutan kann durch Bromierung von 1-Butanol mittels Bromwasserstoffsäure oder Phosphortribromid gewonnen werden.[4] Auch die Bromierung mit Natriumbromid und Schwefelsäure liefert 1-Brombutan.[5]
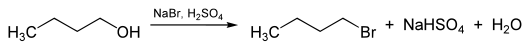
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]1-Brombutan bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt bei 12 °C.[1][6] Der Explosionsbereich liegt zwischen 2,6 Vol.‑% (145 g/m3) als untere Explosionsgrenze (UEG) und 5,6 Vol.‑% als obere Explosionsgrenze (OEG).)[1][6] Die Zündtemperatur beträgt 265 °C.[1][6] Der Stoff fällt somit in die Temperaturklasse T3.
Verwendung
[Bearbeiten | Quelltext bearbeiten]1-Brombutan kann zur Alkylierung und zur Herstellung von Butyllithium aus Grignard-Verbindungen verwendet werden. Durch Reaktion von 1-Brombutan mit Quecksilber(II)-fluorid kann 1-Fluorbutan gewonnen werden.[7]
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Versuchsvorschrift: Alkylierung von Malonsäurediethylester mit 1-Brombutan zu 2-(Ethoxy-carbonyl)hexansäure-ethylester (PDF) der Sammlung Integriertes Organisch-chemisches Praktikum der Universität Regensburg, abgerufen am 30. Oktober 2011.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h i j k l m n o p Eintrag zu 1-Brombutan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Januar 2023. (JavaScript erforderlich)
- ↑ a b c Eintrag zu 1-Brombutan bei TCI Europe, abgerufen am 27. Juni 2011.
- ↑ Frank B. Tutwiler, R. L. McKee: The Iodide Ion Exchange Reaction with 2-Haloethyl Alkyl Ethers and n-Butyl Bromide. In: Journal of the American Chemical Society. 76, 1954. S. 6342–6344. doi:10.1021/ja01653a029.
- ↑ Autorenkollektiv: Organikum. 22. Auflage. Wiley-VCH, 2004, ISBN 978-3-527-31148-4.
- ↑ Uni Siegen: Arbeitsvorschrift zur Herstellung von 1-Brombutan (PDF; 14 kB).
- ↑ a b c E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen. Band 1: Brennbare Flüssigkeiten und Gase. Wirtschaftsverlag NW – Verlag für neue Wissenschaft, Bremerhaven 2003.
- ↑ I.L. Knunyants, G.G. Yakobson: Syntheses of Fluoroorganic Compounds. Springer Science & Business Media, 2012, ISBN 978-3-642-70207-5, S. 4 (eingeschränkte Vorschau in der Google-Buchsuche).


 French
French Deutsch
Deutsch

