α-Hederin – Wikipedia
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
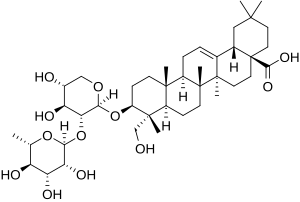
| Name | α-Hederin | ||||||||||||||||||
| Andere Namen | (3β,4α)-3-{[2-O-(6-Desoxy-α-L-mannopyranosyl)-α-L-arabinopyranosyl]oxy}-23-hydroxyolean-12-en-28-säure | ||||||||||||||||||
| Summenformel | C41H66O12 | ||||||||||||||||||
| Kurzbeschreibung | weißer Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 750,96 g·mol−1 | ||||||||||||||||||
| Aggregatzustand | fest[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||

α-Hederin (alpha-Hederin) ist ein schwach wasserlösliches Saponin und pentacyclisches Triterpenoid, welches sich unter anderem in Pflanzen wie Hedera helix (Gemeiner Efeu), Nigella sativa (Echter Schwarzkümmel), Kalopanax septemlobus (Baumaralie) oder der Gattung der Pulsatilla (Kuhschellen) finden lässt. In diesen Pflanzen entsteht es aus dem Aglykon Hederagenin und kann durch Glykosylierung in das bisdesmosidische Saponin Hederacosid C überführt werden.
Gewinnung
[Bearbeiten | Quelltext bearbeiten]α-Hederin kann durch enzymatische oder chemische Hydrolyse von Hederacosid C, welches das Hauptsaponin des Efeus ist, gewonnen und danach aufgereinigt werden. Darüber hinaus ist auch eine Teilsynthese ausgehend vom Methylester des Hederagenins beschrieben.[2]
Medizinische Bedeutung
[Bearbeiten | Quelltext bearbeiten]α-Hederin ist ein verhältnismäßig gut untersuchter Wirkstoff, dem durch präklinische Untersuchungen zahlreiche Eigenschaften zugesprochen werden. Zu diesen Eigenschaften zählen:
- Antiinflammatorisch[3][4][5][6][7]
- Spasmolytisch[8][9][10][11]
- Sekretolytisch[9]
- Antioxidativ[12]
- Antifungal[13]
- Anticancerogen[14][15]
- Antileishmanial[16]
Der Reinstoff spielt klinisch kaum eine Rolle, ist allerdings in Extrakten aus Efeublättern vor allem in Form seiner Vorstufe Hederacosid C enthalten und findet Verwendung in der Behandlung von akuten Bronchitiden und erkältungsbedingten Atemwegserkrankungen. Darüber hinaus ist α-Hederin im islamischen Raum als wichtiger Bestandteil des Schwarzkümmels in der Volksmedizin bekannt.
Pharmakologische Wirkung
[Bearbeiten | Quelltext bearbeiten]
Über α-Hederin ist eine selektive Wechselwirkung mit den β2-Adrenozeptoren bekannt, welche sich unter anderem vermehrt in den Atemwegen wiederfinden lassen. β2-Adrenozeptoren werden bei starker Stimulation von den jeweiligen Zellen (z. B. Typ II Alveolarzellen oder Zellen der glatten Bronchialmuskulatur) internalisiert, d. h. von der Zelloberfläche entfernt, um die Ansprechbarkeit durch den natürlichen Rezeptoragonisten Adrenalin zu senken.
Nach Aktivierung ausreichend vieler β2-Adrenozeptoren kommt es in Folge erhöhter intrazellulärer cAMP-Konzentration zur Phosphorylierung des Rezeptors durch zwei verschiedene Enzyme (PKA und GRK2), die letztlich die Translokation der phosphorylierten Rezeptoren zu sogenannten Coated Pits auslösen, wo in der Folge die Internalisierung der Rezeptoren stattfindet. α-Hederin fungiert als indirekter GRK2-Inhibitor, was bedeutet, dass α-Hederin nicht als GRK2-Blocker zu verstehen ist, sondern vielmehr den Zugang zur Phosphorylierungsstelle des β2-Adrenozeptor für GRK2 soweit erschwert, dass es zu keiner ausreichenden Phosphorylierung kommt.[17] Dadurch wird die Internalisierung verhindert und β2-Adrenozeptoren bleiben in großem Maße auf der Zelloberfläche vorhanden, wo sie die durch Adrenalin vermittelten Effekte (z. B. durch erhöhte cAMP-Konzentrationen bedingte Surfactant-Sekretion und Bronchodilatation) verstärken können.[9]
Auch der Mechanismus der antiinflammatorischen Wirkung wird in einer Beeinflussung des β2-adrenergen Signalwegs vermutet. So gibt es einen positiven Zusammenhang zwischen der Expression von Interleukin-6 (IL-6) und der β2-adrenozeptorvermittelten Expression von β-Arrestin 2. β-Arrestin 2 bindet an den IκBα-NFκB-Komplex, wodurch eine Phosphorylierung durch die IκB Kinase gehemmt wird. Fehlt die Phosphorylierung, kann dieser Komplex nicht gespalten werden, NFκB kann nicht in den Zellkern transloziert werden und das Gen, z. B. das für IL-6, nicht transkribiert werden. Hierdurch wird schließlich weniger IL-6 gebildet. Auch eine Verhinderung der Internalisierung des Toll-Like-Receptor 4 wird diskutiert.[5]
Für die anticancerogene Wirkung von α-Hederin wird seine spezielle Interaktion mit der Membran verantwortlich gemacht, die deren Cholesterolgehalt drastisch zu senken vermag.[18]
Sicherheitshinweise
[Bearbeiten | Quelltext bearbeiten]In höheren Konzentrationen wirkt α-Hederin im Zellversuch hämolytisch (HD50 < 30 µM).[18]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g Datenblatt α-Hederin, analytical standard bei Sigma-Aldrich, abgerufen am 11. Oktober 2017 (PDF).
- ↑ Karen Plé, Martin Chwalek, Laurence Voutquenne-Nazabadioko: Synthesis ofα-Hederin,δ-Hederin, and Related Triterpenoid Saponins. In: European Journal of Organic Chemistry. 2004, 2004, S. 1588, doi:10.1002/ejoc.200300723.
- ↑ R. Keyhanmanesh, S. Saadat, M. Mohammadi, A. A. Shahbazfar, M. Fallahi: The Protective Effect of α-Hederin, the Active Constituent of Nigella sativa, on Lung Inflammation and Blood Cytokines in Ovalbumin Sensitized Guinea Pigs. In: Phytotherapy Research. Band 29, Nummer 11, November 2015, S. 1761–1767, doi:10.1002/ptr.5429, PMID 26292851.
- ↑ M. Fallahi, R. Keyhanmanesh, A. M. Khamaneh, M. A. Ebrahimi Saadatlou, S. Saadat, H. Ebrahimi: Effect of Alpha-Hederin, the active constituent of Nigella sativa, on miRNA-126, IL-13 mRNA levels and inflammation of lungs in ovalbumin-sensitized male rats. In: Avicenna journal of phytomedicine. Band 6, Nummer 1, 2016 Jan-Feb, S. 77–85, PMID 27247924, PMC 4884220 (freier Volltext).
- ↑ a b J. Schulte-Michels, F. Runkel, S. Gokorsch, H. Häberlein: Ivy leaves dry extract EA 575® decreases LPS-induced IL-6 release from murine macrophages. In: Die Pharmazie. Band 71, Nummer 3, März 2016, S. 158–161, PMID 27183712.
- ↑ Y. K. Kim, R. G. Kim, S. J. Park, J. H. Ha, J. W. Choi, H. J. Park, K. T. Lee: In vitro antiinflammatory activity of kalopanaxsaponin A isolated from Kalopanax pictus in murine macrophage RAW 264.7 cells. In: Biological & Pharmaceutical Bulletin. Band 25, Nummer 4, April 2002, S. 472–476, PMID 11995927.
- ↑ S. Saadat, M. Mohammadi, M. Fallahi, R. Keyhanmanesh, M. R. Aslani: The protective effect of α-hederin, the active constituent of Nigella sativa, on tracheal responsiveness and lung inflammation in ovalbumin-sensitized guinea pigs. In: The Journal of Physiological Sciences. Band 65, Nummer 3, Mai 2015, S. 285–292, doi:10.1007/s12576-015-0367-6, PMID 25752254.
- ↑ M. Mendel, M. Chłopecka, N. Dziekan, W. Karlik, M. Wiechetek: Participation of extracellular calcium in α-hederin-induced contractions of rat isolated stomach strips. In: Journal of Ethnopharmacology. Band 146, Nummer 1, März 2013, S. 423–426, doi:10.1016/j.jep.2012.12.023, PMID 23274745.
- ↑ a b c A. Sieben, L. Prenner, T. Sorkalla, A. Wolf, D. Jakobs, F. Runkel, H. Häberlein: Alpha-hederin, but not hederacoside C and hederagenin from Hedera helix, affects the binding behavior, dynamics, and regulation of beta 2-adrenergic receptors. In: Biochemistry. Band 48, Nummer 15, April 2009, S. 3477–3482, doi:10.1021/bi802036b, PMID 19278262.
- ↑ A. Trute, J. Gross, E. Mutschler, A. Nahrstedt: In vitro antispasmodic compounds of the dry extract obtained from Hedera helix. In: Planta medica. Band 63, Nummer 2, April 1997, S. 125–129, doi:10.1055/s-2006-957627, PMID 9140224.
- ↑ A. Wolf, R. Gosens, H. Meurs, H. Häberlein: Pre-treatment with α-hederin increases β-adrenoceptor mediated relaxation of airway smooth muscle. In: Phytomedicine : international journal of phytotherapy and phytopharmacology. Band 18, Nummer 2–3, Januar 2011, S. 214–218, doi:10.1016/j.phymed.2010.05.010, PMID 20637581.
- ↑ I. Gülçin, V. Mshvildadze, A. Gepdiremen, R. Elias: Antioxidant activity of saponins isolated from ivy: alpha-hederin, hederasaponin-C, hederacolchiside-E and hederacolchiside-F. In: Planta medica. Band 70, Nummer 6, Juni 2004, S. 561–563, PMID 15241892.
- ↑ T. A. Prescott, L. P. Rigby, N. C. Veitch, M. S. Simmonds: The haploinsufficiency profile of α-hederin suggests a caspofungin-like antifungal mode of action. In: Phytochemistry. Band 101, Mai 2014, S. 116–120, doi:10.1016/j.phytochem.2014.01.022, PMID 24569176.
- ↑ M. A. Randhawa, M. S. Alghamdi: Anticancer activity of Nigella sativa (black seed) - a review. In: The American Journal of Chinese Medicine. Band 39, Nummer 6, 2011, S. 1075–1091, doi:10.1142/S0192415X1100941X, PMID 22083982.
- ↑ J. H. Lorent, C. Léonard, M. Abouzi, F. Akabi, J. Quetin-Leclercq, M. P. Mingeot-Leclercq: α-Hederin Induces Apoptosis, Membrane Permeabilization and Morphologic Changes in Two Cancer Cell Lines Through a Cholesterol-Dependent Mechanism. In: Planta medica. Band 82, Nummer 18, Dezember 2016, S. 1532–1539, doi:10.1055/s-0042-114780, PMID 27574896.
- ↑ F. Delmas, C. Di Giorgio, R. Elias, M. Gasquet, N. Azas, V. Mshvildadze, G. Dekanosidze, E. Kemertelidze, P. Timon-David: Antileishmanial activity of three saponins isolated from ivy, alpha-hederin, beta-hederin and hederacolchiside A1, as compared to their action on mammalian cells cultured in vitro. In: Planta medica. Band 66, Nummer 4, Mai 2000, S. 343–347, doi:10.1055/s-2000-8541, PMID 10865451.
- ↑ J. Schulte-Michels, A. Wolf, S. Aatz, K. Engelhard, A. Sieben, M. Martinez-Osuna, F. Häberlein, H. Häberlein: α-Hederin inhibits G protein-coupled receptor kinase 2-mediated phosphorylation of β2-adrenergic receptors. In: Phytomedicine : international journal of phytotherapy and phytopharmacology. Band 23, Nummer 1, Januar 2016, S. 52–57, doi:10.1016/j.phymed.2015.12.001, PMID 26902407.
- ↑ a b K. Wojciechowski, M. Orczyk, T. Gutberlet, T. Geue: Complexation of phospholipids and cholesterol by triterpenic saponins in bulk and in monolayers. In: Biochimica et Biophysica Acta. Band 1858, Nummer 2, Februar 2016, S. 363–373, doi:10.1016/j.bbamem.2015.12.001, PMID 26654784.


 French
French Deutsch
Deutsch