Diazoniumsalze – Wikipedia
| Diazoniumsalze (Auswahl) |
|---|
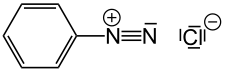 Phenyldiazoniumchlorid (aromatisches Diazoniumsalz) in Wasser bei 0 °C etwas haltbar |
Methandiazoniumchlorid (aliphatisches Diazoniumsalz) sehr unbeständig |
Diazoniumsalze sind eine Stoffklasse organisch-chemischer Verbindungen mit der allgemeinen Strukturformel Ar–N2+ X−. Dabei steht Ar für eine organische, aromatische Arylgruppe und X− steht für ein nicht näher spezifiziertes Anion. Die einfachsten Vertreter dieser Stoffgruppe sind die bei niedrigen Temperaturen einigermaßen stabilen Phenyldiazonium-Salze. Aliphatische Diazoniumsalze sind instabil. Beim Erhitzen (Thermolyse) oder beim Bestrahlen (Photolyse) entstehen, unter Abspaltung von Stickstoff (N2), Carbene.[1]
Darstellung
[Bearbeiten | Quelltext bearbeiten]Aromatische Diazoniumsalze lassen sich durch Diazotierung primärer aromatischer Amine mit Nitrit im sauren Milieu bei tiefer Temperatur darstellen.
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Reine Diazoniumsalze sind instabil, teilweise explosiv und lassen sich nur in wässriger Lösung (bei Temperaturen < 5 °C) handhaben. Beim Versuch, die Salze wasserfrei zu erhalten zerfallen sie explosiv, lassen sich aber mit sterisch anspruchsvollen Anionen stabilisieren und dann isolieren.
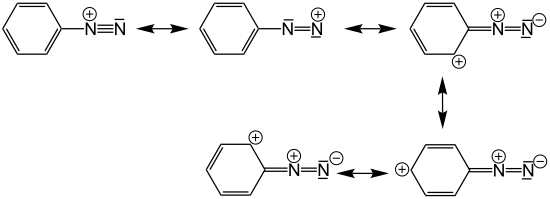
Aromatische Diazoniumsalze (hier das Phenyldiazonium-Kation) sind wegen der möglichen Mesomeriestabilisierung der positiven Ladung deutlich stabiler als aliphatische Diazoniumsalze:
Verwendung
[Bearbeiten | Quelltext bearbeiten]- Aromatische Diazoniumsalze sind Zwischenprodukte bei der Synthese aromatischer Verbindungen durch den Angriff von Nucleophilen, z. B. bei der sogenannten Verkochung, bei der Phenole gebildet werden, oder bei der Sandmeyer-Reaktion, die zu halogenierten Aromaten oder zu aromatischen Nitrilen führt.
- Als schwach elektrophile Reagentien greifen aromatische Diazoniumkationen andere Aromaten an elektronenreichen Positionen an. Bei dieser Reaktion, der sogenannten Azokupplung, werden dann Azofarbstoffe gebildet.
- Bei der Diazotierung von chiralen α-Aminosäuren treten Diazoniumsalze als Zwischenprodukte auf, die in wässriger Lösung stereoselektiv zu α-Hydroxycarbonsäuren gleicher Konfiguration reagieren.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Siegfried Hauptmann: Organische Chemie, Verlag Harri Deutsch, 1985, S. 531, ISBN 3-87144-902-4.


 French
French Deutsch
Deutsch