Cromatografía , la enciclopedia libre


La cromatografía es un método físico de separación para la caracterización de mezclas complejas cuyo objetivo es separar los distintos componentes, la cual tiene aplicación en todas las ramas de la ciencia; en el principio de retención selectiva, cuyo objetivo es separar los distintos componentes de una mezcla, permitiendo identificar y determinar las cantidades de dichos componentes. Diferencias sutiles en el coeficiente de partición de los compuestos dan como resultado una retención diferencial sobre la fase estacionaria y, por tanto, una separación efectiva en función de los tiempos de retención de cada componente de la mezcla.
La cromatografía puede cumplir dos funciones básicas que no se excluyen mutuamente:
- Separar los componentes de la mezcla, para obtenerlos más puros y que puedan ser usados posteriormente (etapa final de muchas síntesis).
- Medir la proporción de los componentes de la mezcla (finalidad analítica). En este caso, las cantidades de material empleadas suelen ser muy pequeñas.
La cromatografía puede ser "preparativa" o "analítica". El propósito de la cromatografía preparativa es separar los componentes de una mezcla para su uso posterior, por lo que es una forma de purificación.[1][2] Este proceso está asociado a costes más elevados debido a su modo de producción.[3][4] La cromatografía analítica se realiza normalmente con cantidades más pequeñas de material y sirve para establecer la presencia o medir las proporciones relativas de analitos en una mezcla. Los dos tipos no son mutuamente excluyentes.[5].
Etimología
[editar]Cromatografía deriva del griego χρῶμα chroma, que significa "color", y γράφειν graphein, que significa "escribir". La combinación de estos dos términos se heredó directamente de la invención de la técnica utilizada por primera vez para separar pigmentos.[6]
Historia
[editar]La cromatografía, (proviene del griego χρῶμα chrōma y γράφω gráphō, que significan respectivamente "color" y "escribir, registrar", literalmente "escritura de color", o "registro de color") , fue empleada originalmente con sustancias coloreadas.
Ya en 1850, Runge describió la formación de zonas coloreadas cuando se depositaban gotas de sustancias colorantes sobre papel secante, pero el desarrollo más importante vino con los experimentos de Mijaíl Tsvet[7] [8](1872-1919), que empleó por primera vez en 1906 el término "cromatografía". A comienzos del año 1903, Mijaíl Tsvet, botánico ruso, logró separar una mezcla de pigmentos de plantas (clorofilas) en una columna de carbonato de calcio. Más tarde, en 1910, cromatografió un extracto de yema de huevo en una columna de inulina. Sus investigaciones, sin embargo, no fueron utilizadas por otros investigadores hasta 1931. Esta demora quizá se debió al hecho de que los trabajos de Tsvet fueron publicados en ruso y en una revista que no tenía amplia circulación.
El rápido desarrollo de la cromatografía como herramienta analítica sensible no ocurrió hasta 1931, cuando Kuhn, con Lederer y con Winterstein, emplearon la técnica para el análisis de pigmentos de plantas, confirmando los primeros trabajos de Tsvet y su predicción de que el caroteno no era una sola sustancia, sino una mezcla de varios homólogos estrechamente relacionados. Al mismo tiempo, el tamaño de las columnas empleadas fue aumentando para poder recuperar los componentes separados. La técnica, por lo tanto, no era solo analítica sino preparatoria.
Por aquel entonces la cromatografía en columna tenía aplicaciones limitadas, dado que los componentes que se podían separar eran invariablemente lípidos. Pasaron 10 años antes de que A. J. P. Martin y R. L. M. Synge desarrollaran una técnica mediante la cual se pudieran separar compuestos acuosos o hidrofílicos. Esto marcó un nuevo interés en la técnica y en 1944 Consden, Gordon y Martin lograron separar mezclas complejas de aminoácidos en papel. Al poco tiempo, en 1947, en Estados Unidos, la Comisión de Energía Atómica dio a conocer información sobre el uso de la cromatografía de intercambio iónico para la separación de productos de fisión nuclear. También por entonces, en esa misma década de 1940, Martin y Synge apuntaron la posibilidad de que la fase móvil pudiera ser un gas y años después, en 1951, el propio Martin, junto con su colaborador A. T. James publicaron un trabajo en el que se describía el primer cromatógrafo de gases. En los siguientes años, la cromatografía de gases se convertiría en la técnica cromatográfica más eficaz para analizar sustancias volátiles, siendo la industria petroquímica una de las más beneficiadas por este avance[8]. Años después, en 1952, A. J. P. Martin y R. L. M. Synge recibirían el Premio Nobel de Química por sus contribuciones a la cromatografía, dada la gran importancia que adquirió esta técnica.
El desarrollo más reciente en el campo de la cromatografía se deriva de los trabajos de Stahl, quien en 1956 presentó una técnica práctica mediante la que una capa delgada sílice gel, celulosa o alúmina era diseminada sobre una placa de vidrio. Esta técnica, llamada cromatografía de capa fina, resultó ser un método de análisis más rápido y más sensible para el examen de mezclas complejas y, en muchos casos, ha sustituido a otros métodos similares más antiguos de cromatografía en papel toche.
En 1959, Porath y Flodin introdujeron una nueva técnica llamada cromatografía de filtración de gel. Esta se ha convertido en una nueva y poderosa herramienta para la separación de sustancias de alto peso molecular, particularmente las proteínas, y ha encontrado muchas aplicaciones en los campos de la bioquímica, la medicina, la fisiología y la biología. La mayoría de las técnicas de filtración en gel utilizan columnas y recientemente se han hecho trabajos con una combinación de filtración en gel y materiales de intercambio iónico, logrando que las separaciones complejas sean extremadamente rápidas y eficientes.
Los primeros equipos de cromatografía de gases aparecieron en el mercado a mediados del siglo XX. A su vez, la cromatografía líquida de alta resolución (HPLC High Performance Liquid Chromatography, en inglés) comenzó a desarrollarse en los años 1960, aumentando su importancia en las décadas siguientes, hasta convertirse en la técnica cromatográfica más empleada. Sin embargo esto se irá modificando con el paso de los años.
Clasificación de los métodos de separación en cromatografía
[editar]Las distintas técnicas cromatográficas[9] pueden dividirse según cómo esté dispuesta la fase estacionaria:
- Cromatografía plana. La fase estacionaria se sitúa sobre una placa plana o sobre un papel. Las principales técnicas son:
- Cromatografía en columna. La fase estacionaria se sitúa dentro de una columna. Según el fluido empleado como fase móvil se distinguen:
La cromatografía de gases se aplica a numerosos compuestos orgánicos, ya que es muy útil en muestras que contienen compuestos volátiles que no descomponen a la temperatura del punto de ebullición. En algunos casos en que los componentes analitos de la muestra no son no volátiles o se descomponen a las temperaturas de trabajo de la técnica, se recurre a procesos denominados de "derivatización", a fin de convertirlos en otros compuestos que se volatilicen en las condiciones de análisis sin degradarse.
Dentro de la cromatografía líquida, destaca la cromatografía líquida de alta resolución (HPLC, del inglés High Performance Liquid Chromatography), que es la técnica cromatográfica más empleada en la actualidad, normalmente en su modalidad de fase reversa, en la que la fase estacionaria tiene carácter no polar, y la fase móvil posee carácter polar (generalmente agua o mezclas con elevada proporción de la misma o de otros disolvente polares, como por ejemplo, metanol). El nombre de "reversa" viene dado porque tradicionalmente la fase estacionaria estaba compuesta de sílice o alúmina, de carácter polar, y por tanto la fase móvil era un disolvente orgánico poco polar. Una serie eluotrópica es un rango de sustancias de diferentes polaridades que actúan como fase móvil y que permiten observar un mejor desplazamiento sobre una fase estacionaria.

| Tipos | Fase móvil | Fase estacionaria |
| Cromatografía en papel | Líquido | Papel de celulosa. |
| Cromatografía en capa fina | Líquido | Gel de sílice o alúmina. |
| Cromatografía de gases | Gas | Columnas capilares de sílice fundida, con recubrimientos internos de varios tipos de siloxanos enlazados, columnas empaquetadas con tierras diatomeas hechas de tubos de vidrio o metal. |
| Cromatografía líquida en fase reversa | Líquido (polar) | Relleno de siloxano de octilo o siloxano de octadecilo. |
| Cromatografía líquida en fase normal | Líquido (menos polar) | Relleno de sílice, alúmina o un soporte al que se unen químicamente grupos polares (ciano, amino, etc). |
| Cromatografía líquida de intercambio iónico | Líquido (polar) | Resinas de intercambio iónico. |
| Cromatografía líquida de exclusión | Líquido | Relleno de pequeñas partículas de sílice o polímeros con red de poros uniforme. |
| Cromatografía líquida de adsorción | Líquido | Partículas finamente divididas de sílice o de alúmina. |
| Cromatografía de fluidos supercríticos | Líquido | Columnas abiertas de sílice fundida con recubrimientos internos de varios tipos de siloxanos enlazados y de enlaces cruzados. |
Términos empleados en cromatografía
[editar]Como en cualquier técnica o metodología científica, la cromatografía emplea una terminología concreta de amplio uso entre los profesionales usuarios de dichas técnica[10][11]
- Analito es la sustancia que se va a separar durante la cromatografía.
- Fase móvil es la fase que se mueve en una dirección definida. Puede ser un líquido (cromatografía de líquidos o CEC), un gas (cromatografía de gases) o un fluido supercrítico (cromatografía de fluidos supercríticos). La muestra que se está separando/analizando (formada de analito/s y el disolvente) se inyecta en la fase móvil que se mueve a través de la columna. En el caso de la cromatografía líquida de alta resolución, HPLC, la fase móvil es un disolvente no polar como el hexano (fase normal) o bien algún disolvente polar (cromatografía de fase reversa).
- Fase estacionaria es la sustancia que está fija en una posición durante la cromatografía. Un ejemplo es la capa de gel de sílice en la cromatografía en capa fina.
- Cromatografía analítica se emplea para determinar la existencia y posiblemente también la concentración de un analito en una muestra.
- Fase enlazada es una fase estacionaria que se une de forma covalente a las partículas de soporte o a las paredes internas de la columna.
- Cromatograma es el resultado gráfico de la cromatografía. En el caso de separación óptima, los diferentes picos o manchas del cromatograma se corresponden a los componentes de la mezcla separada.
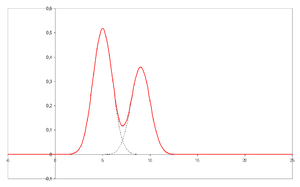
Cromatograma con picos no resueltos (separados). 
Cromatograma con dos picos resueltos. - En el eje X se representa el tiempo de retención, y en el eje Y una señal (obtenida, por ejemplo, a partir de un espectrofotómetro, un espectrómetro de masas o cualquier otro de los diversos detectores) correspondiente a la respuesta creada por los diferentes analitos existentes en la muestra. En el caso de un sistema óptimo, la señal es proporcional a la concentración del analito específico separado.
- Cromatógrafo es el equipo que permite una separación sofisticada. Por ejemplo, un cromatógrafo de gases o un cromatógrafo de líquidos.
- Cromatografía es el método físico de separación en el cual los componentes que se van a separar se distribuyen entre dos fases, una de las cuales es estacionaria (fase estacionaria) mientras la otra (la fase móvil) se mueve en una dirección definida.
- Eluyente es la fase móvil que atraviesa la columna.
- Serie eluotrópica es una lista de disolventes clasificados según su poder de dilución.
- Fase inmovilizada es una fase estacionaria que está inmovilizada sobre partículas de soporte, o en la pared interior del tubo contenedor o columna.

- Cromatografía preparativa se usa para purificar suficiente cantidad de sustancia para un uso posterior, más que para análisis.
- Tiempo de retención es el tiempo característico que tarda un analito particular en pasar a través del sistema (desde la columna de entrada hasta el detector) bajo las condiciones fijadas. Véase también: Índice de retención de Kovats
- Muestra es la materia que va a ser analizada en la cromatografía. Puede consistir en un simple componente o una mezcla de varios. Cuando la mezcla es tratada en el curso del análisis, la fase o fases que contienen los analitos de interés es llamada igualmente muestra mientras el resto de sustancias cuya separación no resulta de interés es llamada residuo.
- Soluto es cada uno de los componentes de la muestra que va a ser separado.
- Disolvente es toda sustancia capaz de solubilizar a otra,y especialmente la fase móvil líquida en cromatografía de líquidos.
- Capacidad de carga Es la cantidad máxima de muestra que puede ser separada en una sola carga.
- Capacidad de fraccionamiento Es el número máximo de componentes que pueden ser separados en una sola operación.
- Selectividad Es la capacidad de poder discriminar y distinguir entre dos componentes.
Técnicas por la forma del lecho cromatográfico
[editar]Cromatografía en columna
[editar]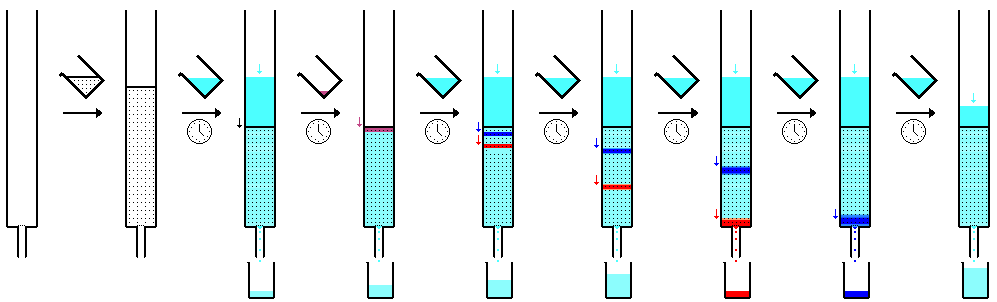 La cromatografía en columna es una técnica de separación en la que el lecho estacionario se encuentra dentro de un tubo. Las partículas de la fase estacionaria sólida o el soporte recubierto con una fase estacionaria líquida pueden llenar todo el volumen interior del tubo (columna empaquetada) o concentrarse en o a lo largo de la pared interior del tubo dejando un camino abierto y sin restricciones para la fase móvil en la parte central del tubo (columna tubular abierta). Las diferencias en las velocidades de movimiento a través del medio se calculan a diferentes tiempos de retención de la muestra[11][12]. En 1978, W. Clark Still introdujo una versión modificada de la cromatografía en columna denominada cromatografía en columna flash (flash).[13][14] La técnica es muy similar a la cromatografía en columna tradicional, excepto que el disolvente es conducido a través de la columna aplicando presión positiva. Esto permitió realizar la mayoría de las separaciones en menos de 20 minutos, con separaciones mejoradas en comparación con el método antiguo. Los sistemas modernos de cromatografía flash se venden como cartuchos de plástico preenvasados, y el disolvente se bombea a través del cartucho. Los sistemas también pueden conectarse con detectores y colectores de fracciones que proporcionan automatización. La introducción de bombas de gradiente dio lugar a separaciones más rápidas y a un menor uso de disolventes.
La cromatografía en columna es una técnica de separación en la que el lecho estacionario se encuentra dentro de un tubo. Las partículas de la fase estacionaria sólida o el soporte recubierto con una fase estacionaria líquida pueden llenar todo el volumen interior del tubo (columna empaquetada) o concentrarse en o a lo largo de la pared interior del tubo dejando un camino abierto y sin restricciones para la fase móvil en la parte central del tubo (columna tubular abierta). Las diferencias en las velocidades de movimiento a través del medio se calculan a diferentes tiempos de retención de la muestra[11][12]. En 1978, W. Clark Still introdujo una versión modificada de la cromatografía en columna denominada cromatografía en columna flash (flash).[13][14] La técnica es muy similar a la cromatografía en columna tradicional, excepto que el disolvente es conducido a través de la columna aplicando presión positiva. Esto permitió realizar la mayoría de las separaciones en menos de 20 minutos, con separaciones mejoradas en comparación con el método antiguo. Los sistemas modernos de cromatografía flash se venden como cartuchos de plástico preenvasados, y el disolvente se bombea a través del cartucho. Los sistemas también pueden conectarse con detectores y colectores de fracciones que proporcionan automatización. La introducción de bombas de gradiente dio lugar a separaciones más rápidas y a un menor uso de disolventes.
En la adsorción en lecho expandido, se utiliza un lecho fluidizado, en lugar de una fase sólida formada por un lecho empaquetado. Esto permite omitir los pasos iniciales de limpieza, como la centrifugación y la filtración, para caldos de cultivo o lodos de células rotas.
La cromatografía de fosfocelulosa utiliza la afinidad de unión de muchas proteínas de unión al ADN por la fosfocelulosa. Cuanto más fuerte sea la interacción de una proteína con el ADN, mayor será la concentración de sal necesaria para eluir esa proteína.[15]
Cromatografía plana
[editar]La cromatografía plana es una técnica de separación en la que la fase estacionaria está presente como o sobre un plano. El plano puede ser un papel, sirviendo como tal o impregnado por una sustancia como lecho estacionario (cromatografía en papel) o una capa de partículas sólidas extendidas sobre un soporte como una placa de vidrio (cromatografía en capa fina). Los distintos compuestos de la mezcla de la muestra recorren distancias diferentes en función de la fuerza con la que interaccionan con la fase estacionaria en comparación con la fase móvil. El factor de retención específico (Rf) de cada compuesto químico puede utilizarse para ayudar en la identificación de una sustancia desconocida.
Cromatografía en papel
[editar]

La cromatografía en papel es una técnica que consiste en colocar un pequeño punto o línea de muestra solución sobre una tira de cromatografía en papel. El papel se coloca en un recipiente con una capa poco profunda de disolvente y se sella. A medida que el disolvente asciende por el papel, se encuentra con la mezcla de la muestra, que comienza a ascender por el papel con el disolvente. Este papel está hecho de celulosa, una polar, y los compuestos dentro de la mezcla viajan más lejos si son menos polares. Las sustancias más polares se adhieren más rápidamente al papel de celulosa y, por lo tanto, no llegan tan lejos.
Cromatografía en capa fina (TLC)
[editar]
La cromatografía en capa fina (TLC) es una técnica de laboratorio ampliamente utilizada para separar diferentes sustancias bioquímicas en función de sus atracciones relativas a las fases estacionaria y móvil. Es similar a la cromatografía en papel. Sin embargo, en lugar de utilizar una fase estacionaria de papel, utiliza una fase estacionaria de una fina capa de adsorbente como gel de sílice, alúmina o celulosa sobre un sustrato plano e inerte. La TLC es muy versátil; se pueden separar múltiples muestras simultáneamente en la misma capa, lo que la hace muy útil para aplicaciones de cribado como el análisis de los niveles de fármacos y la pureza del agua.[16] La posibilidad de contaminación cruzada es baja, ya que cada separación se realiza en una capa nueva. En comparación con el papel, tiene la ventaja de que los ciclos son más rápidos, las separaciones mejores, los análisis cuantitativos mejores y la posibilidad de elegir entre diferentes adsorbentes. Para una resolución aún mejor y una separación más rápida que utilice menos disolvente, se puede utilizar la TLC de alto rendimiento. Un uso popular más antiguo había sido diferenciar cromosomas observando la distancia en el gel (la separación de era un paso separado).
Cromatografía de desplazamiento
[editar]El principio básico de la cromatografía de desplazamiento es: Una molécula con alta afinidad por la matriz cromatográfica (el desplazante) compite eficazmente por los sitios de unión, y por tanto desplaza a todas las moléculas con afinidades menores.[17] Existen diferencias claras entre la cromatografía de desplazamiento y la de elución. En el modo de elución, las sustancias suelen emerger de una columna en picos estrechos y gaussianos. Se desea una separación amplia de los picos, preferiblemente hasta la línea de base, para obtener la máxima purificación. La velocidad a la que cualquier componente de una mezcla desciende por la columna en el modo de elución depende de muchos factores. Pero para que dos sustancias viajen a velocidades diferentes, y por tanto se resuelvan, debe haber diferencias sustanciales en alguna interacción entre las biomoléculas y la matriz cromatográfica. Los parámetros de funcionamiento se ajustan para maximizar el efecto de esta diferencia. En muchos casos, la separación basal de los picos sólo puede lograrse con elución en gradiente y cargas bajas de la columna. Así pues, dos inconvenientes de la cromatografía en modo de elución, especialmente a escala preparativa, son la complejidad operativa, debida al bombeo de disolvente en gradiente, y el bajo rendimiento, debido a las bajas cargas de las columnas. La cromatografía de desplazamiento tiene ventajas sobre la cromatografía de elución en el sentido de que los componentes se resuelven en zonas consecutivas de sustancias puras en lugar de "picos". Dado que el proceso aprovecha la no linealidad de las isotermas, se puede separar una mayor alimentación de columna en una columna dada con los componentes purificados recuperados en concentraciones significativamente más altas.
Técnicas por estado físico de la fase móvil
[editar]Cromatografía de gases
[editar]La cromatografía de gases (GC), también conocida a veces como cromatografía gas-líquido, (GLC), es una técnica de separación en la que la fase móvil es un gas. La separación cromatográfica de gases se realiza siempre en una columna, que suele ser "empaquetada" o "capilar". Las columnas de relleno son los caballos de batalla rutinarios de la cromatografía de gases, ya que son más baratas y fáciles de usar y suelen ofrecer un rendimiento adecuado. Las columnas capilares suelen ofrecer una resolución muy superior y, aunque son más caras, cada vez se utilizan más, sobre todo para mezclas complejas. Además, las columnas capilares pueden dividirse en tres clases: tubulares abiertas de capa porosa (PLOT), tubulares abiertas recubiertas de pared (WCOT) y tubulares abiertas recubiertas de soporte (SCOT). Las columnas PLOT son únicas en el sentido de que la fase estacionaria se adsorbe a las paredes de la columna, mientras que las columnas WCOT tienen una fase estacionaria unida químicamente a las paredes. Las columnas SCOT son en cierto modo la combinación de los dos tipos mencionados en el sentido de que tienen partículas de soporte adheridas a las paredes de la columna, pero esas partículas tienen fase líquida unida químicamente a ellas.[18] Ambos tipos de columnas están fabricadas con materiales no adsorbentes y químicamente inertes. El acero inoxidable y el vidrio son los materiales habituales para las columnas empaquetadas y el cuarzo o la sílice fundida para las columnas capilares.
Cromatografía líquida
[editar]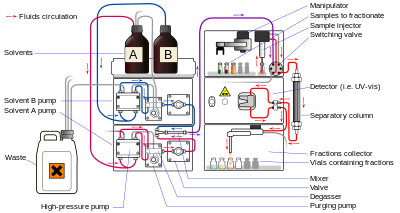
La cromatografía líquida (CL) es una técnica de separación en la que la fase móvil es un líquido. Puede realizarse en columna o en plano. La cromatografía líquida actual, que generalmente utiliza partículas de relleno muy pequeñas y una presión relativamente alta, se denomina cromatografía líquida de alta eficacia.
En la HPLC la muestra es forzada por un líquido a alta presión (la fase móvil) a través de una columna que está empaquetada con una fase estacionaria compuesta de partículas de forma irregular o esférica, una capa monolítica porosa, o una membrana porosa. Los monolitos son "medios cromatográficos esponjosos"[19] y están formados por un bloque interminable de partes orgánicas o inorgánicas. La HPLC se divide históricamente en dos subclases diferentes basadas en la polaridad de las fases móvil y estacionaria. Los métodos en los que la fase estacionaria es más polar que la fase móvil (por ejemplo, tolueno como fase móvil, sílice como fase estacionaria) se denominan cromatografía líquida de fase normal (NPLC) y lo contrario (por ejemplo, mezcla de agua y metanol como fase móvil y C18 (octadecilsilil) como fase estacionaria) se denomina cromatografía líquida de fase inversa (RPLC).
Véase también
[editar] Wikimedia Commons alberga una categoría multimedia sobre Cromatografía.
Wikimedia Commons alberga una categoría multimedia sobre Cromatografía.- Proceso de separación
- Serie eluotrópica
- Cromatografía de gases
- Cromatografía en capa fina
- Cromatografía de inmunoafinidad
Referencias
[editar]- ↑ González-González, Mirna; Mayolo-Deloisa, Karla; Rito-Palomares, Marco (1 de enero de 2020), «Capítulo 5 - Avances recientes en la cromatografía monolítica basada en anticuerpos para aplicaciones terapéuticas», en Matte, Allan, ed., Aproximaciones a la purificación, análisis y caracterización de terapias basadas en anticuerpos (en inglés) (Elsevier): 105-116, ISBN 978-0-08-103019-6, S2CID 226450210.
- ↑ Alternative bioseparation operations: life beyond packed-bed chromatography T.M. Przybycien, N.S. Pujar y L.M. Steele Curr Opin Biotechnol, 15 (5) (2004), pp. 469-478
- ↑ Ongkudon, Clarence M.; Kansil, Tamar; Wong, Charlotte (2014). «Desafíos y estrategias en la preparación de adsorbentes cromatográficos monolíticos de gran volumen basados en polímeros». Journal of Separation Science 37 (5): 455-464. ISSN 1615-9314. PMID 24376196. doi:10.1002/jssc.201300995.
- ↑ González-González, Mirna; Mayolo-Deloisa, Karla; Rito-Palomares, Marco (1 de enero de 2020), «Capítulo 5 - Avances recientes en cromatografía monolítica basada en anticuerpos para aplicaciones terapéuticas», en Matte, Allan, ed., Aproximaciones a la purificación, Analysis and Characterization of Antibody-Based Therapeutics (en inglés) (Elsevier): 105-116, ISBN 978-0-08-103019-6, S2CID 226450210.
- ↑ Hostettmann K, Marston A, Hostettmann M (1998). Técnicas de cromatografía preparativa aplicaciones en el aislamiento de productos naturales (Second edición). Berlin, Heidelberg: Springer Berlin Heidelberg. p. 50. ISBN 9783662036310.
- ↑ Harper, Douglas. «chromatography». Online Etymology Dictionary.
- ↑ La cromatografía. Fundamentos de tecnología de productos fitoterapéuticos. Nikolai Sharapin. Editorial Convenio Andrés Bello, 2000. ISBN 9586980014. Pág. 159-190.l
- ↑ a b Polo, Luis M. (2015). «Cap. 1.5. Reseña histórica de la cromatografía». Fundamentos de cromatografía. Dextra Editorial. p. 27. ISBN 978-84-16277-58-2.
- ↑ Técnicas de bioquímica y biología molecular. Jorge David Roriguez Miranda. Editorial Reverté, 1991. ISBN 8429118195. Cap. 8: Cromatografía. Pág. 179
- ↑ Glosario de los términos más usados en cromatografía. Introducción a la Cromatagrafía. Stella Torres de Young. Ediciones de la Univ. Nacional de Colombia. ISBN 9581701192. Pág. 15
- ↑ a b Ettre, L. S. (1995). Nomenclatura para cromatografía. Madrid: GCTA (RSEQ). ISBN 84-605-2385-3.
- ↑ Manish T. «¿Cómo funciona la cromatografía en columna?». BrightMags. Archivado desde el original el 21 de abril de 2017. Consultado el 7 de abril de 2017.
- ↑ Still WC, Kahn M, Mitra A (1978). «Técnica cromatográfica rápida para separaciones preparativas con resolución moderada». J. Org. Chem. 43 (14): 2923-2925.
- ↑ Harwood LM, Moody CJ (1989). WileyBlackwell, ed. Química orgánica experimental: Principios y Práctica (Ilustrada edición). pp. 180-185. ISBN 978-0-632-02017-1.
- ↑ Bourgeois S, Pfahl M (1976). «Repressors». En Anfinsen CB, Edsall JT, Richards FM, ed. Avances en Química de Proteínas 30. Academic Press. pp. 6-7. ISBN 978-0-12-034230-3. PMID 779429.
- ↑ Bernard., Fried (2003). Handbook of Thin-Layer Chromatography. Marcel Dekker Inc. ISBN 978-0824748661. OCLC 437068122.
- ↑ Cromatografía de desplazamiento 101 Archivado el 15 de septiembre de 2008 en Wayback Machine.. Sachem, Inc. Austin, TX 78737
- ↑ Rahman, M.; El-Aty, A.M.A.; Choi, J.-H.; Shin, H.-C.; Shin, S.-C.; Shim, J.-H. (Noviembre 2015). «Capítulo 3 Visión general básica sobre columnas de cromatografía de gases». Analytical Separation Science. pp. 823-834. ISBN 9783527333745.
- ↑ González-González, Mirna; Mayolo-Deloisa, Karla; Rito-Palomares, Marco (1 de enero de 2020), «Capítulo 5 - Avances recientes en cromatografía monolítica basada en anticuerpos para aplicaciones terapéuticas», en Matte, Allan, ed., Aproximaciones a la purificación, Analysis and Characterization of Antibody-Based Therapeutics (en inglés) (Elsevier): 105-116, ISBN 978-0-08-103019-6, S2CID 226450210.


 French
French Deutsch
Deutsch
