Phénylalanine ammonia-lyase — Wikipédia
| N° EC | EC |
|---|---|
| N° CAS | |
| Cofacteur(s) | MIO |
| IUBMB | Entrée IUBMB |
|---|---|
| IntEnz | Vue IntEnz |
| BRENDA | Entrée BRENDA |
| KEGG | Entrée KEGG |
| MetaCyc | Voie métabolique |
| PRIAM | Profil |
| PDB | RCSB PDB PDBe PDBj PDBsum |
| GO | AmiGO / EGO |
La phénylalanine ammonia-lyase (PAL), EC , est une enzyme de type lyase présente chez les plantes et les mycètes (champignons). La PAL catalyse la conversion de l'acide aminé phénylalanine en acide cinnamique, avec libération d'ammoniac (NH3) :
Cette réaction est la première étape de la synthèse de produits phytochimiques appelés phénylpropanoïdes.
La PAL appartient à la famille des lyases, plus spécifiquement à la famille des enzymes catalysant les réactions de rupture de liaison carbone-azote (EC 4.3). La PAL participe à 5 voies métaboliques : métabolisme de la tyrosine, métabolisme de la phénylalanine, cycle de l'azote, biosynthèse des phénylpropanoïdes et biosynthèse des alcaloïdes II.
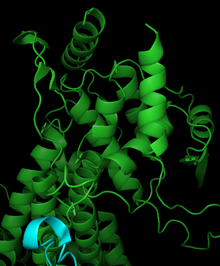
Structure
[modifier | modifier le code]L'enzyme est codée par trois ou quatre gènes, il existe donc dans de nombreuses plantes plusieurs isoformes paralogues. À la date de 2007, 5 structures ont été identifiées pour cette classe d'enzyme, avec les codes PDB 1T6J, 1T6P, 1W27, 1Y2M,, et 2NYF.
Intérêt thérapeutique
[modifier | modifier le code]L'administration de phénylalanine ammonia-lyase à des patients atteints de Phénylcétonurie est actuellement étudiée. En effet, elle permettrait de dégrader la principale cause des symptômes de cette maladie : l'accumulation de Phénylalanine. Cette stratégie thérapeutique potentielle permettrait ainsi de remplacer le régime actuellement imposé aux patients, qui est particulièrement contraignant et difficilement observable.
Notes et références
[modifier | modifier le code]- (en) Joseph C. Calabrese, Douglas B. Jordan, Amechand Boodhoo, Sima Sariaslani et Todd Vannelli, « Crystal Structure of Phenylalanine Ammonia Lyase: Multiple Helix Dipoles Implicated in Catalysis », Biochemistry, vol. 43, no 36, , p. 11403-11416 (lire en ligne) DOI 10.1021/bi049053+


 French
French Deutsch
Deutsch