Quinolone — Wikipédia
Les quinolones et fluoroquinolones[1],[2],[3] forment une large classe d'antibactériens de synthèse qui comprennent les dérivés de l'acide nalidixique découvert en 1962 et utilisé chez l'homme dès l'année suivante. Cette famille d'antibactériens a fait l'objet de recherches très importantes aboutissant au dépôt de plus de 10 000 brevets. L'ajout de l'atome de fluor dans les années 1970 a permis d'augmenter fortement la pénétration des molécules quinolones dans les cellules (jusqu'à 200 fois plus) : ce fut la naissance des fluoroquinolones, puissants antibiotiques capables de lutter contre une grande variété de germes chez l'homme et l'animal.
L'apparition sur le marché dans les années 1980 de la norfloxacine, ofloxacine, ciprofloxacine, péfloxacine et loméfloxacine ont permis aux fluoroquinolones de devenir des antibiotiques de référence pour de nombreuses infections, comme les pyélonéphrites aiguës ou les prostatites. S'ils sont essentiels dans le traitement de certaines infections bactériennes, les fluoroquinolones font toutefois l'objet de précautions d'utilisation, en raison de leurs possibles effets secondaires invalidants, potentiellement graves voire irréversibles[4], touchant notamment les tendons (en particulier les tendons d'Achille), les articulations et le système nerveux (neuropathies dont douleurs neuropathiques). Les mesures de suivi et d'alerte de ces derniers varient selon les pays. Un rapport remis en par l'INAMI, organisme belge de sécurité sociale, montrait, qu'à cette date, la principale indication de prescription des fluoroquinolones concerne les infections (ou risque d'infection) des voies aériennes.
Usage et évolution des molécules
[modifier | modifier le code]Près de la moitié des quinolones mises sur le marché se sont vu retirer ou restreindre leur licence d'utilisation, mais vers 1998, les ventes de fluoroquinolones augmentent et vont même exploser à partir de 2001, avec l'apparition de produits de nouvelle génération.
Fin 2001, la psychose du bioterrorisme, après les attentats du , pousse nombre de gens à se protéger du bacille du charbon à l'aide de produits à base de ciprofloxacine ou d'ofloxacine, multipliant les ventes quotidiennes de ces antibiotiques par 10. C'est ce que certains ont appelé l'heure de gloire des fluoroquinolones.
En , le Comité Economique des Produits de Santé estimera que les fluoroquinolones sont trop prescrites en France, et exigera des laboratoires fabricants que le temps de visite médicale qui leur est consacré soit réduit de 30 % sur trois ans.
La recherche vise aujourd'hui de nouvelles générations de quinolones à spectre d'action encore élargi, mais avec moins d'effets secondaires. Des applications anti-cancéreuses sont actuellement explorées.
Mode d'action et efficacité des fluoroquinolones
[modifier | modifier le code]Mode d'action
[modifier | modifier le code]
Les quinolones ciblent l'ADN gyrase et les topoisomérases II et IV, empêchant la réplication de l'ADN bactérien. Leur mode d'action comprend un effet oxydant sur les bactéries, mais leur effet principal est dû à la fixation de la molécule quinolone sur l'ADN lors de la phase de réplication de l'ADN (phase S) précédant la division cellulaire. La topoisomérase II est la protéine qui permet à une bactérie ne mesurant que 2 μm sur 1 μm en moyenne de contenir un ADN long de 1 700 μm (effet de surenroulement de l'ADN sur lui-même). L'inhibition de la topoisomérase II induit des cassures dans l'ADN (effet clastogène). Les quinolones se fixent par ailleurs sur les extrémités des brins d'ADN qui ne peuvent plus se réassembler. Cette formation d'un complexe ADN-quinolones est irréversible. L'étape suivante est celle de la mort cellulaire programmée (apoptose). Il semble cependant que dans de nombreux cas, la bactérie ne meure pas immédiatement : encore présente dans l'organisme, elle ne peut plus se reproduire. Cela pourrait expliquer le remarquable effet post-antibiotique que l'on observe avec les fluoroquinolones, effet qu'aucune étude n'explique de manière satisfaisante à ce jour.
Classification des quinolones
[modifier | modifier le code]Les quinolones sont habituellement classées en première, seconde, troisième et quatrième génération. Les molécules de la seconde à la quatrième génération intègrent au moins un atome de fluor dans leur structure et prennent le nom de fluoroquinolones.
Les molécules de la seconde à la quatrième génération se distinguent de la première génération par une meilleure pénétration sérique et tissulaire. Leur spectre d’activité, initialement limité aux bactéries à Gram négatif aérobies, s’est étendu successivement aux bactéries à Gram positif et aux anaérobies[5]. Cependant dans chaque génération de nombreuses molécules ont été retirées du marché ou ont vu leur usage restreint à cause de leurs effets indésirables graves. La signalétique suivante identifie le statut de chaque molécule :
- Le signe † suivi d’un numéro CAS indique les molécules dont le développement a été stoppé.
- Le signe † suivi d’un nom commercial indique les spécialités retirées du marché.
- Le signe ‡ indique les spécialités dont l’usage est restreint aux cas d’échec ou d’impossibilité des autres options thérapeutiques.
Seules la ciprofloxacine et la lévofloxacine sont autorisées sans restriction d’usage à la fois en Europe, aux États-Unis et en Asie. Aux États-Unis elles restent toutefois soumises aux « avertissements encadrés de noir » mentionnés plus loin dans cet article. Malgré ses effets indésirables et compte tenu des services rendus, la ciprofloxacine figure dans la liste des « médicaments essentiels » dressée par l’OMS (Organisation mondiale de la santé). L’ofloxacine et la lévofloxacine sont également citées dans cette liste mais uniquement comme médicaments seconde ligne pour le traitement des tuberculoses multirésistantes[6].
1re génération
[modifier | modifier le code]Les quinolones de la première génération incluent l’acide nalidixique et d’autres molécules apparentées. Elles sont actives contre les bactéries à Gram négatif (mais pas le genre Pseudomonas). Leur taux sérique et leur diffusion tissulaire sont faibles, ce qui limite leur usage aux infections urinaires non compliquées.
- acide nalidixique : FR Negram, Negram Forte; USA NegGam, Wintomylon.
- acide oxolinique : FR †Urostrate; USA †Uroxin.
- acide pipémidique : FR Pipram, Pipram Forte; USA †Dolcol.
- acide piromidique : USA †Panacid.
- cinoxacine : USA †Cinobac.
- fluméquine : FR Apurone; USA †Flubactin.
- rosoxacine : FR †Eracine; USA †Eradacin.
2e génération
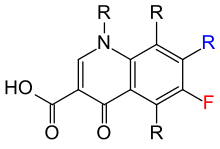
[modifier | modifier le code]La norfloxacine est la première molécule de la seconde génération. Elle est dérivée de l’acide nalidixique par l’introduction d’un atome de fluor en position C6 et d’un groupe pipérazine en position C7. Le fluor est caractéristique des fluoroquinolones, la pipérazine augmente l’activité antibactérienne de la molécule. La ciprofloxacine est dérivée à son tour de la norfloxacine par l’introduction d’un groupe cyclopropyl en position N1 qui améliore sa biodisponibilité.
Le spectre Gram négatif est élargi par rapport à la première génération, il couvre désormais le genre Pseudomonas (en particulier Pseudomonas aeruginosa). Sont également couverts certains germes à Gram positif dont Staphylococcus aureus (mais pas Streptococcus pneumoniae) et certains pathogènes responsables de pneumonies atypiques tels que Chlamydia pneumoniae, Legionella pneumophila et Mycoplasma pneumoniae.
La norfloxacine, la loméfloxacine et l’énoxacine, faute d’une biodisponibilité suffisante, restent cantonnées aux infections des voies urinaires. Au contraire, la ciprofloxacine et l’ofloxacine, qui bénéficient d’un taux sérique plus élevé et d’une meilleure diffusion dans les tissus, sont capables de traiter de nombreux sites d’infection.
- ciprofloxacine : FR Ciflox; USA Cipro, Ciprobay, Ciproxin, Maroc : Ciproxine et générique Catex
- énoxacine : FR Enoxor, Penetrex; USA †Enroxil, †Penetrex.
- fléroxacine : USA †Megalone, †Roquinol.
- loméfloxacine : FR Logiflox, Décalogiflox; USA †Maxaquin.
- norfloxacine : FR Noroxine; USA ‡Janacin, ‡Lexinor, ‡Noroxin, ‡Quinabic.
- ofloxacine : FR Oflocet, Monoflocet; USA †Floxin, †Oxaldin, †Tarivid.
- péfloxacine : FR Péflacine; USA †Peflacine.
L’ofloxacine n’est plus commercialisée sur le marché américain pour cause de concurrence avec la lévofloxacine.
3e génération
[modifier | modifier le code]La troisième génération n’est pas homogène. La lévofloxacine est simplement l’énantiomère lévogyre de l’ofloxacine. La grépafloxacine, la sparfloxacine et la témafloxacine ont en commun l’ajout sur le groupe pipérazine positionné en C7 d’un groupe méthyle stériquement volumineux qui a pour effet de renforcer l’activité anti-streptocoque.
Les agents de la troisième génération ont une activité accrue contre les bactéries Gram positives incluant Streptococcus pneumoniae et Streptococcus pyogenes. Elles sont également actives contre les pathogènes responsables de pneumonies atypiques. Elles conservent une large couverture Gram-négative mais sont moins actives que la ciprofloxacine contre le genre Pseudomonas. Elles sont parfois dites « quinolones respiratoires » par opposition avec les « quinolones urinaires » des générations précédentes.
- balofloxacine : USA †Baloxin; Asie Q-Roxin.
- grépafloxacine : USA †Raxar.
- lévofloxacine : FR Tavanic; USA Levaquin; Asie Cravit.
- pazufloxacine : Asie Pasil, Pazucross.
- sparfloxacine : FR †Zagam; USA †Zagam.
- témafloxacine : USA †Omnifllox.
- tosufloxacine : Asie Ozex, Tosacin.
La grépafloxacine a été retirée du marché à cause de sa cardiotoxicité. La sparfloxacine a été retirée pour cause de cardiotoxicité et de phototoxicité sévère. La témafloxacine a été retirée parce qu’elle provoquait des anémies hémolytiques et des hypoglycémies graves. La tosufloxacine reste commercialisée au Japon malgré un profil toxique controversé incluant nephrotoxicité, hépatotoxicité et risque de thrombocytopénie.
4e génération
[modifier | modifier le code]La quatrième génération conserve l’activité Gram-négative et Gram-positive de la troisième génération tout en couvrant largement les anaérobies, en particulier Bacteroides fragilis. Pour obtenir ce résultat la gatifloxacine et la moxifloxacine substituent un groupe méthoxyle en C8, la clinafloxacine opère une substitution halogène au même endroit, tandis que la trovafloxacine opte pour une substitution en N8. La gatifloxacine et la moxifloxacine sont classées en troisième ou en quatrième génération selon les sources.
- clinafloxacine : USA †105956-99-8.
- garénoxacine : USA †91421-42-0 ; Asie Geninax.
- gémifloxacine : USA ‡Factive.
- moxifloxacine : FR ‡Izilox ; USA ‡Avelox.
- gatifloxacine : USA †Tequin, †Zymar.
- sitafloxacine : USA †127254-12-0 ; Asie Gracevit.
- trovafloxacine : USA †Trovan.
- prulifloxacine : Asie Quisnon.
La gatifloxacine a été retirée du marché pour cause de diabètes sévères, de cardiotoxicité et d’hépatotoxicité. La trovafloxacine a été retirée pour cause d’hépatotoxicité (l’affaire nigériane décrite plus loin a surgi postérieurement à ce retrait). La clinafloxacine malgré une efficacité prometteuse a été stoppée en phase III pour cause de phototoxicité majeure et parce qu’elle provoquait des hypoglycémies sévères. L’usage de la moxifloxacine a été restreint en France et aux États-Unis pour cause de cardiotoxicité et d’hépatotoxicité.
En cours de développement
[modifier | modifier le code]Spectre d'activité
[modifier | modifier le code]Les fluoroquinolones sont des antibiotiques à large spectre. Cependant chacune d’entre elles possède un spectre d’activité particulier. Les spectres de la ciprofloxacine et de la lévofloxacine figurent à titre d’exemples dans les deux tableaux fournis ci-après. Les notations S, SD et R indiquent les germes sensibles, à sensibilité diminuée et résistants vis-à-vis de chacune des molécules. Les abréviations « méti-S » et « méti-R » désignent respectivement les staphylocoques sensibles et résistants à la méticilline.
Les tableaux montrent que la lévofloxacine possède un spectre élargi en gram positif et en anaérobies, tandis que la ciprofloxacine est bien établie en gram négatif. Certaines résistances bactériennes sont plus marquées avec la ciprofloxacine parce que sa diffusion est plus ancienne.
Résistances antibactériennes
[modifier | modifier le code]On observe une augmentation de la résistance à certaines fluoroquinolones largement distribuées comme la ciprofloxacine. Plusieurs hypothèses sont avancées :
- Comme ce fut le cas pour d'autres classes d'antibiotiques par le passé, l'important volume de prescription en particulier en milieu hospitalier favorise les résistances bactériennes.
- L'utilisation massive de fluoroquinolones vétérinaires favoriserait la sélection de souches microbiennes résistantes dans l'environnement.
L'efficacité des antibiotiques de seconde génération dans les infections serait de 60 à 95 %, l'écart venant du type de germe concerné.
Parmi les bactéries résistantes, on peut citer les aérobies à Gram positif : Enterococci, Listeria monocytogenes, Nocardia asteroides, Staphylococcus méti-R.
En 2016, l'OMS a recommandé d'abandonner la prescription de quinolones pour lutter contre la gonorrhée[7]
Indications
[modifier | modifier le code]Compte tenu de la gravité de certains de ces effets indésirables des antibiotiques de la familles des fluoroquinolones, comme une atteinte du système nerveux (neuropathies périphériques), des troubles neuro-psychiatriques, une affection du système musculo-squelettique (douleurs et gonflements au niveau des articulations, inflammation voire rupture des tendons, douleurs et/ou faiblesse au niveau des muscles), et de leur caractère durable dans le temps, invalidant et potentiellement irréversible, l’Agence européenne des médicaments (EMA) a réévalué en 2018 -2019 le rapport bénéfice/risque des fluoroquinolones avec une forte dégradation. Cette réévaluation a conduit notamment à restreindre sévèrement leurs indications thérapeutiques dans toute l'Europe et à actualiser leur profil de sécurité d’emploi[8].
Les indications des fluoroquinolones diffèrent selon la molécule et également selon le pays. Elles sont établies à partir des germes sensibles, des études cliniques et des autres produits antibactériens disponibles. Sont résumées ici, à titre d’exemple, les indications françaises de la ciprofloxacine et de la lévofloxacine pour les patients adultes ne souffrant pas d’autre pathologie que l’infection pour laquelle ils sont traités.
Ciprofloxacine
- Certaines infections sévères à bacilles Gram négatif ou à staphylocoques sensibles
- Urétrite gonococcique chez l'homme
- Infections urinaires basses et hautes compliquées ou non
- Infections intestinales
- Infections ostéoarticulaires
- Sinusites chroniques
- Certains cas d’otites malignes ou chroniques
- Infections de la peau et du tissu mou
- Maladie du charbon (curatif ou prophylactique post-exposition)
- Infections panophtalmiques ou endophtalmiques
Lévofloxacine
- Sinusites aiguës
- Exacerbations aiguës des bronchites chroniques
- Pneumonies communautaires
- Prostatites
- Pyélonéphrites aiguës
- Infections biliaires
- Infections intestinales
- Maladie du charbon (curatif ou prophylactique post-exposition)
Les prescripteurs déterminent leurs choix thérapeutiques en fonction des indications des médicaments et également de leur rapport bénéfice risque. L’efficacité reconnue des fluoroquinolones représente un bénéfice certain, cependant leur profil toxique limite leur usage aux infections sévères ou au cas de souches bactériennes multirésistantes.
En 2007 l’INAMI, organisme chargé de l’assurance maladie belge, a étudié l’adéquation entre les prescriptions de fluoroquinolones par les médecins généralistes et les « règles de bonne pratique médicale » en vigueur dans le pays. Le rapport d’étude[9] montre que 90 % des prescriptions sont inadéquates, principalement parce que les prescripteurs ont abusé des fluoroquinolones en première intention.
Le même rapport met en perspective les consommations de fluoroquinolones dans différents pays européens. La consommation belge est 10 fois celle du Danemark, ce qui recoupe l’ordre de grandeur des prescriptions inadéquates.. La consommation française quant à elle est 9 fois celle du Danemark. À la suite de la publication de l’étude, les autorités belges ont pris des mesures correctives et les prescriptions de fluoroquinolones ont nettement diminué durant l’année 2008.
Limitations et risques des fluoroquinolones
[modifier | modifier le code]Contre-indications
[modifier | modifier le code]Les fluoroquinolones sont contre-indiquées dans les cas suivants :
- intolérance à une quelconque des fluoroquinolones ;
- en particulier, antécédents de tendinopathie, de neuropathie ou d'effets indésirables graves sous fluoroquinolones ;
- en cas de risque de survenue d'anévrisme, de dissection aortique ou de risque de régurgitation/insuffisance des valves cardiaques ;
- enfant ou adolescent en croissance (risque d'atteinte des cartilages) ;
- femme enceinte ou allaitante (risques de malformation) ;
- athlète en période d’entrainement ou de compétition (risque accru de tendinite et de rupture de tendon) ;
- insuffisance cardiaque, hépatique ou rénale grave ;
- épilepsie : risque de déclenchement des convulsions ou d’abaissement du seuil épileptogène ;
- myasthénie : risque d’affaiblissement des muscles respiratoires mettant en jeu le pronostic vital ;
- déficit en glucose-6-phosphate déshydrogénase (G6PD) : risque de réaction hémolytique.
Mises en garde et précautions d'emploi
[modifier | modifier le code]Les précautions et les mises en garde suivantes sont associées aux fluoroquinolones :
- à ne prendre qu'en absence d'autres traitements possibles ;
- consulter son médecin en cas de maux de tête, de douleurs dans les membres ou de craquements des articulations ;
- les réactions allergiques (y compris le choc anaphylactique) ne sont pas dose-dépendantes et peuvent survenir dès la première prise ;
- le patient doit éviter une exposition prolongée au soleil et aux rayonnements ultraviolets UVA et UVB pendant la durée du traitement et les trois jours suivant l'arrêt du traitement ;
- chez l'adulte de moins de 30 ans, la survenue d'arthropathies est à surveiller de près ;
- chez l'adulte de plus de 65 ans, le risque de tendinopathie est très nettement majoré ;
- l’apparition de signes de tendinite nécessite de consulter son médecin sans attendre[10], la mise au repos du tendon concerné, et plus spécifiquement des deux tendons d’Achille (y compris si un seul d’entre eux semble atteint) par une contention appropriée ou des talonnettes ; la survenue d’une tendinopathie impose de ne plus avoir recours ultérieurement à cette classe d’antibiotiques[10] ;
- le rapport bénéfice-risque doit être plus particulièrement évalué chez les insuffisants rénaux, les diabétiques et les personnes prenant une corticothérapie concomitante même inhalée ;
- consulter immédiatement un médecin en cas de survenue de signes évocateurs d’une arythmie cardiaque : palpitations, impression de battements cardiaques rapides ou irréguliers[10] ;
- quelles que soient les précautions prises, et quel que soit le patient, certains effets indésirables apparus pendant le traitement ou après la fin de celui-ci sont susceptibles de s’établir durablement, voire d'évoluer en infirmités permanentes.
Allergies ou hypersensibilités
[modifier | modifier le code]Les fluoroquinolones peuvent donner lieu aux manifestations allergiques suivantes :
- urticaire, photoallergie (photosensibilité)
- maladie sérique ;
- œdème de Quincke (angio-œdème) ;
- réaction anaphylactique, choc anaphylactique ;
- syndrome de Stevens-Johnson ;
- syndrome de Lyell (nécrolyse épidermique toxique) ;
- douleurs chroniques importantes (fibromyalgie).
Le pronostic vital est engagé pour l’œdème de Quincke laryngé, le choc anaphylactique, ainsi que pour les syndromes de Stevens-Johnson et de Lyell, cités ici par ordre de rareté croissante.
Germes opportunistes et infections nosocomiales
[modifier | modifier le code]La destruction de la flore bactérienne par les fluoroquinolones permet à certaines bactéries opportunistes de coloniser les niches vacantes, essentiellement en milieu hospitalier :
- Candida albicans : responsable de candidose (notamment : mycose vaginale) et récemment de septicémie ;
- Staphylococcus aureus (staphylocoque doré) : responsable d’infections cutanées suppuratives ainsi que de septicémie chez les patients immunodéprimés ;
- Clostridium difficile : responsable de diarrhée nosocomiale et de colite pseudomembraneuse pouvant évoluer en mégacôlon toxique (risque fatal).
Une étude réalisée en 2001-2002 sur plusieurs CHU français[11]a montré que lorsque l'on réduisait l'usage de fluoroquinolones de 85 %, le nombre d'infections par des staphylocoques dorés résistant à la méticilline (Staphylococcus aureus méti-R abrégé en SARM) diminuait très significativement. Les résultats extrapolés au niveau national permettent d'affirmer que chaque année, environ 20 000 infections à SARM (sur 140 000 au total) sont directement imputables aux traitements par fluoroquinolones. Ce problème a poussé depuis 2003 les autorités belges à lutter contre la surprescription de fluoroquinolones, accusées également de coûter trop cher au contribuable alors qu'aucune efficacité supérieure aux traitements classiques n'a pu être mise en évidence dans les infections des voies aériennes.
Deux études canadiennes[12],[13], publiées en 2005 et 2006 respectivement, viennent confirmer l’implication majeure des fluoroquinolones dans les infections par le SARM (MRSA) et par le Clostridium difficile (CDAD). L’étude sur le SARM montre que la prise de fluoroquinolones multiplie le risque d’infection par un facteur 2,5 pour la souche bactérienne concernée, alors que les autres antibiotiques n’influent pas sur le risque. L’étude sur l’infection à Clostridium difficile prouve que les fluoroquinolones multiplient le risque d'infection par 4,3 tandis que les autres antibiotiques (macrolides ou bêta-lactamines) le multiplient seulement par un facteur compris entre 1,5 et 1,9.
Interactions médicamenteuses
[modifier | modifier le code]Les fluoroquinolones peuvent interagir avec d’autres médicaments, soit par leur affinité avec le cytochrome P450 1A2, soit par d’autres mécanismes.
Les fluoroquinolones, mais surtout la ciprofloxacine, ont la capacité d’inhiber le cytochrome P450 1A2, ce qui a pour effet de ralentir la métabolisation par le foie de certains médicaments. Le taux sérique de ces médicaments, s’ils sont prescrits à leur posologie standard, tend alors à atteindre des niveaux anormalement élevés, ce qui provoque une amplification non souhaitée de leurs effets positifs ou une exacerbation de leurs effets indésirables.
Les interactions suivantes sont liées au moins en partie au cytochrome P450 1A2 :
- caféine (présente dans le café) : réactions d’intolérance au café ;
- théophylline (présente dans le thé, utilisée comme diurétique, psychoanaleptique et bronchodilatateur) : effets indésirables sur le système nerveux central, comparables à ceux de la théophylline seule surdosée, pouvant aller jusqu’aux convulsions (risque fatal signalé pour la ciprofloxacine) ;
- warfarine (anticoagulant oral) : déséquilibre INR, risque d’hémorragie ;
- ropinirole (agoniste des récepteurs dopaminergiques) ;
- tizanidine (agoniste des récepteurs alpha-2 adrénergiques).
À l’inverse, certains médicaments sont susceptibles de potentialiser les effets indésirables des fluoroquinolones :
- corticoïdes (corticostéroïdes) : risque accru de tendinites et de ruptures tendineuses ;
- AINS (anti-inflammatoires non stéroïdiens incluant a priori les coxibs) : risque accru d’effets sur le système nerveux central et de convulsions.
Enfin, les interactions ci-après peuvent également survenir :
- insuline et hypoglycémiants oraux : risque d’hypoglycémie ou hyperglycémie ;
- ciclosporine (agent immunosuppresseur utilisé dans le domaine de la transplantation d’organes): certaines études[14] envisagent un risque accru de néphrotoxicité et de rejet de greffes.
Effets indésirables
[modifier | modifier le code]Effets indésirables immédiats, prolongés et décalés
[modifier | modifier le code]Cette section traite des effets indésirables des fluoroquinolones, hormis les allergies et les interactions médicamenteuses qui sont décrites séparément. Les effets indésirables se séparent en deux catégories distinctes :
- un petit nombre d’effets à court terme communs à tous les antibiotiques (nausée, diarrhée, vomissement),
- un nombre important d’effets toxiques spécifiques aux fluoroquinolones, souvent des effets de classe, dont l’intensité et la durée sont très variables selon les individus.
Les effets toxiques dans leurs manifestations aiguës et/ou durables peuvent provoquer de graves invalidités provisoires ou définitives.
L’incidence des effets indésirables des fluoroquinolones, comprise entre 5 % et 16 %[15], est comparable à celle des autres antibiotiques de puissance équivalente. Les effets les plus fréquents sont les nausées, la diarrhée et les vomissements. Le plus souvent ils sont bénins et ils disparaissent spontanément à la fin du traitement. L’étude à court terme menée par le CDC (Centers for Disease Control And Prevention)[16]sur 10.000 personnes soumises à un traitement prophylactique contre l’anthrax montre une grande similitude des effets indésirables les plus communs de la ciprofloxacine (une fluoroquinolone) et de la doxycycline (une tétracycline). Cependant une petite partie de ces personnes ont par la suite, et avec la ciprofloxacine seulement, développé des effets indésirables à long terme suffisamment graves pour leur faire entamer des actions judiciaires groupées (voir : les postiers américains). En résumé, les effets indésirables des fluoroquinolones, analogues en pourcentage à ceux des autres antibiotiques, se distinguent cependant par l’existence d’une toxicité spécifique, aux conséquences potentiellement graves, touchant une minorité de patients, mais suffisante pour modifier le ratio bénéfice risque.
La dynamique des effets toxiques des fluoroquinolones[17]est largement méconnue du public et des prescripteurs. Les trois schémas suivants sont possibles, ils sont cités par ordre de fréquence décroissante :
- effet immédiat : apparaît pendant le traitement, disparaît dès la fin de celui-ci,
- effet durable : apparaît pendant le traitement, persiste après la fin de celui-ci parfois pendant une longue période de temps (plusieurs mois ou plusieurs années[18]),
- effet décalé : identique à l’effet durable mais apparaît après la fin du traitement, parfois longtemps après (plusieurs mois ou plusieurs années[19]).
Les effets décalés sont difficiles à diagnostiquer car en général ni le patient ni le médecin ne font le rapprochement entre les symptômes et la prise antérieure d’une fluoroquinolone. La précaution consistant à arrêter le traitement dès l’apparition des effets indésirables ne peut rien contre les effets décalés.
Liste des effets indésirables
[modifier | modifier le code]Les effets indésirables listés ci-dessous, sauf ceux notés « non homologués », sont documentés dans les notices françaises et américaines des fluoroquinolones :
| Manifestations générales | Fatigue physique et mentale, sensation de mal-être, transpiration excessive, douleurs, courbatures. |
| Manifestations musculosquelettiques | Arthralgie (douleurs articulaires), craquements articulaires, raidissement ou gonflement des articulations, raidissement de la nuque, douleurs aux extrémités (mains et pieds), attaque de goutte, arthrite, arthrose, rhizarthrose (aux mains), détérioration des cartilages et des ligaments, tendinite, tendinopathies pouvant aller jusqu'à la rupture tendineuse notamment au tendon d'Achille mais aussi aux épaules, genoux, mains et également à la mâchoire, myalgie (douleurs musculaires), crampes musculaires, fonte musculaire, faiblesse musculaire, myasthénie (fatigabilité excessive des muscles à l’effort), augmentation de la créatine phosphokinase (CPK) en relation avec les atteintes musculaires, rupture musculaire, rhabdomyolyse (destruction des cellules musculaires). La rupture tendineuse est rare et semble favoriser par la prise concomitante de corticoïdes[20]. |
| Manifestations neurologiques (système nerveux central) | Céphalées (maux de tête), étourdissements, sensations ébrieuses, sensation de tête vide, désorientation, vertiges, troubles du sommeil (y compris : insomnie chronique), rêves anormaux, ataxie (en particulier troubles de la marche et de l’équilibre), sensation de décharges électriques, tremblements, convulsions (de type épileptique), grand mal, hypertension intracrânienne. |
| Manifestations cognitives (système nerveux central) | Troubles de l’attention, difficultés d’élocution, amnésie parfois associée à une sensation de lavage de cerveau. |
| Manifestations psychiatriques (système nerveux central) | Anxiété, agitation, hyperactivité psychomotrice, instabilité émotionnelle, dépression, idées et actes suicidaires, dépersonnalisation, délire, confusion mentale, hallucinations (pouvant concerner les cinq sens), réaction psychotique. |
| Manifestations neurologiques (système nerveux périphérique) | Paresthésie (fourmillements, picotements), hypoesthésie (engourdissements), dysesthésie (douleurs, brûlures), sensation de faiblesse, fasciculations (contractions involontaires et isolées). |
| Manifestations oculaires | Douleurs oculaires, yeux secs, vision floue, diminution de l’acuité visuelle, chromatopsie (modification de la perception des couleurs), diplopie (double vision), surbrillance des lumières, photophobie, corps flottants, éclairs, perte transitoire de la vision, décollement de rétine[21]. |
| Manifestations auditives | Acouphènes, hypoacousie (diminution de l’acuité auditive), perte transitoire de l’audition. |
| Autres manifestations sensorielles | Modification du goût (dysgueusie), perte du gout, modification de l’odorat, perte de l’odorat. |
| Manifestations cutanées | Photosensibilisation dans le domaine des UVA et des UVB, exacerbation des coups de soleil, prurit (démangeaison), éruption cutanée, perte d’élasticité de la peau, hyperpigmentation (la peau devient plus sombre), veines plus apparentes, cicatrisation de mauvaise qualité, alopécie (chute des cheveux), érythème (rougeur de la peau), dermatite exfoliative, œdème, érythème noueux, érythème polymorphe. |
| Manifestations cardiovasculaires | Palpitations, tachycardie, hypotension, hypertension, angine de poitrine (angor pectoris), vasculite (inflammation des parois des vaisseaux sanguins), phlébite ou thrombose veineuse profonde, thrombose cérébrale, arythmie (trouble du rythme cardiaque), allongement de l’intervalle QT, torsades de pointes, fibrillation auriculaire, fibrillation ventriculaire, extrasystoles, syncope, arrêt cardiaque ou infarctus du myocarde. Il semble exister une augmentation du risque de survenue d'un anévrisme aortique ou d'une dissection[22] mais cela reste discuté[23]. |
| Manifestations respiratoires | Dyspnée (difficulté à respirer, essoufflement), hoquet (caractérisé par des contractions involontaires du diaphragme), bronchospasme, épistaxis (saignement de nez), œdème pulmonaire, hémoptysie (rejet de sang au cours d’un effort de toux), embolie pulmonaire. |
| Manifestations digestives | Nausées, vomissements, constipation, diarrhée, gastralgie (douleurs abdominales), dyspepsie (reflux d’acide dans l’œsophage), perte de l’appétit, bouche sèche, muqueuse orale douloureuse, dysphagie (gêne pour avaler), saignements gastro-intestinaux, perforation intestinale, pancréatite, pancréatite aiguë. |
| Manifestations hépatiques | Augmentation des transaminases (ALAT, ASAT), augmentation de la bilirubine, augmentation de la gamma glutamyl transférase, augmentation des phosphatases alcalines, altération de la fonction hépatique (dont augmentation des LDH), inhibition du cytochrome P450 1A2 (voir: interactions médicamenteuses), ictère (jaunisse), ictère cholestatique, hépatite, nécrose hépatique, hépatite fulminante, insuffisance hépatique, insuffisance hépatique aiguë. |
| Manifestations rénales | Altération de la fonction rénale (dont augmentation de la créatinine et de l’urée), cristallurie, néphrite, néphrite interstitielle, insuffisance rénale, insuffisance rénale aiguë. |
| Manifestations urogénitales | Impuissance sexuelle, hyperuricémie (taux excessif d’acide urique dans le sérum sanguin), hémorragie urétrale, hématurie microscopique ou macroscopique (présence de sang dans les urines), polyurie (urines abondantes), rétention urinaire. |
| Manifestations hématologiques | Hyperplaquettose ou thrombocytose (excès de plaquettes), thrombocytémie (production excessive de plaquettes par la moelle osseuse), thrombopénie ou thrombocytopénie (manque de plaquettes), purpura ou pétéchie (mini-hémorragies sous la peau dues au déficit en plaquettes), leucopénie (manque de globules blancs), agranulocytose (manque de granulocytes), neutropénie (manque de neutrophiles), éosinophilie (excès d’éosinophiles), anémie hémolytique (destruction excessive de globules rouges), aplasie médullaire (production insuffisante de globules blancs, de globules rouges et de plaquettes par la moelle osseuse), pancytopénie (nombre insuffisant de globules et de plaquettes). |
| Manifestations lymphatiques | Lymphadénopathie (atteinte des ganglions lymphatiques). |
| Troubles de la glycémie | Hyperglycémie, hypoglycémie ou les deux alternativement, en particulier chez les patients diabétiques traités par insuline ou hypoglycémiants oraux[24] (voir aussi : Interaction médicamenteuse). |
| Manifestations non homologuées | Déchirure musculaire, infirmité motrice provisoire ou définitive pouvant nécessiter l’usage d’attelles, de béquilles ou d’un fauteuil roulant, perte de poids parfois suivie d’un gain de poids excessif, diminution de la taille (hauteur) de la personne, impression de vieillissement prématuré, veines apparentes, ongles striés verticalement, augmentation des fautes de frappe au clavier (par exemple : inversion des lettres), perte du schéma corporel, changement de la personnalité, yeux secs, difficultés d’accommodation à la distance, à la lumière ou aux contrastes lumineux, problèmes dentaires en relation avec la sécheresse buccale, intolérance à certains médicaments même s’ils ont été utilisés antérieurement avec succès par le patient (par exemple: anesthésiques dentaires locaux à base d’articaïne), augmentation de la pression oculaire, glaucome. |
Les effets indésirables sont classés ici en fonction du lieu où ils se manifestent et non pas de l’endroit où se situe leur cause. Les nausées peuvent provenir d’une irritation du système digestif mais également d’une réaction du système nerveux central. Dans le second cas même les patients recevant un traitement par voie intraveineuse sont concernés. La bouche sèche et les yeux secs dépendent d’un neuromédiateur (l’acétylcholine). Le système nerveux est également à l’origine de certaines manifestations sensorielles, musculaires ou cardiaques. Par ailleurs, certaines manifestations oculaires sont liées aux muscles et aux tendons qui actionnent les yeux.
Issue fatale possible pour: nécrose ou insuffisance hépatique aigüe, insuffisance rénale aigüe, rhabdomyolyse, acte suicidaire, arrêt cardiaque.
Les effets cités concernent principalement les fluoroquinolones systémiques. Les fluoroquinolones ophtalmiques peuvent aussi produire certains de ces effets mais le risque est minoré. Cependant il existe des effets spécifiques aux fluoroquinolones ophtalmiques, tels que : chémosis, érosion de la cornée, ulcère de la cornée, hyperémie oculaire (œil rouge), œdème des paupières, érythème des paupières.
Chez des modèles animaux
[modifier | modifier le code]Cette section présente des risques additionnels tirés du modèle animal et potentiellement applicables aux humains.
Souris sans poils
[modifier | modifier le code]D’après une étude finlandaise, certaines fluoroquinolones ont des effets carcinogènes sur les souris de type hairless ou souris sans poils[25]. La présence d’effets carcinogènes ou leur absence peut d’ailleurs devenir un argument de publicité comparative entre les molécules[26]: « La moxifloxacine n'a pas montré de potentiel carcinogène sur un essai d'initiation/promotion effectué chez le rat. De nombreuses quinolones sont photoréactives et peuvent induire des effets phototoxiques, photomutagènes et photocarcinogènes. En revanche, la moxifloxacine est dénuée de propriétés phototoxiques et photogénotoxiques sur des études in vitro et in vivo alors que, dans ces mêmes conditions, d'autres quinolones ont induit des effets. ». Toutefois en l’absence de données cliniques convaincantes le cancer de la peau n’est pas classé parmi les effets indésirables des fluoroquinolones chez les humains.
Mécanismes toxiques possibles
[modifier | modifier le code]Ces substances génèrent de nombreux effets secondaires, dont parfois de lourdes invalidités temporaires ou définitives. Des effets tendineux, allant jusqu'à la rupture de tendon(s) en divers endroits du corps ont été signalés dès 1983. Les années 1990 seront marquées par une crise de confiance exemplaire[27] de la part des prescripteurs, en particulier en France. Les essais sur les animaux montrent de plus un potentiel cancérigène sur tous les mammifères et tératogène sur le rat[28], d'atteintes cartilagineuses graves sur la plupart des mammifères immatures. En 1997, les chercheurs[29] décrivent les effets tendineux des fluoroquinolones. La péfloxacine, accusée depuis des années de provoquer de nombreuses tendinopathies, deviendra marginale.
La concentration de fluoroquinolone dans le cerveau est importante et est à l'origine d'effets neuropsychiatriques comparables à ceux des benzodiazépines. Les fluoroquinolones représentent 4 % de tous les effets psychiatriques notifiés à l'ANSM ; cela les situe en huitième position, n'étant précédées que par des neuroleptiques.
Les mécanismes toxiques ne sont pas clairement établis :
- captation des cations, en particulier le magnésium, altérant le métabolisme cellulaire et induisant une production de toxines létales pour les cellules. Il a été démontré chez le rat que la carence en magnésium entraîne des lésions tendineuses similaires à celles observées avec les fluoroquinolones.
- effet toxique direct : l'ADN du noyau serait directement endommagé, comme dans le cas des bactéries. Cette hypothèse expliquerait la rapidité de survenue des effets toxiques observés chez certains sujets. Le potentiel d'action de la ciprofloxacine sur l'ADN des cellules humaines, récemment mis en évidence, appuie cette hypothèse.
- altération du métabolisme mitochondrial : émise en 1997, cette hypothèse est remise en cause par des études plus récentes. Si l'ADN mitochondrial est effectivement une cible des fluoroquinolones, les concentrations nécessaires pour obtenir une toxicité importante dépasseraient largement les concentrations thérapeutiques.
- effets biochimiques : la ciprofloxacine stimule la métalloprotéinase matricielle 2[30] et 3[31], favorisant la dégradation du collagène, ce qui pourrait favoriser la fragilité des tendons et le risque vasculaire (anévrisme).
La rémanence des fluoroquinolones dans les tissus expliquerait le passage à la chronicité de certaines séquelles[32]: un seul cachet peut provoquer des remaniements tendineux pendant 6 mois chez le rat. Il faudrait selon certains fabricants environ 6 mois pour que la concentration en fluoroquinolones descende sous le seuil d'action.
Litiges et procès
[modifier | modifier le code]Pfizer et l'affaire du Trovan
[modifier | modifier le code]Le , le Washington Post fait état d'un rapport des autorités nigérianes mettant en cause le leader pharmaceutique mondial Pfizer qui aurait pratiqué un essai illégal de la trovafloxacine (Trovan) en 1996 sur près de 200 enfants et nourrissons à l'occasion d'une épidémie de méningite, provoquant des décès et de lourds handicaps liés en particulier à de l'arthrite[33]. Pfizer affirmera avoir obtenu l'accord oral des familles des enfants.Cette affaire, ébruitée dès 2000, aurait inspiré le roman La constance du jardinier à John le Carré.
Pfizer, engagé dans une longue bataille judiciaire sur cette affaire, a finalement le accepté de verser aux autorités nigérianes la somme de 75 millions de dollars en échange de l’arrêt des poursuites[34].Le médicament concerné, une fluoroquinolone possédant 3 atomes de fluor, a été mis sur le marché en 1998 en Europe avant d'être interdit en raison de graves effets hépatiques[35]. Il n’a jamais été autorisé en France.
Le FDA et l’affaire des « encadrés noirs »
[modifier | modifier le code]La littérature médicale rapporte pour la première fois en 1972 des effets indésirables musculo-squelettiques attribués à l’acide nalidixique, ancêtre des quinolones[36]. Onze ans plus tard, des cas de maladies rhumatismales sont signalés à la suite de l’usage de la norfloxacine, une fluoroquinolone[37]. En réponse à une lettre publiée à ce sujet en 1995 dans le New England Journal of Medicine, des officiels du FDA américain (Food and Drug Administration) se déclarent prêts à « mettre à jour la notice de toutes les fluoroquinolones commercialisées, afin d’y inclure un avertissement concernant le risque de rupture tendineuse »[38].
En , constatant que FDA n’a pas tenu son engagement, Public Citizen (une association de défense des consommateurs créée par Ralph Nader) dépose une pétition pour obliger le FDA à agir[39]. Deux mois plus tard le FDA, faisant droit à cette pétition, publie une alerte dans son bulletin médical et ordonne que les notices des fluoroquinolones soient modifiées, afin d’inclure une information sur le risque tendineux.
Neuf ans plus tard, en 2005, la Procureure Générale de l’Illinois dépose une seconde pétition auprès du FDA. Elle va plus loin cette fois-ci et demande une mise en garde renforcée concernant le risque de rupture tendineuse, qui se traduise par un avertissement encadré de noir sur la notice des fluoroquinolones (Black Box Warning) ainsi que par l’envoi de lettres d’information aux prescripteurs. Le FDA répond qu’il n’a pas encore pris de décision en ce sens. L’encadré noir représente le plus haut niveau de mise en garde dont le FDA dispose.
En 2006, Public Citizen, soutenu par la Procureure Générale de l’Illinois, vient appuyer la demande d’encadré noir par une troisième pétition[40].
Le FDA n’ayant répondu ni à la seconde ni à la troisième pétition, alors que la loi l’y obligeait, Public Citizen engage un procès en pour le forcer à réagir[41]. Le , la justice donne raison à Public Citizen. Le FDA demande alors aux fabricants de fluoroquinolones systémiques d’apposer un encadré noir sur leurs notices et également d’élaborer un guide thérapeutique destiné à sensibiliser les patients au risque de rupture des tendons[42].
La France n’a pas pour l’instant mis en place un tel niveau d'alerte, les tendinites sont simplement mentionnées dans les sections « mises en garde » des notices. Cela crée une importante incohérence entre les avertissements données aux consommateurs européens et ceux dont bénéficient les consommateurs nord-américains. Les données de pharmacovigilance disponibles indiquent pourtant un risque accru de tendinopathies pour le consommateur français, qui pourrait être lié à l'utilisation plus grande en France de produits glucocorticoïdes amplifiant les effets indésirables tendineux des fluoroquinolones. Cette différence sur les notices des fluoroquinolones a connu un précédent notable et toujours d'actualité: bien que les risques d'atteintes séquellaires du système nerveux périphérique soient obligatoires depuis 2004 dans les notices américaines, ils sont absents des notices françaises.
L’affaire des postiers américains
[modifier | modifier le code]Un recours collectif a été déposé contre Bayer AG par des employés du bureau de poste de Brentwood (à Washington), d’autres bureaux de poste, du Capitole et de la société American Media (en Floride). Ces employés, qui ont pris de la ciprofloxacine à titre prophylactique lors des attaques à l’anthrax en 2001, se plaignent d’effets secondaires durablement invalidants tels que des ruptures de tendons, des lésions articulaires, des lésions du système nerveux central et périphérique ainsi que des problèmes cardiaques et gastro-intestinaux[43].
Les plaignants, défendus par le cabinet d’avocats Sheller, Ludwig & Badey, déclarent qu’ils n’ont pas été prévenus des effets indésirables potentiellement graves auxquels ils ont été exposés. Ils n’ont pas non plus été informés de l’existence de médicaments de substitution aussi efficaces et plus sûrs que la ciprofloxacine. Ils réclament par conséquent des dommages et intérêts en compensation du préjudice qu’ils ont subi. Toutefois leur recours échoue en 2004 et ils abandonnent les poursuites.
Un nouveau recours collectif concernant la ciprofloxacine a été déposé en 2008 dans l’État du New Jersey par un second groupe de postiers. Son résultat n’est pas encore connu. La doxycycline (qui n’est pas une fluoroquinolone) a été utilisée en parallèle de la ciprofloxacine lors de la crise de l’anthrax. Elle n’a fait l’objet d’aucun recours collectif.
Perspectives d’avenir
[modifier | modifier le code]Les des-F(6)-quinolones
[modifier | modifier le code]Les fluoroquinolones anti-cancéreuses
[modifier | modifier le code]Un certain nombre d'études des années 2000 ont montré que les fluoroquinolones n'agissaient pas seulement sur les cellules procaryotes (comme les bactéries) mais également sur les cellules eucaryotes (comme celles des humains). L'administration concomitante de ciprofloxacine et d'étoposide a montré une compétition entre ces deux molécules qui appartiennent à la famille des inhibiteurs de topoisomérase II. Un effet anti-tumoral notable a été démontré sur des cellules humaines in vitro pour la ciprofloxacine, qui induit comme l'étoposide l'apoptose cellulaire des cellules cancéreuses en scindant l'ADN. L'activité anti-cancéreuse de la ciprofloxacine a été établie à un douzième de celle de l'étoposide, mais la toxicité pour l'ADN des cellules humaines serait en revanche nettement supérieure pour la ciprofloxacine. Réciproquement, des études ont montré dès 1985 que l'étoposide possédait une activité anti-bactérienne.
De nouvelles fluoroquinolones sont actuellement mises au point et constituent une piste de recherche contre le cancer. L'une d'entre elles a montré en laboratoire une activité anti-cancéreuse 50 fois supérieure à celle de l'étoposide.
Références
[modifier | modifier le code]- (en)"The Quinolones", Vincent T. Andriole; Editeur Butterworth-Heinemann, 3e édition (2006).
- (en)"Quinolone Antimicrobial Agents", David C. Hooper, Ethan Rubinstein; Editeur ASM Press, 3e edition, (2003).
- « Quinolones », sur pharmacomedicale.org (consulté le )
- Agence nationale de sécurité du médicament et des produits de santé - Les antibiotiques : Fluoroquinolones
- (en) New Antibiotics in Pulmonar and Critical Care Medicine PG. Ambrose, RC. Owens – Seminary in Respiratory and Critical Care Medicine – 2000;21(1) – Janvier 2000
- (en) WHO Model List of Essential Medicines 16th list – Mars 2009
- Kupferschmidt K (2016), The world may soon run out of drugs to treat gonorrhea; 2016-08-30, consulté 2016-09-11
- « Quinolone- and fluoroquinolone-containing medicinal products - referral | European Medicines Agency », sur www.ema.europa.eu (consulté le )
- (fr) Rapport INAMI sur les Quinolones E-project 05/010 – Août 2007
- ANSM - Profil de sécurité des quinolones administrées par voie générale - Point d'Information
- (fr) Fluoroquinolones : une aubaine pour le SARM ? P. Charbonneau – (lire page 23)
- (en) Emergence of fluoroquinolones as the predominant risk factor for Clostridium difficile-associated diarrhea : a cohort study during an epidemic in Quebec J. Pepin, N. Saheb, MA.. Coloumbe, etc – Clinical Infectious Diseases – 1;41(9):1254-60 – Novembre 2005
- (en) Fluoroquinolones and Risk for Methicillin-resistant Staphylococcus aureus L. LeBlanc, J. Pépin, etc – Emerging Infectious Diseases Journal – Volume 12 – Number 9 – Septembre 2006
- (en) Moderate Interaction - Cyclosporine vs Selected Quinolones Medscape: revue de 9 références
- (en) Specific Toxicologic Aspects of Quinolones W. Christ, T.Lehnhert, B. Ulbrich – Review of Infectious diseases – Janvier Février 1988
- (en) Antimicrobial Postexposure Prophylaxis for Anthrax : Adverse Events and Adherence CW. Shepard, M. Soriano-Gabarro, ER. Zell, J.Hayslett, etc – CDC studies – Vol 8, N°10 – Octobre 2002
- (en) The Flox Report – Quinolone Antibiotics Toxicity – March 2007
- (en) Peripheral Neuropathy Associated with Fluoroquinolones JS Cohen – The Annals of Pharmacotherapy – Volume 35 – Décembre 2001 – (lire page 4)
- (en) Antimicrobial safety: focus on fluoroquinolones RC Owens, PG Ambrose – Infectious Diseases Society of America – 41 Suppl2: S144-57 – Juillet 2005 – (lire page 8)
- Stephenson AL, Wu W, Cortes D, Rochon PA, Tendon injury and fluoroquinolone use: a systematic review, Drug Saf, 2013;36:709-21
- (en) U.S. http://jama.ama-assn.org/content/307/13/1414.abstract
- Pasternak B, Inghammar M, Svanström H, Fluoroquinolone use and risk of aortic aneurysm and dissection: nationwide cohort study, BMJ, 2018;360:k678
- Huh K, Kang M, Jung J, Lack of association between fluoroquinolone use and aortic aneurysm or dissection, Eur Heart J, 2023;44:4476–84
- (en) U.S. Food and Drug Administration ""Summary of product characteristics Proquin, Maxaquin, Noroxin, Floxin" 11 mai 2007.
- (en) Quinolone antibacterials: a new class of photochemical carcinogens Mäkinen M, Forbes PD, Stenbäck F – Février 1997 – J Photochem Photobiol B – Feb;37(3):182-7
- (fr) Vidal: Notice Izilox
- (fr)"Tendinopathies induites par les médicaments" Gilles Hayem, Rev Rhum [Ed Fr] 2002 ; 69 : 406-10.
- (fr)"Quinolones et grossesse : des données animales inquiétantes et peu de données cliniques."; article de Michel Damase, revue Prescrire, août 1998; Volume 18, 186; ISSN 0247-7750; pages 530-534
- (fr)"Tendons et fluoroquinolones: des problèmes non résolus." Kahn MF, Hayem G., Rev. Rhum., 1997, 64(7-9), 511-513.
- Tsai WC, Hsu CC, Chen CP et al. Ciprofloxacin up-regulates tendon cells to express matrix metalloproteinase-2 with degradation of type I collagen, J Orthop Res, 2011;29:67-73
- Corps AN, Harrall RL, Curry VA, Fenwick SA, Hazleman BL, Riley GP, Ciprofloxacin enhances the stimulation of matrix metalloproteinase 3 expression by interleukin-1beta in human tendon-derived cells. A potential mechanism of fluoroquinolone-induced tendinopathy, Arthritis Rheum, 2002;46:3034-40
- (fr) "Tendinopathies induites par les médicaments" Gilles Hayem, Rev Rhum [Ed Fr] 2002 ; 69 : 406-10
- (en) Panel Faults Pfizer in '96 Clinical Trial In Nigeria The Washington Post - Joe Stephens - 7 mai 2006
- (en) Pfizer to Pay $75 Million to Settle Trovan Testing Suit The Washington Post - Joe Stephens - 31 juillet 2009
- (en) Acute liver failure due to trovafloxacin: CT findings DOI 10.1007/PL00011876
- (en) Nalidixic acid arthralgia Can Med Assoc J - Bailey RR, Natale R, Linton AL - Octobre 1972 - (ISSN 0008-4409) -
- (en) Norfloxacin-induced rheumatic disease NZ Med J - Bailey RR, Kirk JA, Peddie BA - Juillet 1983 - (ISSN 0028-8446) - (réservé aux abonnés)
- (en) More on fluoroquinolone antibiotics and tendon rupture N Engl J Med - Szarfman A, Chen M, Blum MD - Janvier 1995 - DOI 10.1056/NEJM199501193320319 - (ISSN 0028-4793) -
- (en) Petition to Require a Warning on All Fluoroquinolone Antibiotics Public Citizen - 1er Août 1996
- (en) Public Citizen Petitions the FDA to Include a Black Box Warning on Fluoroquinolone Antibiotics Public Citizen - 29 août 2006
- (en) Public Citizen v. Food and Drug Administration (FDA) (Fluoroquinolone) Public Citizen - 3 janvier 2008
- (en) Post-marketing Safety Information for Patients and Providers FDA - 7 juillet 2008
- (en) « Anthrax Scare Leaves Trail of Cipro Victims - Class Actions filed in Two States » Sheller Ludwig & Badey - 17 octobre 2003


 French
French Deutsch
Deutsch