Sirolimus — Wikipédia
| Sirolimus | ||
 | ||
 | ||
| Identification | ||
|---|---|---|
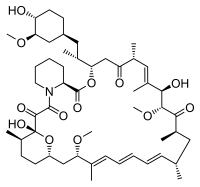
| Nom UICPA | (3S,6R,7E,9R,10R,12R,14S,15E,17E,19E,21S,23S, 26R,27R,34aS)-9,10,12,13,14,21,22,23,24,25,26, 27,32,33,34,34a-hexadécahydro-9,27-dihydroxy-3- [(1R)-2-[(1S,3R,4R)-4-hydroxy-3-méthoxycyclohexyl]- 1-méthyléthyl]-10,21-diméthoxy-6,8,12,14,20,26- hexaméthyl-23,27-époxy-3H-pyrido[2,1-c][1,4]- oxaazacyclohentriacontine-1,5,11,28,29 (4H,6H,31H)-pentone | |
| Synonymes | rapamycine | |
| No CAS | ||
| No ECHA | 100.107.147 | |
| Code ATC | L04 | |
| PubChem | 6436030 | |
| SMILES | ||
| InChI | ||
| Propriétés chimiques | ||
| Formule | C51H79NO13 [Isomères] | |
| Masse molaire[1] | 914,171 9 ± 0,050 4 g/mol C 67,01 %, H 8,71 %, N 1,53 %, O 22,75 %, | |
| Données pharmacocinétiques | ||
| Biodisponibilité | 20 % | |
| Liaison protéique | 92 % | |
| Métabolisme | Hépatique (CYP3A4) Glycoprotéine P | |
| Demi-vie d’élim. | 57 - 63 h | |
| Excrétion | Fécale essentiellement | |
| Considérations thérapeutiques | ||
| Classe thérapeutique | Immunosuppresseur | |
| Voie d’administration | Orale | |
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier | ||
Le sirolimus, appelé également rapamycine, est un médicament qui, comme la ciclosporine et le tacrolimus, est classé parmi les immunosuppresseurs. Pour des raisons mal comprises, il semble pouvoir contribuer à allonger la durée de vie de souris et d'autres mammifères[2].
Historique
[modifier | modifier le code]Il a été isolé en 1975 par une équipe de chercheurs canadiens à partir d'une bactérie filamenteuse, Streptomyces hygroscopicus, provenant du sol de l'île de Pâques, laquelle est connue sous le nom de Rapa Nui en langue rapanui. La rapamycine a été considérée dans un premier temps comme un antibiotique de type macrolide[3]. Ses effets immunodépresseurs ont été décrits dès 1977[4].
Mécanisme d'action
[modifier | modifier le code]Bien qu'il ait un nom similaire au tacrolimus, il n'agit pas de la même façon. Son mécanisme d'action est lié à l'inhibition de la protéine mTOR (mammalian Target Of Rapamycin ou encore : « cible de la rapamycine chez les mammifères »).
In vitro, il bloque la prolifération calcium-dépendante sans altérer la transcription des cytokines (comme le font la ciclosporine et le tacrolimus). Il inhibe donc la synthèse d'anticorps promue par les interleukines dans les lymphocytes B[5].
La molécule, introduite dans la nourriture, semble allonger significativement la durée de vie des souris. Selon une étude de David Harrison (Jackson Laboratory, Maine, États-Unis) et Randy Strong (université du Texas) publiée dans le journal Nature, la rapamycine serait ainsi le premier médicament capable d'allonger la durée de vie de mammifères[2].
| sirolimus | |
| Informations générales | |
|---|---|
| Princeps |
|
| Classe | agents immunosuppresseurs, immunosuppresseur sélectif, inhibiteur du mTOR (mammalian target of rapamycine) ATC code L04AA10 |
| Forme | comprimés enrobés, à 0,5, 1 et 2 mg, solution buvable à 1 mg·ml-1 |
| Administration | per os |
| Laboratoire | Pfizer |
| Identification | |
| No CAS | |
| No ECHA | 100.107.147 |
| Code ATC | L04AA10 et S01XA23 |
| DrugBank | DB00877 |
| modifier | |
Pharmacocinétique
[modifier | modifier le code]Similaire au tacrolimus, l'absorption orale est avec faible biodisponibilité et grande variabilité inter-individuelle. Le sirolimus se rencontre dans le sang majoritairement lié aux érythrocytes. Sa grande liposolubilité lui confère des propriétés de fixation aux tissus ainsi que la possibilité de passer la barrière hémato-encéphalique ainsi que la barrière placentaire. Il peut être excrété dans le lait maternel.
Effets indésirables
[modifier | modifier le code]Les effets indésirables du sirolimus sont variés[6] :
- hypertriglycéridémie et hypercholestérolémie ;
- thrombopénie (diminution du nombre de plaquettes sanguines) et leucopénie (diminution du nombre de globules blancs) ;
- infertilité masculine ;
- pneumopathies interstitielles de mécanisme immuno-allergique ;
- …
Près du tiers des patients arrêtent le traitement, donné comme immunodépresseur, en raison de ces effets[7].
Interactions médicamenteuses
[modifier | modifier le code]Comme la ciclosporine et le tacrolimus, il a une grande interaction avec toxicité non négligeable, avec les inducteurs/inhibiteurs du CYP3A4
Utilisation
[modifier | modifier le code]Il est utilisé essentiellement comme immunodépresseur lors d'une transplantation rénale.
Il pourrait avoir des effets intéressants dans la réduction de la taille des kystes rénaux lors d'une polykystose rénale type dominant et lors d'une sclérose tubéreuse de Bourneville[8].
Outre son action en tant qu'immunosuppresseur, le sirolimus est utilisé dans certains stents actifs, dispositif métallique implanté dans des artères lors d'une angioplastie pour empêcher le resserrement (resténose) de celles-ci : il en imbibe les mailles métalliques du « ressort » diminuant ainsi fortement la prolifération cellulaire qui est responsable de cette resténose.
Un dérivé du sirolimus, l'évérolimus, a été étudié dans la prévention de la maladie coronarienne du greffon cardiaque qui touche 50 % des greffés cardiaques dans les cinq ans qui suivent la transplantation et première cause de décès après la première année suivant la greffe : le dérivé du sirolimus a montré sa supériorité par rapport à l'azathioprine notamment[9].
Il est également utilisé dans le traitement de certains hémangiomes
Recherche
[modifier | modifier le code]
Trois études américaines citées par la revue Nature[2] ont montré une augmentation de l'espérance de vie chez les souris, en particulier celles âgées, mais au détriment du système immunitaire. Elle est en cours d'études chez le chien[10].
Cette molécule est également envisagée dans le traitement de certains cas de troubles du spectre autistique[11],[12].
Dans une étude de 2018, la rapamycine a donné des résultats intéressants sur la prévention de la presbyacousie (perte auditive liée à l'âge) en diminuant la perte des cellules ciliées externes chez les souris[13].
Notes et références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Harrison DE, Strong R, Sharp ZD. et al. « Rapamycin fed late in life extends lifespan in genetically heterogeneous mice » [letter] Nature 2009;(460):392-5. DOI 10.1038/nature08221.
- Sehgal SN, Baker H, Vezina C, Rapamycin (AY-22, 989) a new antifungal antibiotic. II. Fermentation, isolation and characterization. J Antibiot (Tokyo), 1975;28:727–735.
- Martel RR, Klicius J, Galet S, Inhibition of the immune response by rapamycin, a new antifungal antibiotic, Can J Physiol, 1977;55:48–51.
- (en) Morelon E, Mamzer-Bruneel MF, Peraldi MN, Kreis H. « Sirolimus: a new promising immunosuppressive drug. Towards a rationale for its use in renal transplantation » Nephrol Dial Transplant. 2001;16:18-20.
- (en) Buhaescu I, Izzedine H, Covic A, « Sirolimus challenging current perspectives », Ther Drug Monit, no 28, , p. 577-84. (PMID 17038868, résumé)
- (en) Cravedi P, Ruggenenti P, Remuzzi G, « Sirolimus to replace calcineurin inhibitors? Too early yet », Lancet, no 373, , p. 1235-6. (PMID 19362662, lire en ligne)
- (en) Bissler JJ, McCormack FX, Young LR, Elwing JM, Chuck G, Leonard JM, Schmithorst VJ, Laor T, Brody AS, Bean J, Salisbury S, Franz DN, « Sirolimus for angiomyolipoma in tuberous sclerosis complex or lymphangioleiomyomatosis », N Engl J Med, vol. 358, no 2, , p. 140-51. (PMID 18184959, PMCID PMC3398441, DOI 10.1056/NEJMoa063564, lire en ligne [html]).
- (en) Howard J Eisen, Tuzcu EM, Dorent R, Bernhardt P et al.; RAD B253 Study Group, « Everolimus for the prevention of allograft rejection and vasculopathy in cardiac-transplant recipients », N Engl J Med, vol. 349, no 9, , p. 847-58. (PMID 12944570, DOI 10.1056/NEJMoa022171, lire en ligne [html]).
- (en-US) « Dr. Matt Kaeberlein on WormBot and the Dog Aging Project », sur www.lifespan.io (consulté le )
- (en) Ehninger D, Silva AJ, « Rapamycin for treating Tuberous sclerosis and Autism spectrum disorders », Trends Mol Med, vol. 17, no 2, , p. 78-87. (PMID 21115397, PMCID PMC3075964, DOI 10.1016/j.molmed.2010.10.002, lire en ligne [html]).
- Jalinière H, « Autisme : un excès de synapses qui pourrait être réversible » Sciences et Avenir, 25 août 2014.
- (en) « Rapamycin but not acarbose decreases age-related loss of outer hair cells in the mouse Cochlea », Hearing Research, vol. 370, , p. 11–15 (ISSN 0378-5955, DOI 10.1016/j.heares.2018.09.003, lire en ligne, consulté le )
Voir aussi
[modifier | modifier le code]Liens externes
[modifier | modifier le code]- Page spécifique dans la base de données sur les produits pharmaceutiques (Canada)
- Compendium suisse des médicaments : spécialités contenant Sirolimus
- Page spécifique sur le Répertoire Commenté des Médicaments, par le Centre belge d'information pharmacothérapeutique
- Page spécifique sur le Vidal.fr


 French
French Deutsch
Deutsch