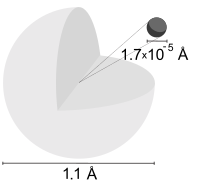
Atomul de hidrogen în tabelul nuclidelor Reprezentarea atomului de hidrogen , unde raza confirmă cea indicată de modelul atomic Bohr Atomul de hidrogen este atomul hidrogenului , care este cel mai simplu element chimic . Este alcătuit dintr-un nucleu pozitiv compus dintr-un singur proton și un electron ce se mișcă în jurul nucleului pe o orbită închisă.
Mișcarea electronului în atomul de hidrogen (sau hidrogenoid) a fost studiată și cu metodele mecanicii cuantice .
Energia potențială a electronului este:
U = − Z e 2 4 π ϵ 0 r , {\displaystyle U=-{\frac {Ze^{2}}{4\pi \epsilon _{0}r}},} unde:
Ecuația lui Schrödinger are forma:
Δ Ψ + 8 π 2 m 0 h 2 ( E + Z e 2 4 π ϵ 0 r ) Ψ = 0 , {\displaystyle \Delta \Psi +{\frac {8\pi ^{2}m_{0}}{h^{2}}}\left(E+{\frac {Ze^{2}}{4\pi \epsilon _{0}r}}\right)\Psi =0,} unde:
Soluțiile în coordonate sferice sunt:
Ψ n l m = ( 1 2 π ) 1 / 2 ⋅ ( 2 n r 0 ) 1 / 2 ⋅ ( 1 2 n π ) 1 / 2 ⋅ {\displaystyle \Psi _{nlm}=\left({\frac {1}{2\pi }}\right)^{1/2}\cdot \left({\frac {2}{nr_{0}}}\right)^{1/2}\cdot \left({\frac {1}{2n\pi }}\right)^{1/2}\cdot } ⋅ [ ( n − l + 1 ) ! [ ( n + 1 ) ! ] 3 ] 1 / 2 ⋅ [ 2 l + 1 2 ⋅ l − | m | ! l + | m | ! ] 1 / 2 ⋅ P l m ( cos θ ) e i m ϕ e − ρ 2 ρ l L n + l 2 l + 1 , {\displaystyle \cdot \left[{\frac {(n-l+1)!}{[(n+1)!]^{3}}}\right]^{1/2}\cdot \left[{\frac {2l+1}{2}}\cdot {\frac {l-|m|!}{l+|m|!}}\right]^{1/2}\cdot P_{l}^{m}(\cos \theta )e^{im\phi }e^{-{\frac {\rho }{2}}}\rho ^{l}L_{n+l}^{2l+1},}
în care:
r 0 = h 2 4 π 2 m 0 e 2 {\displaystyle r_{0}={\frac {h^{2}}{4\pi ^{2}m_{0}e^{2}}}} reprezintă raza atomului de hidrogen în stare fundamentală, iar:
ρ = − 8 π 2 m 0 E h 2 {\displaystyle \rho ={\sqrt {-{\frac {8\pi ^{2}m_{0}E}{h^{2}}}}}} L n + l 2 l + 1 {\displaystyle L_{n+l}^{2l+1}} polinoamele generalizate Laguerre .Pl m (cos θ) sunt funcțiile sferice asociate de gradul l și de ordinul m , iar n , l , m sunt numerele cuantice principal, azimutal, respectiv magnetic.
Soluțiile ecuației sunt compatibile cu realitatea fizică numai pentru anumite valori ale energiei E , numite valori proprii, egale cu:
E n = − m 0 Z 2 e 4 8 ϵ 0 2 n 2 h 2 , {\displaystyle E_{n}=-{\frac {m_{0}Z^{2}e^{4}}{8\epsilon _{0}^{2}n^{2}h^{2}}},} deci energia electronului este cuantificată.
Starea normală sau fundamentală a unui atom hidrogenoid corespunde valorilor n=1, l=0, m=0 ale numerelor cuantice. Funcția de undă are valoarea proprie:
Ψ 100 = 1 ( π r 0 3 ) 1 / 2 ⋅ e − r r 0 {\displaystyle \Psi _{100}={\frac {1}{(\pi r_{0}^{3})^{1/2}}}\cdot e^{-{\frac {r}{r_{0}}}}} și energia are valoarea:
E 1 = − m 0 Z 2 e 4 8 ϵ 0 2 h 2 . {\displaystyle E_{1}=-{\frac {m_{0}Z^{2}e^{4}}{8\epsilon _{0}^{2}h^{2}}}.} 


 French
French Deutsch
Deutsch


![{\displaystyle \cdot \left[{\frac {(n-l+1)!}{[(n+1)!]^{3}}}\right]^{1/2}\cdot \left[{\frac {2l+1}{2}}\cdot {\frac {l-|m|!}{l+|m|!}}\right]^{1/2}\cdot P_{l}^{m}(\cos \theta )e^{im\phi }e^{-{\frac {\rho }{2}}}\rho ^{l}L_{n+l}^{2l+1},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4b1db1cf82e80a004333ca7b0ffc9ecbe7e9c674)





