Гидрид кальция — Википедия
| Гидрид кальция | |
|---|---|
 | |
| Общие | |
| Систематическое наименование | Гидрид кальция |
| Традиционные названия | Гидрид кальция; водородистый кальций |
| Хим. формула | |
| Рац. формула | |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 42,094 г/моль |
| Плотность | 1,70 г/см³ |
| Классификация | |
| Рег. номер CAS | 7789-78-8 |
| PubChem | 105052 и 3033859 |
| Рег. номер EINECS | 232-189-2 |
| SMILES | |
| InChI | |
| ChemSpider | 94784 |
| Безопасность | |
| ЛД50 | 200—450 мг/кг |
| Токсичность | ирритант |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Гидри́д ка́льция — бинарное неорганическое соединение кальция и водорода с химической формулой . Относится к классу солеобразных гидридов.
Применяется для получения газообразного водорода, для твердофазного термического восстановления тугоплавких металлов из их оксидов, в качестве осушающего агента, как аналитический реагент для количественного определения влагосодержания органических жидкостей и кристаллизационной воды в кристаллических веществах.
Физические свойства
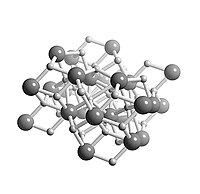
[править | править код]Твёрдое бесцветное кристаллическое вещество. Примесями обычно окрашен в серый цвет. Кристаллизуется в орторомбической сингонии oP12 — кристаллической структуре типа — минерала котунита[1].
Не растворяется в растворителях, с которыми не взаимодействует.
Плавится с разложением при 816 °С. В атмосфере водорода, особенно при повышенном давлении, его пиролиз существенно снижается.
Химические свойства
[править | править код]Является сильным восстановителем.
Взаимодействует с водой, образуя водород и гидроксид кальция:
- кДж.
Взаимодействие с кислотами с образованием водорода и соответствующей кальциевой соли, например:
- .
Окисляется кислородом при температуре свыше 300—400 °С:
- .
Восстанавливает оксиды многих металлов до металла, например:
- .
Получение
[править | править код]Пропусканием водорода над нагретой до температуры около 400 °C стружкой кальция:
- .
Применение
[править | править код]Применяется как удобный твердый источник водорода. 1 кг при взаимодействии с водой образует 1064 л (приведённого к нормальным условиям). Поэтому, несмотря на дороговизну метода, часто используется для наполнения воздушных шаров, оболочек метеорологических зондов и небольших аэростатов водородом. С этой же целью применяется в лабораториях для получения чистого водорода.
Несмотря на то, что его осушающие свойства уступают таким распространённым осушителям как силикагель или пентаоксид фосфора, часто применяется в качестве осушителя органических жидкостей, топлив и смазочных масел.
В лабораторной практике используется для количественного определения содержания воды в топливах и других веществах с помощью волюмометрического анализа, влажность определяется по объёму выделившегося водорода.
Также применяется для восстановления тугоплавких металлов из их оксидов.
В годы Второй мировой войны применялся на подводных лодках для создания ложных мишеней и маскировки подводных лодок от ультразвуковых гидролокаторов противника — так как всплывающие пузырьки водорода хорошо отражают и рассеивают ультразвуковые волны сонаров[2].
Меры безопасности
[править | править код]Вещество токсично. ПДК 180 мг/дм³. При взаимодействии с водой и кислотами выделяет водород, который может образовать взрывоопасные смеси с воздухом. Также при этой реакции образуется едкая щёлочь — гидроксид кальция.
Примечания
[править | править код]- ↑ Wells A. F. (1984) Structural Inorganic Chemistry, Oxford: Clarendon Press. ISBN 0-19-855370-6.
- ↑ McNeil, Ian. An Encyclopedia of the History of Technology. — 2002-06-01. — ISBN 9781134981649. Источник. Дата обращения: 19 февраля 2021. Архивировано 1 августа 2020 года.
Литература
[править | править код]- Химическая энциклопедия / Редкол.: Кнунянц И. Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1971. — Т. 1. — 561 с.
- Справочник химика / Редкол.: Никольский Б. П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.


 French
French Deutsch
Deutsch







