Acetylklorid – Wikipedia
| Acetylklorid | |
 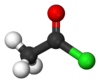 | |
| Systematiskt namn | Etanoylklorid |
|---|---|
| Kemisk formel | CH3COCl |
| Molmassa | 78,498 g/mol |
| Utseende | Färglös vätska |
| CAS-nummer | 75-36-5 |
| SMILES | CC(=O)Cl |
| Egenskaper | |
| Densitet | 1,10 g/cm³ |
| Löslighet (vatten) | Hydrolys |
| Smältpunkt | -112 °C |
| Kokpunkt | 51 °C |
| Faror | |
| Huvudfara | |
| NFPA 704 | |
| LD50 | 910 mg/kg |
| SI-enheter & STP används om ej annat angivits | |
Acetylklorid är ett derivat av ättiksyra och är den enklaste syrakloriden. Den har formeln CH3COCl.
Egenskaper
[redigera | redigera wikitext]Acetylklorid hydrolyseras häftigt vid kontakt med vatten och bildar ättiksyra (CH3COOH) och saltsyra (HCl). Vid kontakt med vattenånga bildas en vit rök av syra löst små vattendroppar.
Framställning
[redigera | redigera wikitext]Acetylklorid kan framställas av ättiksyra (CH3COOH) och tionylklorid (SOCl2).
Användning
[redigera | redigera wikitext]Acetylklorid används ofta vid Friedel-Crafts-acylering där acetylgruppen binds till en kolvätemolekyl med aluminiumklorid som katalysator.
Se även
[redigera | redigera wikitext]Källor
[redigera | redigera wikitext]- Material Safety Data Sheet Mallinckrodt Baker
- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Acetyl chloride, tidigare version.


 French
French Deutsch
Deutsch


