Kväveoxider – Wikipedia
Kväveoxider är föreningar av syre och kväve eller en blandning av sådana föreningar:
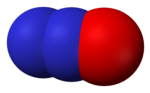
- Kväveoxid, även kallad kvävemonoxid, (NO), kväve(II)oxid
- Kvävedioxid (NO2), kväve(IV)oxid
- Dikväveoxid, lustgas, (N2O), kväve(-I,III)oxid
- Nitrosylazid (N4O), kväve(-I,0,I,II)oxid
- Nitratradikal (NO3), kväve(VI)oxid
- Dikvävetrioxid (N2O3), kväve(II,IV)oxid
- Dikvävetetroxid (N2O4), kväve(IV)oxid
- Dikvävepentoxid (N2O5), kväve(V)oxid
- Trinitramid (N(NO2)3), kväve(III,V)oxid
Inom atmosfärkemi, luftföroreningar och besläktade områden avser kväveoxider NOx (NO och NO2).[1][2]
Bara de tre förstnämnda kan isoleras vid rumstemperatur. N2O3, N2O4 och N2O5 sönderfaller snabbt vid rumstemperatur. NO3, N4O, och N(NO2)3 är mycket reaktiva.
N2O är stabil och tämligen icke-reaktiv i rumstemperatur, medan NO och NO2 är rätt reaktiva men rätt stabila när de isolerats.
Illustrationer
[redigera | redigera wikitext]-
Kväveoxid, NO -
Kvävedioxid, NO2 -
Dikväveoxid, N2O -
Dikvävetrioxid, N2O3 -
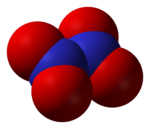
Dikvävetetroxid, N2O4 -
Dikvävepentoxid, N2O5
NOx
[redigera | redigera wikitext]NOx är ett samlingsnamn för de oxider av kväve som uppstår vid förbränning vid höga temperaturer, särskilt i förbränningsmotorer. Främst uppstår kvävemonoxid (NO), som oxideras i luft till kvävedioxid (NO2). Kvävedioxid reagerar sedan med vattenmolekyler (H2O) i luften och bildar salpetersyra (HNO3). NO och NO2 kallas också nitrösa gaser.
Kväveoxiders inverkan på ozonskiktet
[redigera | redigera wikitext]Det bildas naturligt kväveoxider på jordytan genom mikrobiologiska processer och uppe i Jordens atmosfär genom kosmisk strålning som till exempel röntgenstrålning. Men också flygplan, konstgödning och kärnvapenexplosioner skapar kväveoxider som verkar skadande på ozonlagret. Samtidigt bidrar kväveoxider till att ozon bildas.[3]
Källor
[redigera | redigera wikitext]- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Nitrogen oxide, 26 augusti 2012.
- ^ United States Clean Air Act, 42 U.S.C. § 7602
- ^ Seinfeld, John H.; Pandis, Spyros N. (1997), Atmospheric Chemistry and Physics: From Air Pollution to Climate Change, Wiley-Interscience, ISBN 0-471-17816-0
- ^ Titel: Naturen i fokus / sid:63 / Förlag: Focus, Esselte Focus Uppslagsböcker AB, Stockholm 1984, / Huvudredaktör: Professor Kai Curry-Lindahl / ISBN 91-20-04974-9
Se även
[redigera | redigera wikitext]- Lustgas
- Dikvävetetroxid (ibland oegentligt kallat "kvävetetroxid")


 French
French Deutsch
Deutsch