Псевдомембранозний коліт — Вікіпедія
| Псевдомембранозний коліт | |
|---|---|
 Комп'ютерна томографія живота при псевдомембранозному коліті. Виділяється уражена низхідна частина товстої кишки (Colon descendens) | |
| Інші назви | Антибіотикоасоційований коліт Clostridium difficile коліт |
| Спеціальність | інфекційні хвороби |
| Симптоми | гарячка, діарея, блювання, нудота, запор, біль у животі, сверблячка, жовтяниця, диспепсія і печія |
| Ускладнення | токсичний мегаколон, перфорація кишечника, сепсис |
| Причини | Clostridium difficile[1] |
| Фактори ризику | антибіотики, інгібітори протонної помпи |
| Ведення | fecal bacteriotherapyd |
| Препарати | ванкоміцин[2][3], colestyramined[2], colesevelamd[2], colestipold[2], метронідазол[2][3], bacitracin ad[2] і fidaxomicind[3] |
| Класифікація та зовнішні ресурси | |
| МКХ-10 | A04.704.7. |
| DiseasesDB | 2820 |
| MeSH | D004761 |
| | |
Псевдомембранозний коліт або антибіотикоасоційований коліт — захворювання, яке виникає коли нормальна флора кишки сильно ушкоджена антибіотиками (в основному через ятрогенію), що призводить до посиленого розмноження патологічних бактерій, зокрема (Clostridioides difficile) Токсини, які виділяють клостридії, спричинюють гарячку, біль у животі, нудоту, діарею та дегідратацію.
Clostridioides difficile — грампозитивна, анаеробна бактерія, які не входить до складу флори кишки.
Будь-який антибіотик протягом чотирьох тижнів після припинення вживання може спричинити антибіотико-асоційований коліт, .
Через токсини, які виділяють клостридії (цитотоксини: токсин А і токсин В), може розвинутися діарея з дуже тяжким перебігом, значною втратою рідини та дегідратацією. Токсини Clostridioides difficile руйнують шари слизової оболонки і спричинюють значне виділення фібрину, відкладання якого в кишці при колоноскопії описуються як «котячі голови».
У 2002 р. у Північній Америці був описаний штам NAP1 (північноамериканський імпульсний вид типу 1)[4] який може утворювати значно більше токсинів і тому вважається більш вірулентним.
Оскільки Clostridioides difficile значною мірою руйнується в кислому середовищі шлунка, вживання інгібіторів протонної помпи є фактором ризику появи антибіотико—асоційованої діареї.[5]
Крім того, різні антибіотики по-різному сприяють колонізації клостридіями. Лінкозаміди, цефалоспорини та хінолонові антибіотики є найбільш небезпечними при формуванні цього типу діареї. Антибіотики порушують нормальну (фізіологічну) флору кишечника, яка діє як «захисний бар'єр» у здоровій кишці.[6]

Пронос і спазми в животі — основні прояви захворювання, але вони можуть зустрічатися і при багатьох інших захворювань. Тільки у близько 10-20 % всіх пацієнтів із підозрою на C. difficile є позитивний результат при лабораторному дослідженні.
При тяжкому перебігу захворювання, при тяжкій діареї, спостерігається значна втрата рідини. Як ускладнення може виникнути токсичний мегаколон, перфорація товстої кишки, перитоніт і септичний шок.[7]
Такий перебіг захворювання називають фульмінантним колітом. Можна визначити три фактори для прогнозування летального результату: вік старше 70 років, велике збільшення або зниження лейкоцитів і порушення роботи серцево-судинної системи з необхідністю медикаментозної підтримки, іноді інтубації.[8] Штам NAP1 / 027, який був вперше виділений під час епідемії в Квебеку в 2002 році, він демонструє неконтрольоване виділення токсинів in vitro, був пов'язаний з серйознішим перебігом захворювання.[9]
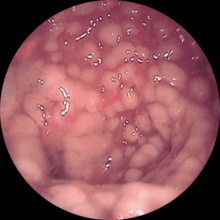
Потовщення кишкової стінки товстої кишки можна побачити при проведенні УЗД та на комп'ютерній томографії. Ендоскопічно спостерігаються світлі відкладення фібрину в товстій кишці, частина з яких плямиста, частина з них злита.
Остаточно допомагає виявити хворобу дослідження калу на наявність збудника або його токсинів. Аналіз цитотоксину — це золотий стандарт. При наявності клостридійних токсинів, мікроскопічно помітні характерні зміни фібробластів.[4]
Одним з найбільш поширених тестів є імуноферментний аналіз на самі токсини, або фермент бактерій (глутаматдегідрогеназу). Обидва тести менш чутливі, ніж попередні методи. Однак вони технічно прості, недорогі й можуть бути виконані протягом декількох годин. Тест на бактеріальний фермент показує лише наявність бактерій, а не їхнє вироблення токсинів. Як результат, є сенс поєднувати обидва тести. Так само використовують ПЛР, яка виявляє ДНК бактерії.[4]
Зауважте, Вікіпедія не дає медичних порад! Якщо у вас виникли проблеми зі здоров'ям — зверніться до лікаря. |
Найважливішим у лікуванні C. difficile-асоційованої діареї є припинення, якщо це можливо, того лікування, що передувало появі діареї. Найчастіше це припинення антибіотикотерапії. Як свідчили давніші дослідження, при легкій формі захворювання (немає гарячки, болю в животі та лейкоцитозу) цього може бути цілком достатньо і діарея минає упродовж 2–3 днів. Якщо припинити антибіотикотерапію неможливо, то слід перейти на препарати з груп низького ризику. При середньотяжких і тяжких формах обов'язкова цілеспрямована антибактеріальна терапія проти C. difficile, нині її призначають і при легких формах (коли у хворого є 3 випорожнення неоформленим калом на добу без лейкоцитозу).[10]
У тяжких випадках терапію розпочинають, не чекаючи лабораторного підтвердження C. difficile-асоційованої етіології. Схемою першого вибору при легких і середньотяжких формах вважають оральне призначення метронідазолу по 0,25 г 4 рази або 0,5 г 3 рази на добу упродовж 10–14 днів. Як терапію другої лінії при невдачі або протипоказаннях для призначення метронідазолу (зокрема вагітним і дітям до 10 років) рекомендують ванкоміцин 0,125 г 4 рази на добу упродовж того ж часу. При неефективності упродовж 3–4 діб, дозу ванкоміцину збільшують до 0,25 г 4 рази на добу, а при потребі (якщо колектомія не показана) — до 0,5 г 4 рази на добу.
Пацієнтам, в яких не вдається досягти успіху при фульмінантному захворюванні, при перфорації кишки або токсичному мегаколоні показане оперативне лікування.
- ↑ Disease Ontology — 2016.
- ↑ а б в г д е NDF-RT
- ↑ а б в Drug Indications Extracted from FAERS — doi:10.5281/ZENODO.1435999
- ↑ а б в J. G. Bartlett: Clostridium difficile: progress and challenges. / Ann N Y Acad Sci. 2010 Dec;1213, S. 62–69, PMID 21175676
- ↑ M. Aseeri, T. Schroeder, J. Kramer, R. Zackula: Gastric acid suppression by proton pump inhibitors as a risk factor for clostridium difficile-associated diarrhea in hospitalized patients. In: Am J Gastroenterol. 2008 Sep;103(9), S. 2308—2313, PMID 18702653.
- ↑ KRINKO-Empfehlung Hygienemaßnahmen bei Clostridioides difficile-Infektion (CDI). 2019, S. 907. [Архівовано 2020-09-18 у Wayback Machine.] Abgerufen am 26. September 2019.
- ↑ Gerd Herold und Mitarbeiter: Innere Medizin. Köln 2013, S. 867 f.
- ↑ E. A. Sailhamer, K. Carson, Y. Chang, N. Zacharias u. a.: Fulminant Clostridium difficile colitis: patterns of care and predictors of mortality. In: Arch Surg. 2009 May;144(5), S. 433—439; discussion 439—440. PMID 19451485.
- ↑ M. Warny, J. Pepin, A. Fang, G. Killgore, A. Thompson u. a.: Toxin production by an emerging strain of Clostridium difficile associated with outbreaks of severe disease in North America and Europe. / Lancet. 2005 Sep 24-30;366(9491), S. 1079—1084. PMID 16182895.
- ↑ Журнал «Медицина світу» - Журнал для широкого кола лікарів. msvitu.com. Процитовано 28 липня 2020. (рос.)
- Cleary R.K. Clostridium difficile-associated diarrhea and colitis: clinical manifestations, diagnosis, and treatment. Dis Colon Rectum. Nov 1998;41(11):1435-49.
- Giesemann T., Egerer M., Jank T., Aktories K. Processing of Clostridium difficile toxins. J Med Microbiol. 2008 Jun;57(Pt 6):690-6.
- Sailhamer E.A., Carson K., Chang Y., et al. Fulminant Clostridium difficile colitis: patterns of care and predictors of mortality. Arch Surg. May 2009;144(5):433-9; discussion 439-40.
- Lysiuk, Yu S.; Kohut, L. M.; Romanchak, D. L.; Voytovych, O. V. (2017). Псевдомембранозний коліт — практичні аспекти діагностики і лікування (короткий огляд літератури). Шпитальна хірургія. Журнал імені Л. Я. Ковальчука (4). с. 96–101. ISSN 2414-4533. doi: 10.11603/2414-4533.2017.4.8016
- Посохова К. А. Антибіотик-асоційоване ураження кишечнику / К. А. Посохова // Інфекційні хвороби. -2010. -№ 4. -С. 69-80.
- Sartelli, M., Malangoni, M.A., Abu-Zidan, F. M., Griffiths, E.A., Bella, S.D., McFarland, L.V., & Eltringham, I. (2015). WSES guidelines for management of Clostridium difficile infection in surgical patients. World Journal of Emergency Surgery, 10(38), 1-23.
- Al-Jashaami, Layth & DuPont, Herbert. (2016). Management of Clostridium difficile Infection. Gastroenterology & Hepatology. 12. 609—616
| Це незавершена стаття про хворобу, синдром або розлад. Ви можете допомогти проєкту, виправивши або дописавши її. |


 French
French Deutsch
Deutsch