4-Thujole – Wikipedia
| 4-Thujole | ||
| Name | cis-4-Thujol | trans-4-Thujol |
| Strukturformel | 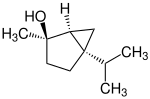 |  |
| CAS-Nummer | 117305-49-4 | 7712-82-5 |
| 546-79-2 | ||
| PubChem | 62367 | |
| Wikidata | Q27101876 | |
| Summenformel | C10H18O | |
| Molare Masse | 154,14 g·mol−1 | |
4-Thujole (auch 4-Thujanole oder Sabinenhydrat) sind eine Gruppe stereoisomerer Terpenalkohole. Von den 3-Thujolen unterscheiden sie sich durch die Position der Hydroxylgruppe.
Vorkommen
[Bearbeiten | Quelltext bearbeiten]4-Thujole kommen in verschiedenen ätherischen Ölen vor, in dem von Thymian[1] und von Türkischem Oregano[2] kommen beide Isomere vor. In der Thymianart Thymus satureiodes kommt trans-4-Thujol vor[3], in der Oregano-Unterart Origanum bastetanum etwa 30 % cis-4-Thujol.[4] Auch in mehreren Arten der Gattung Artemisia kommen 4-Thujole vor.[5][6] Sonnenblumen enthalten Ester die aus einer Kaurancarbonsäure und einem 4-Thujol als Alkoholkomponente bestehen.[7]
4-Thujole wirken vermutlich auch als Kairomone, anhand derer Käfer den Gesundheitszustand von Bäumen einschätzen und dadurch möglichst geschwächte Bäume als Nahrungsquelle auswählen können. Fichtenrinde sondert trans-4-Thujol ab, das von Buchdruckern detektiert werden kann. Die Gemeine Thuja sondert cis-4-Thujol ab, das von Phloeosinus aubei (Familie Rüsselkäfer) detektiert wird.[8][9][10]
- Thymian
- Artemisia pontica
- Türkischer Oregano
- Sonnenblume
Gewinnung
[Bearbeiten | Quelltext bearbeiten]Als Ausgangspunkt für die Synthese von trans-4-Thujol kann (−)-3-Thujol verwendet werden. Dazu wird zunächst die Hydroxygruppe mesyliert und dann mit Kaliumhydroxid und [18]Krone-6 eliminiert. Dadurch entstehen zwei positionsisomere Alkene von denen eines selektiv hydroxyliert werden kann. Hierzu wird ein Syntheseschritt mit gleichzeitiger Oxidation und Reduktion angewandt. Durch Lösung mit dem Zwischenprodukt, Bengalrosa und Tetrabutylammoniumborhydrid in Chloroform wird während Bestrahlung mit einer Natriumlampe konstant Sauerstoff strömen gelassen. Der entstehende Allylalkohol kann dann zu trans-4-Thujol hydriert werden.[11]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]4-Thujanole wirken antibakteriell gegen verschiedene Arten, insbesondere gram-negative.[1]
Verwendung
[Bearbeiten | Quelltext bearbeiten]4-Thujanole werden als Duftstoff in Shampoos, Parfum und anderen Kosmetika, sowie in Reinigungs- und Waschmitteln verwendet. Die jährlich weltweit verwendete Menge (Stand 2008) ist mit unter 100 kg gering.[12] Das Stereoisomerengemisch ist in der EU unter der FL-Nummer 02.085 als Aromastoff für Lebensmittel allgemein zugelassen.[13]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b D. Vokou, S. Kokkini, J-M. BessiÈRe: Origanum onites (Lamiaceae) in Greece: Distribution, volatile oil yield, and composition. In: Economic Botany. Band 42, Nr. 3, Juli 1988, S. 407–412, doi:10.1007/BF02860163.
- ↑ D. Vokou, S. Kokkini, J-M. BessiÈRe: Origanum onites (Lamiaceae) in Greece: Distribution, volatile oil yield, and composition. In: Economic Botany. Band 42, Nr. 3, Juli 1988, S. 407–412, doi:10.1007/BF02860163.
- ↑ J. D. Miquel, H. M. J. Richard, F. G. Sandret: Volatile constituents of Moroccan thyme oil. In: Journal of Agricultural and Food Chemistry. Band 24, Nr. 4, Juli 1976, S. 833–835, doi:10.1021/jf60206a038.
- ↑ Oswaldo Socorro, Inmaculada Tárrega, Francisco Rivas: Essential oils from wild and micropropagated plants of Origanum bastetanum. In: Phytochemistry. Band 48, Nr. 8, August 1998, S. 1347–1349, doi:10.1016/S0031-9422(97)00926-6.
- ↑ Flora Haider, Narendra Kumar, Ali Arif Naqvi, Guru Das Bagchi: Oil Constituents of Artemisia nilagirica var. septentrionalis Growing at Different Altitudes. In: Natural Product Communications. Band 5, Nr. 12, Dezember 2010, S. 1934578X1000501, doi:10.1177/1934578X1000501227.
- ↑ Kiplimo, Joyce J., et al. "Chemical composition and larvicidal activity of essential oil of Artemisia pontica." (2016).
- ↑ Jan St. Pyrek: Neutral Diterpenoids of Helianthus annuus. In: Journal of Natural Products. Band 47, Nr. 5, September 1984, S. 822–827, doi:10.1021/np50035a012.
- ↑ Christian Schiebe, C. Rikard Unelius, Suresh Ganji, Muhammad Binyameen, Göran Birgersson, Fredrik Schlyter: Styrene, (+)-trans-(1R,4S,5S)-4-Thujanol and Oxygenated Monoterpenes Related to Host Stress Elicit Strong Electrophysiological Responses in the Bark Beetle Ips typographus. In: Journal of Chemical Ecology. Band 45, Nr. 5-6, Juni 2019, S. 474–489, doi:10.1007/s10886-019-01070-8, PMID 31053976, PMC 6570694 (freier Volltext).
- ↑ Anna Jirošová, Blanka Kalinová, Roman Modlinger, Rastislav Jakuš, C. Rikard Unelius, Miroslav Blaženec, Fredrik Schlyter: Anti‐attractant activity of (+)‐ trans ‐4‐thujanol for Eurasian spruce bark beetle Ips typographus : Novel potency for females. In: Pest Management Science. Band 78, Nr. 5, Mai 2022, S. 1992–1999, doi:10.1002/ps.6819.
- ↑ G. Bozsik, A. Tröger, W. Francke, G. Szőcs: Thuja occidentalis : identification of volatiles and electroantennographic response by the invasive cedar bark beetle, Phloeosinus aubei. In: Journal of Applied Entomology. Band 140, Nr. 6, Juli 2016, S. 434–443, doi:10.1111/jen.12272.
- ↑ Peter Baeckström, Bohumir Koutek, David Šaman, Jan Vrkoč: A convenient synthesis of trans-sabinene hydrate from (−)-3-thujol via a highly selective ene reaction of singlet oxygen. In: Bioorganic & Medicinal Chemistry. Band 4, Nr. 3, März 1996, S. 419–421, doi:10.1016/0968-0896(96)00020-X.
- ↑ S.P. Bhatia, C.S. Letizia, A.M. Api: Fragrance material review on 4-thujanol. In: Food and Chemical Toxicology. Band 46, Nr. 11, November 2008, S. S295–S296, doi:10.1016/j.fct.2008.06.024.
- ↑ Food and Feed Information Portal Database | FIP. Abgerufen am 31. August 2023.


 French
French Deutsch
Deutsch


