Carbocatione
In chimica organica, si definisce carbocatione (talvolta chiamato impropriamente "ione carbonio"[1]) un catione derivato da una molecola organica la cui carica risiede su un atomo di carbonio. La carica positiva rende la particella estremamente reattiva, in grado di legarsi ad anioni o di sottrarre elettroni da altre molecole vicine (in altre parole, si comportano da elettrofili[2]).
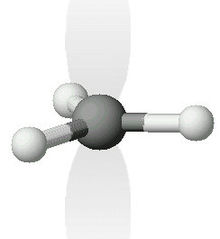
I carbocationi alchilici derivano dagli alcani per scissione eterolitica[3] e hanno una geometria simile a quella dei radicali alchilici: l'atomo di carbonio che reca la carica positiva ha ibridazione sp2, e ha quindi struttura planare; l'orbitale p perpendicolare al piano del carbocatione, non coinvolto nell'ibridazione, è vuoto.
Sebbene i carbocationi alchlici siano piuttosto instabili, nel 1962 George A. Olah mise a punto la loro preparazione in pentafluoruro di antimonio (SbF5), dove risultano abbastanza stabili per essere rilevati con indagini spettroscopiche.[4]
Stabilità
[modifica | modifica wikitesto]Similmente ai radicali, sono detti primari i carbocationi alchilici aventi struttura R-CH2+, secondari quelli aventi struttura R2CH+ e terziari quelli aventi struttura R3C+.
CH3-CH2-CH2-CH2+ carbocatione primario
+ CH3-CH2-CH-CH3 carbocatione secondario
+ CH3-C-CH3 | carbocatione terziario CH3
Il carattere primario, secondario o terziario influisce sulla stabilità e sulla reattività dei carbocationi in misura ancora maggiore a quanto avviene per i corrispondenti radicali.
Oltre all'effetto induttivo stabilizzante esercitato dai gruppi R vicini, fondamentale è anche l'iperconiugazione. L'ordine di stabilità dei carbocationi alchilici è terziario > secondario > primario.[5] [6]
I carbocationi possono essere anche stabilizzati per risonanza, quando sono coniugati a sistemi π quali doppi legami o anelli aromatici.
CH2=CH-CH2+ ↔ +CH2-CH=CH2 carbocatione allilico
Ph-CH2+ carbocatione benzilico
Particolarmente stabile è il trifenilmetil catione (o catione tritile), ovvero un carbonio portante tre fenili come sostituenti; questo perché la carica positiva viene delocalizzata per risonanza su tutti gli anelli. Il catione fenile invece è molto instabile perché essendo l'orbitale p vuoto perpendicolare al sistema π del benzene, la carica non può essere delocalizzata.
Riarrangiamento
[modifica | modifica wikitesto]I carbocationi subiscono trasposizione (o riarrangiamento), ovvero la migrazione di un atomo di idrogeno o di un gruppo alchilico da un atomo adiacente all'atomo di carbonio carico positivamente (migrazione 1-2). La trasposizione avviene sempre in direzione tale da stabilizzare il carbocatione, quindi i carbocationi primari si trasformano in secondari e terziari e i secondari in terziari.
+ + CH3-CH2-CH-CH2 CH3-CH2-C-CH3 | → | da primario a secondario H H
CH3 CH3 | | CH3-C-CH-CH3 → CH3-C-CH-CH3 da secondario a terziario | + + | CH3 CH3
La trasposizione spiega, ad esempio, perché la disidratazione di un alcol lineare porta a una miscela di prodotti, alcuni anche a catena ramificata, anziché al solo alchene lineare corrispondente. Il passaggio intermedio della reazione è un carbocatione che, prima di perdere uno ione H+ e formare l'alchene, subisce trasposizioni.
Note
[modifica | modifica wikitesto]Bibliografia
[modifica | modifica wikitesto]- T. W. Graham Solomons, Chimica organica, a cura di G. Ortaggi, D. Misiti, 2ª ed., Bologna, Zanichelli, 1988, ISBN 88-08-09414-6. URL consultato il 22 ottobre 2009 (archiviato dall'url originale il 18 gennaio 2012).
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su carbocatione
Wikimedia Commons contiene immagini o altri file su carbocatione
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) IUPAC Gold Book, "carbocation", su goldbook.iupac.org.
- Mnemochimica, "Carbocationi:Cosa sono? Stabilità e Trasposizione", su mnemochimica.it.
- Stabilità dei carbocationi (PDF), su chimica.unipd.it. URL consultato il 16 luglio 2009 (archiviato dall'url originale il 7 marzo 2010).
| Controllo di autorità | GND (DE) 4147294-9 · J9U (EN, HE) 987007537259205171 · NDL (EN, JA) 00565062 |
|---|


 French
French Deutsch
Deutsch