ノーベリウム
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 外見 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 不明 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 一般特性 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 名称, 記号, 番号 | ノーベリウム, No, 102 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 分類 | アクチノイド | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 族, 周期, ブロック | n/a, 7, f | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子量 | [259] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 電子配置 | [Rn] 5f14 7s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 電子殻 | 2, 8, 18, 32, 32, 8, 2(画像) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 物理特性 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 相 | 固体 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度(室温付近) | 9.9±0.4 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 融点 | 827 (推定) °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子特性 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 酸化数 | 2(安定), 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| イオン化エネルギー | 第1: 641.6 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 第2: 1254.3 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 第3: 2605.1 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 共有結合半径 | 176 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| その他 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 結晶構造 | 面心立方格子 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS登録番号 | 10028-14-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 主な同位体 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細はノーベリウムの同位体を参照 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ノーベリウム (英: nobelium [noʊˈbɛliəm, noʊˈbiːliəm]) は原子番号102の人工放射性元素で、元素記号は No である。名称はダイナマイトの開発者で科学を後援したアルフレッド・ノーベルに由来する。放射性金属、10番目の超ウラン元素で、アクチノイド系列の末尾の数字から2番目の元素である。原子番号が100を超えるすべての元素と同様に、ノーベリウムは粒子加速器でそれより軽い元素に荷電粒子を衝突させることによってのみ生成することができる。ノーベリウムの同位体は12種が存在し、最も安定なものは半減期58分の259Noである。259Noよりも半減期が短い255No(半減期3.1分)は大規模な生成が可能で、化学分野では最も一般的に使用される。
化学実験ではノーベリウムは周期表のイッテルビウムより重い同族体として振る舞うことが確認されている。ノーベリウムの化学的性質は完全判明しておらず、ほとんどは水溶液中でのみ知られる。ノーベリウムが発見される以前は、ほかのアクチノイドに特徴的な+3の酸化数と同様に安定な+2状態を示すと予想されていたが、のちに水溶液中では +2 が +3 よりもはるかに安定で、ノーベリウムを+3状態に保つことが難しいことが判明して予想は確認された。
1950年代と1960年代にスウェーデン、ソ連、アメリカ合衆国の研究所からノーベリウムの発見について多くの主張がなされた。スウェーデンの科学者はすぐにその主張を撤回したが、発見の優先度と元素の命名についてソ連とアメリカの科学者の間で論争となった。IUPAC は1997年にソ連による発見を認めたが、スウェーデンが提案したノーベリウムの名称は、文献で長年使用されていたことから維持された。
発見
[編集]
元素102の発見には複雑な過程があり、スウェーデン、ソ連、アメリカ合衆国のグループにより発見が主張された。検出に関して最初の完全で議論の余地がない報告は、1966年に当時ソ連のドゥブナ合同原子核研究所からされたものである[1]。
元素102の発見について最初の発表は、1957年にスウェーデンのノーベル研究所の物理学者らによるものである。研究チームはキュリウムの標的粒子に13Cイオンを30分間隔で25時間照射したことを報告した。照射の間、ターゲットのイオン交換化学が行われた。50回の照射のうち12回は (8.5±0.1) メガ電子ボルト (MeV) のアルファ粒子を放出する試料を含んでいたが、これはフェルミウム(原子番号 Z=100)およびカリホルニウム (Z=98) よりも早く溶出する滴形状の試料であった。報告された半減期は10分で、251102 もしくは 253102 が割り当てられたが、観測されたアルファ粒子が元素102の電子捕獲により生じた短命のメンデレビウム (Z=101) の同位体に由来する可能性を排除することができなかった[1]。チームがこの新元素にノーベリウム (nobelium, No) の名称を提案[2][3]すると IUPAC はすぐにこの名称を承認した[4]が、ドゥブナのグループは1968年の時点では早急であったとしている[5]。1958年にアメリカローレンス・バークレー国立研究所の科学者たちは実験を繰り返したが、背景効果がない 8.5 MeV の現象を見つけることはできなかった[1]。
1959年にスウェーデンのチームは、1958年にバークレーのチームが元素102を検出できなかったことの説明を試み、自身が発見したことを支持した。のちの研究により半減期が3分を超える 259No よりも軽いノーベリウムの同位体は存在せず、スウェーデンの実験ではそれよりも重い同位体は生成できず、スウェーデンのチームの結果は半減期が8分で、すぐにトリプルアルファ崩壊を経て 8.53612MeV の崩壊エネルギーを持つ213Poに変化する 225Th によるものである可能性が高いことが示された。この仮説は 225Th が使用された反応で容易に生成され、使用された化学的手法では分離されない事実により重みづけられている。後年の研究で、2価の状態は3価の状態よりも安定で、アルファ粒子を放出する試料にはノーベリウムが含まれていないことが示された。2価のノーベリウムは他の3価のアクチノイドでは溶出しなかった[1]。これらの結果からスウェーデンは主張を撤回してその活動を背景効果に関連付けた[4]。
アルバート・ギオルソ、グレン・シーボーグ、John R. Walton、Torbjørn Sikkeland からなるバークレーのチームは、1958年に元素102の合成を主張した。このチームは新たな重イオン線形加速器 (HILAC) を用いてキュリウム(244Cm 95%、246Cm 5%)に 13C と 12C イオンを衝突させた。彼らはスウェーデンのチームにより主張された 8.5MeV の活動を確認することはできなかったが、フェルミウム250からの崩壊を検出することができた。これは見かけの半減期が約3秒である 254102( 246Cmから生成された)の娘粒子である。のちの1963年のドゥブナの研究でも 254102 がこの反応で生成されることが確認されたが、その半減期は実際には50±10秒であった。1967年にバークレーのチームは、発見された同位体は確かに 250Fm であったが、半減期測定が実際に関係していた同位体は 244Cf であって、これはより多い 244Cm から生成された孫娘粒子である崩壊生成物であったと述べ、自身の研究を擁護しようとした。エネルギーの違いはこれまで報告されていなかった「分解能とドリフトの問題」に起因したもので、他の結果にも影響を与えていたはずである。1877年の実験で 252102 は実際に2.3秒の半減期を持つことが示された。1973年の研究で、 250Fm の反跳も使われるエネルギーで反応中に形成された可能性のある 250mFm の異性体転移(半減期1.8秒)から容易に生成されたことも示されている[1]。このことから、この実験ではノーベリウムは実際には生成されなかった可能性が高い[1]。
1959年に、チームは研究を続けておもに 8.3MeV のアルファ粒子を放出して崩壊し、半減期3秒で30%の自発核分裂分岐を伴う同位体を生成できた、と主張した。この活動は当初 254102 とされていたが、のちに 252102 に変更され、困難な条件のためにノーベリウムが生成されたことは確実ではないことも言及した[1]。バークレーのチームは、スウェーデンのチームが提案したノーベリウムという元素名を採用することを決定した[4]。
- 244
96Cm + 12
6C → 256
102No*
→ 252
102No + 4 1
0n
ドゥブナでは1958年と1960年に元素102の合成を目指した実験が行われた。最初の1958年の実験では239, 241Puに16Oイオンを衝突させた。8.5 MeVを超えるエネルギーを持つアルファ崩壊がいくつか観測され、251, 252, 253102が割り当てられたが、チームは鉛やビスマスの不純物から同位体が生成されてしまった(ノーベリウムは生成されない)可能性を除外できないと書いている。後に行われた1958年の実験では水銀、タリウム、鉛、ビスマスの不純物から新しい同位体が生成されることが指摘されたが、科学者たちは半減期が30秒以下、崩壊エネルギーが8.8 ± 0.5 MeVであることに言及し、この反応から元素102が生成されるという結論を支持していた。後の1960年の実験ではこれらが背景効果であることが証明された。1967年の実験でも崩壊エネルギーは8.6 ± 0.4 MeVまで下がったが、いずれも253Noや254Noの値と一致するには高すぎる値であった[1]。その後ドゥブナのチームはまず1970年に、そして1987年に再度これらの結果は決定的なものではないと述べている[1]。
1961年、バークレーの科学者たちはカリホルニウムとホウ素イオンと炭素イオンの反応で元素103を発見したと主張した。彼らは同位体257103の生成を主張し、また、15秒の半減期とアルファ崩壊のエネルギー8.2 MeVを持つ元素102のアルファ崩壊同位体を合成したと主張し、これを255102に割り当てたが、その理由は示さなかった。この値は現在知られている257Noの値と一致しているが、255Noについて現在知られている値とは一致しておらず、この同位体が今回の実験で一役買っていたと考えられるもその発見は決定的なものではなかった[1]。
ドゥブナでも元素102の研究は続けられ、1964年には238Uとネオンイオンの反応によって元素102を合成し、元素102のアルファ崩壊の娘粒子を検出する実験が行われた。生成物を銀キャッチャー箔で運び化学的に精製し、同位体250Fmと252Fmが検出され、この実験で252Fmが得られたことは親粒子にあたる256102も合成された証拠と解釈された。この反応では余剰な中性子と同時にアルファ粒子が放出されて252Fmが直接生成される可能性もあるが、252Fmがキャッチャー箔に直接行かないようにする措置がとられた。256102に対して検出された半減期は8秒であり、これはもっと新しい1967年の値である(3.2 ± 0.2)秒よりもずっと大きい[1]。1966年には254102に向けて243Am(15N,4n)254102と238U(22Ne,6n)254102の反応を用いた実験が行われ、半減期が(50 ± 10)秒であることが分かった。当時はこの値とそれより早いバークレーの実験の値の矛盾は理解されなかったが、後の研究により250mFmの異性体の形成の可能性はバークレーの実験よりもドゥブナの実験の方が低いことが分かった。今から考えると254102についてのドゥブナの実験結果はおそらく正しいものであり、現在では元素102の決定的な検出と考えられている[1]。
再度同じ2つの反応を使用したドゥブナによる非常に説得力のあるさらなる実験が1966年に発表され、254102は実際にはバークレーが主張する3秒よりもはるかに長い半減期を持っていると結論付けられた[1]。その後1967年にバークレーで、1971年にオークリッジ国立研究所で行われた研究で元素102の発見が完全に確認され、それ以前の観測がはっきりした[4]。1966年12月、バークレーのグループはドゥブナの実験を繰り返しこれを完全に確認し、このデータを用いて以前に合成したが当時はまだ同定できなかった同位体を最終的に割り当て、1958年から1961年にノーベリウムを発見したと主張した[4]。
- 238
92U + 22
10Ne → 260
102No*
→ 254
102No + 6 1
0n
1969年、ドゥブナのチームは元素102の化学実験を行い、イッテルビウムの重い同族体として振る舞うという結論を出した。ロシアの科学者たちはそのころ死去したイレーヌ・ジョリオ=キュリーにちなんでジョリオチウム(joliotium, Jo)という名前を提案した。これにより元素の命名について論争が生まれ、これは数十年にわたって解決されず、それぞれのグループが自身が提案した名称を使用していた[4]。
1992年、IUPAC-IUPAP Transfermium Working Group (TWG) は発見の主張を再評価し、1966年のドゥブナの研究のみが原子番号102の原子核を正しく検出し、崩壊を割り当てたと結論付けた。したがって、1959年にバークレーでノーベリウムが検出された可能性はあるが、ドゥブナのチームがノーベリウムを発見したと公式に認められている[1]。しかし、この決定は翌年にバークレーに批判された。彼らは元素101から103までの事例の再開は「時間の無駄」と断じたが、ドゥブナはIUPACの決定に同意した[5]。
1994年、元素の命名についての論争を解決する試みの一環としてIUPACは101から109の元素の名前を批准した。元素102についてはここ30年の間に文献に定着していたこと、及びアルフレッド・ノーベルがこのような形で記念されるべきであるとしてノーベリウムという名前を批准した[6]。この発見者の選択を尊重していない決定に対する反発によりコメント期間が設けられ、1995年にIUPACは新たな提案の一部としてゲオルギー・フリョロフまたはフリョロフ核反応研究所のいずれかにちなみ元素102をフレロビウム(flerovium, Fl)と命名した[7]。この提案も受け入れられず、1997年にノーベリウムという名称に戻った[6]。今日、フレロビウムという名称は同じ元素記号で元素114を指す[8]。
特徴
[編集]物理的性質
[編集]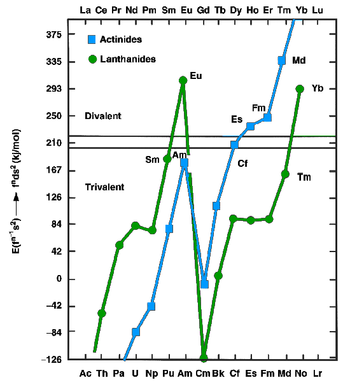
周期表において、ノーベリウムはアクチノイドであるメンデレビウムの右、同じくアクチノイドであるローレンシウムの左、ランタノイドのイッテルビウムの下に位置している。ノーベリウムの金属はまだバルク量では調製されておらず、バルク調製は現在のところ不可能である[10]。しかし、その特性に関して多くの予測といくつかの予備的な実験結果が行なわれている[10]。
ランタノイド及びアクチノイドは金属状態では2価の金属(ユウロピウムやイッテルビウム)または3価の金属(他のほとんどのランタノイド)のいずれかとして存在する。前者はfn+1s2配置を有するのに対し、後者はfnd1s2配置を有する。1975年、JohanssonとRosengrenは2価と3価の金属ランタノイドと金属アクチノイドの凝集エネルギー(結晶化のエンタルピー)の測定値と予測値を研究した[11][12]。結論はノーベリウムの[Rn]5f147s2配置に対する[Rn]5f136d17s2配置の結合エネルギーの増加は、ずっと後半のアクチノイドにも当てはまるように1個の5f電子を6dに促進するのに必要なエネルギーを保証するのに十分ではないというものであった。したがって、アインスタイニウム、フェルミウム、メンデレビウムおよびノーベリウムは2価の金属であると予想されたが、この予想は未だ確認されていない[11]。アクチノイド系列の最後に行くずっと前に2価の状態が優勢になるのは、原子番号の増加に伴って増加する5f電子の相対論的安定化に起因する。この効果はノーベリウムが他のすべてのランタノイドやアクチノイドとは異なり主に3価ではなく2価になることである[13]。1986年に金属ノーベリウムの昇華エンタルピーは126 kJ/molと推定され、この値はアインスタイニウム、フェルミウム、メンデレビウムの値に近く、ノーベリウムが2価の金属を形成するという理論を支持している[10]。他の2価の後半のアクチノイド(3価のローレンシウムを除く)と同様、金属ノーベリウムは面心立方晶構造を仮定する[14]。2価のノーベリウム金属は約197 pmとされている[10]。ノーベリウムの融点は827 °Cと予測されており、隣のメンデレビウムの予測値と同じ値である[15]。密度は約9.9 ± 0.4 g/cm3と予測されている[14]。
化学的性質
[編集]ノーベリウムの化学的性質は未解明のところが多く、水溶液中のものしか知られていない。水溶液中では+3か+2の酸化数をとることができるが、後者の方が安定である[2]。ノーベリウム発見以前は、溶液中での元素102の振る舞いは他のアクチノイドとの類推から、3価の状態が安定であると予想されてきた。しかし、シーボーグは1949年にNo2+イオンが充填した[Rn]5f14殻を含む基底状態の電子配置を持つことから、+2の酸化数も比較的安定であることを予測し、19年後にこの仮説が実証された[16]。
1967年、ノーベリウムの化学的振る舞いをテルビウム、カリホルニウム、フェルミウムのものと比較する実験が行われた。4つの元素全てを塩素と反応させ、得られた塩化物をチューブに沿って堆積させ、それに沿って気体により移動させた。その結果生成されたノーベリウム塩化物は固体表面に強く吸着し他の3元素の塩化物のように揮発性ではないことが分かった。しかしNoCl2とNoCl3の両方とも不揮発性を示すと予想されていたため、この実験ではノーベリウムの好ましい酸化状態が何であるかについては結論が出なかった[16]が、翌年陽イオン交換クロマトグラフィーと共沈実験が約5万個の255No原子で実験され、ノーベリウムは+2の酸化数を好むという結論が出た。これにより、強い酸化剤が存在しない場合、溶液中でのノーベリウムは2価の状態が最も安定であることが示された[16]。No2+イオンは他のアクチノイドとは異なり、2価のアルカリ土類金属に近い振る舞いを示し、クエン酸、シュウ酸、酢酸との間に錯体を形成することが知られている[17]。
1974年に行われた実験ではノーベリウムはアルカリ土類金属とCa2+とSr2+の間で溶出することが示された[16]。ノーベリウムは水溶液中で+2の酸化数が最も一般的で安定な唯一知られているfブロック元素である。これはアクチノイド系列の末端にある5f軌道と6d軌道の間に大きなエネルギーギャップがあるためである[18]。
7s亜殻の相対論的安定化は二水素化ノーベリウムNoH2を大きく不安定化させ、6d3/2スピノル以上の7p1/2スピノルの相対論的安定化はノーベリウム原子の励起状態が予想される6dの寄与ではなく、7sと7pの寄与を持つことを意味する。NoH2分子における長いNo-Hの距離と大きい電荷移動が、この分子の双極子モーメントが5.94 Dと極端なイオン性につながっている。この分子ではノーベリウムが典型元素のような振る舞いを示すことが予測されており、具体的にはそのns2価電子殻配置とコアのような5f軌道を持つアルカリ土類金属のような振る舞いをする[19]。
ノーベリウムの塩化物イオンと錯体形成する能力は、バリウムのそれに最も似ており、むしろ弱く錯体形成する[16]。0.5M硝酸アンモニウム水溶液中のクエン酸塩、シュウ酸塩、酢酸塩と錯体形成する能力は、カルシウムとストロンチウムの間であるが、ストロンチウムのそれに幾らか近い[16]。
E°(No3+→No2+)カップルの標準酸化還元電位は1967年に+1.4から+1.5Vと推定されたが[16]、後の2009年に約+0.75Vであることが判明した[20]。正の値であることはNo2+がNo3+よりも安定でありNo3+が優れた酸化剤であることを示している。E°(No2+→No0)とE°(No3+→No0)の値は情報ソースにより異なるが、標準的な推定値は−2.61と−1.26Vである[16]。E°(No4+→No3+)カップルの値は+6.5Vになると予測されている[16]。No3+とNo2+形成のギブスの自由エネルギーはそれぞれ−342kJ/molと−480kJ/molと推定されている[16]。
原子
[編集]ノーベリウム原子には102個の電子があり、そのうち3つが価電子としてはたらく。これらは[Rn]5f147s2(基底状態項記号1S0)の配置であることが予測されているが、この電子配置の実験的検証は2006年現在では行われていない[10]。化合物を形成するときには3つの価電子が全て失われ、[Rn]5f13コアが残る可能性がある。このことは[Rn]5fn電子配置が3価状態である傾向に一致する。しかしながら、2つの価電子のみが失われ5f14殻が満たされ安定した[Rn]5f14コアが残る可能性の方が高い。ノーベリウムの第1イオン化ポテンシャルは7s電子が5f電子の前にイオン化するという仮定に基づき1974年に最大(6.65 ± 0.07) eVと測定された[21]。この値はノーベリウムが希少であり高い放射能を持っているという理由から、さらに洗練はされていない[22]。6配位と8配位のNo3+のイオン半径は1978年にそれぞれ約90pmと102pmと概算されていた[16]。No2+のイオン半径は2つの有効数字に対して実験的に100pmであることが分かっている[10]。No2+の水和エンタルピーは1486kJ/molと計算されている[16]。
同位体
[編集]ノーベリウムの同位体、質量数250から260と262の12種類が知られており、全て放射性同位体である[23]。さらに、質量数251、253、254の核異性体が知られている[24][25]。これらのうち最も長寿命である同位体は半減期58分の259Noであり、最も長寿命である異性体は半減期1.7秒の251mNoである[24][25]。しかし、まだ発見されていない同位体である261Noはそれより長い170分の半減期を持つと予測されている[24][25]。短寿命の255No(半減期3.1分)は249Cfに12Cイオンを照射することで大量に生成できるため、化学実験によく用いられている[23]。259Noと255Noの次に安定なノーベリウムの同位体は253No(半減期1.62分)、254No(51秒)、257No(25秒)、256No(2.91秒)、252No(2.57秒)である[23][24][25]。残りのノーベリウムの同位体は全て半減期が1秒以下であり、最も短寿命なノーベリウムの同位体(250No)は半減期が0.25ミリ秒である[23][24][25]。同位体254Noは231Paから279Rgまでの一連の扁長核の中間にあり、その核異性体(うち2つが知られている)の形成は球状の陽子殻のすぐ上にくる2f5/2のような陽子軌道により制御されているため、理論的には特に興味深い。これは208Pbと48Caを反応させることで合成できる[26]。
ノーベリウムの同位体の半減期は250Noから253Noまではなめらかに増加するが、254Noで沈み、これを超えると自発核分裂が支配的な崩壊モードとなって偶数-偶数ノーベリウム同位体の半減期は急激に減少する。例えば、256Noの半減期は3秒近くであるが、258Noの半減期は1.2ミリ秒に過ぎない[23][24][25]。このことはノーベリウムではアクチノイド系列の長寿命核の領域、すなわち安定の島に陽子の相互反発による限界があることを示している[27]。偶数-奇数ノーベリウム同位体は質量数の増加に伴って半減期が長くなり、この傾向は257Noで減少に転じる[23][24][25]。
精製
[編集]ノーベリウムの同位体は、262Lrの娘粒子として生成される262Noを除き、そのほとんどがアクチノイドの標的粒子(ウラン、プルトニウム、キュリウム、カリホルニウム、アインスタイニウム)に衝突させることにより生成される[23]が、最も一般的に使用される同位体の255Noは248Cmや249Cfに12Cを照射することにより生成される。後者の方法の方がより一般的であるとされ、249Cfの350μg cm−2のターゲットに毎秒3兆個(3 × 1012)の73MeVの12Cイオンを10分間照射することで、約1200個の255No原子を生成することができる[23]。
255Noが生成されると、隣のアクチノイドであるメンデレビウムを精製するために使われるのと同様の方法で分離することができる。生成された255No原子の反跳運動量はそれらが生成されたターゲットから物理的に遠ざけるために使われ、真空中でターゲットのすぐ後ろにある金属(通常はベリリウム、アルミニウム、白金、金)の薄い箔の上に移動する。これは通常雰囲気ガス(しばしばヘリウム)でノーベリウム原子をトラップし、反応チャンバーの小さな開口部からガスジェットとともにそれを運ぶことにより結合される。長い毛細管を使用し、ヘリウムガス中に塩化カリウムのエアロゾルを含めることでノーベリウム原子を数十メートルにわたって運ぶことができる[28]。箔上に集められたノーベリウムの薄層は箔を完全に溶解させずに希酸で除去することができる[28]。他の3価のアクチノイドとは異なる2価の状態を形成する傾向を利用してノーベリウムを分離することができる。典型的に使われる溶出条件(固定有機相としてビス-(2-エチルヘキシル)リン酸(HDEHP)、移動水相として0.05M塩酸、または陽イオン交換樹脂カラムからの溶離剤として3M塩酸を使用)では、ノーベリウムはカラムを通過して溶出するが、他の3価のアクチノイドはカラムに残る[28]。ただし、直接「キャッチャー」金箔を使用する場合は、HDEHPを使用するクロマトグラフィー抽出カラムから溶出してノーベリウムを分離する前に陰イオン交換クロマトグラフィーを使用して金を分離する必要があるため、その過程は複雑になる[28]。
出典
[編集]- ^ a b c d e f g h i j k l m n Barber, Robert C.; Greenwood, Norman N.; Hrynkiewicz, Andrzej Z.; Jeannin, Yves P.; Lefort, Marc; Sakai, Mitsuo; Úlehla, Ivan M.; Wapstra, Aaldert Hendrik et al. (1993). “Discovery of the transfermium elements. Part II: Introduction to discovery profiles. Part III: Discovery profiles of the transfermium elements”. Pure and Applied Chemistry 65 (8): 1757. doi:10.1351/pac199365081757. (Note: for Part I see Pure and Applied Chemistry, vol. 63, no. 6, pp. 879–886, 1991)
- ^ a b Silva, pp. 1636–7
- ^ Fields, Peter R.; Friedman, Arnold M.; Milsted, John; Atterling, Hugo; Forsling, Wilhelm; Holm, Lennart W.; Åström, Björn (1 September 1957). “Production of the New Element 102”. Physical Review 107 (5): 1460–1462. Bibcode: 1957PhRv..107.1460F. doi:10.1103/PhysRev.107.1460.
- ^ a b c d e f Emsley, John (2011). Nature's Building Blocks: An A-Z Guide to the Elements. Oxford University Press. pp. 368–9. ISBN 978-0-19-960563-7
- ^ a b Ghiorso, Albert; Seaborg, Glenn T.; Oganessian, Yuri Ts.; Zvara, Ivo; Armbruster, Peter; Hessberger, F. P.; Hofmann, Sigurd; Leino, Matti E. et al. (1993). “Responses on 'Discovery of the transfermium elements' by Lawrence Berkeley Laboratory, California; Joint Institute for Nuclear Research, Dubna; and Gesellschaft fur Schwerionenforschung, Darmstadt followed by reply to responses by the Transfermium Working Group”. Pure and Applied Chemistry 65 (8): 1815–1824. doi:10.1351/pac199365081815.
- ^ a b “Names and symbols of transfermium elements”. Pure and Applied Chemistry 69 (12): 2471–2473. (1997). doi:10.1351/pac199769122471.
- ^ Hoffmann, Darleane C.; Lee, Diana M.; Pershina, Valeria (2006). “Transactinides and the future elements”. In Morss, Lester R.; Edelstein, Norman M.; Fuger, Jean. The Chemistry of the Actinide and Transactinide Elements (3rd ed.). Springer. p. 1660. ISBN 978-1-4020-3555-5
- ^ "Element 114 is Named Flerovium and Element 116 is Named Livermorium" (Press release). IUPAC. 30 May 2012. 2012年6月2日時点のオリジナルよりアーカイブ。
- ^ Haire, Richard G. (2006). “Einsteinium”. In Morss, Lester R.; Edelstein, Norman M.; Fuger, Jean. The Chemistry of the Actinide and Transactinide Elements. 3 (3rd ed.). Dordrecht, the Netherlands: Springer. pp. 1577–1620. doi:10.1007/1-4020-3598-5_12. ISBN 978-1-4020-3555-5
- ^ a b c d e f Silva, pp. 1639
- ^ a b Silva, pp. 1626–8
- ^ Johansson, Börje; Rosengren, Anders (1975). “Generalized phase diagram for the rare-earth elements: Calculations and correlations of bulk properties”. Physical Review B 11 (8): 2836–2857. Bibcode: 1975PhRvB..11.2836J. doi:10.1103/PhysRevB.11.2836.
- ^ Hulet, E. Kenneth (1980). “Chapter 12. Chemistry of the Heaviest Actinides: Fermium, Mendelevium, Nobelium, and Lawrencium”. In Edelstein, Norman M.. Lanthanide and Actinide Chemistry and Spectroscopy. ACS Symposium Series. 131. pp. 239–263. doi:10.1021/bk-1980-0131.ch012. ISBN 978-0-8412-0568-0
- ^ a b Fournier, Jean-Marc (1976). “Bonding and the electronic structure of the actinide metals”. Journal of Physics and Chemistry of Solids 37 (2): 235–244. Bibcode: 1976JPCS...37..235F. doi:10.1016/0022-3697(76)90167-0.
- ^ Haynes, William M., ed (2011). CRC Handbook of Chemistry and Physics (92nd ed.). CRC Press. pp. 4.121–4.123. ISBN 978-1-4398-5511-9
- ^ a b c d e f g h i j k l Silva, pp. 1639–41
- ^ 岩波 理化学辞典 第5版. 岩波書店. (1998)
- ^ グリーンウッド, ノーマン; アーンショウ, アラン (1997). Chemistry of the Elements (英語) (2nd ed.). バターワース=ハイネマン. p. 1278. ISBN 978-0-08-037941-8。
- ^ Balasubramanian, Krishnan (4 December 2001). “Potential energy surfaces of Lawrencium and Nobelium dihydrides (LrH2 and NoH2)…”. Journal of Chemical Physics 116 (9): 3568–75. Bibcode: 2002JChPh.116.3568B. doi:10.1063/1.1446029.
- ^ Toyoshima, A.; Kasamatsu, Y.; Tsukada, K.; Asai, M.; Kitatsuji, Y.; Ishii, Y.; Toume, H.; Nishinaka, I. et al. (8 July 2009). “Oxidation of element 102, nobelium, with flow electrolytic column chromatography on an atom-at-a-time scale”. Journal of the American Chemical Society 131 (26): 9180–1. doi:10.1021/ja9030038. PMID 19514720.
- ^ Martin, William C.; Hagan, Lucy; Reader, Joseph; Sugar, Jack (1974). “Ground Levels and Ionization Potentials for Lanthanide and Actinide Atoms and Ions”. Journal of Physical and Chemical Reference Data 3 (3): 771–9. Bibcode: 1974JPCRD...3..771M. doi:10.1063/1.3253147.
- ^ Lide, David R. (editor), CRC Handbook of Chemistry and Physics, 84th Edition, CRC Press, Boca Raton (FL), 2003, section 10, Atomic, Molecular, and Optical Physics; Ionization Potentials of Atoms and Atomic Ions
- ^ a b c d e f g h Silva, pp. 1637–8
- ^ a b c d e f g “Nucleonica :: Web driven nuclear science”. 2020年6月閲覧。 エラー: 閲覧日は年・月・日のすべてを記入してください。
- ^ a b c d e f g Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik (2003), “The NUBASE evaluation of nuclear and decay properties”, Nuclear Physics A 729: 3–128, Bibcode: 2003NuPhA.729....3A, doi:10.1016/j.nuclphysa.2003.11.001
- ^ Kratz, Jens Volker (5 September 2011). The Impact of Superheavy Elements on the Chemical and Physical Sciences (PDF). 4th International Conference on the Chemistry and Physics of the Transactinide Elements. 2013年8月27日閲覧。
- ^ Nurmia, Matti (2003). “Nobelium”. Chemical and Engineering News 81 (36).
- ^ a b c d Silva, pp. 1638–9
参考文献
[編集]- Silva, Robert J. (2011). “Chapter 13. Fermium, Mendelevium, Nobelium, and Lawrencium”. In Morss, Lester R.; Edelstein, Norman M.; Fuger, Jean. The Chemistry of the Actinide and Transactinide Elements. Netherlands: Springer. pp. 1621–1651. doi:10.1007/978-94-007-0211-0_13. ISBN 978-94-007-0210-3
外部リンク
[編集]- Chart of Nuclides. nndc.bnl.gov
- Los Alamos National Laboratory – Nobelium
- Nobelium at The Periodic Table of Videos (University of Nottingham)


 French
French Deutsch
Deutsch