Penisilin - Vikipedi
 Penisilin çekirdek yapısı, burada "R" değişken gruptur | |
| Klinik verisi | |
|---|---|
| AHFS/Drugs.com | Micromedex Detaylı Tüketici Bilgisi |
| Uygulama yolu | İntravenöz, intramüsküler, ağız yoluyla |
| ATC kodu | |
| Hukuki durum | |
| Hukuki durum |
|
| Farmakokinetik veri | |
| Metabolizma | Karaciğer |
| Eliminasyon yarı ömrü | 0,5 ile 56 saat arasında |
| Boşaltım | Böbrekler |
Penisilinler (P, PCN veya PEN) aslen Penicillium küflerinden, özellikle de P. chrysogenum ve P. rubens'ten elde edilen bir grup β-laktam antibiyotiktir. Klinik kullanımdaki penisilinlerin çoğu P. chrysogenum tarafından derin tank fermantasyonu kullanılarak sentezlenir[1] ve daha sonra saflaştırılır.[2][3] Bir dizi doğal penisilin keşfedilmiştir, ancak sadece iki saflaştırılmış bileşik klinik kullanımdadır: penisilin G (intramüsküler veya intravenöz kullanım) ve penisilin V (ağız yoluyla verilir). Penisilinler, stafilokok ve streptokokların neden olduğu birçok bakteriyel enfeksiyona karşı etkili olan ilk ilaçlar arasındaydı. Günümüzde farklı bakteriyel enfeksiyonlar için hala yaygın olarak kullanılmaktadırlar, ancak birçok bakteri türü yoğun kullanımın ardından direnç geliştirmiştir.
Nüfusun %10'u penisilin alerjisi olduğunu iddia etmektedir, ancak pozitif deri testi sonuçlarının sıklığı kaçınılan her yıl %10 oranında azaldığından, bu hastaların %90'ı sonunda penisilini tolere edebilmektedir. Ayrıca, penisilin alerjisi olanlar genellikle sefalosporinleri (başka bir β-laktam grubu) tolere edebilirler çünkü immünoglobulin E (IgE) çapraz reaktivitesi sadece %3'tür.[4]
Penisilin 1928 yılında İskoç bilim adamı Alexander Fleming tarafından P. rubens'in ham bir özü olarak keşfedilmiştir.[5] Fleming'in öğrencisi Cecil George Paine, 1930 yılında penisilini göz enfeksiyonunu (yenidoğan konjonktiviti) tedavi etmek için başarıyla kullanan ilk kişi oldu. Saflaştırılmış bileşik (penisilin F) 1940 yılında Oxford Üniversitesinde Howard Florey ve Ernst Boris Chain liderliğindeki bir araştırma ekibi tarafından izole edildi. Fleming saflaştırılmış penisilini ilk kez 1942 yılında streptokok menenjitini tedavi etmek için kullandı.[6] 1945 Nobel Fizyoloji veya Tıp Ödülü Chain, Fleming ve Florey tarafından paylaşıldı.
Bazı yarı sentetik penisilinler daha geniş bir bakteri spektrumuna karşı etkilidir: bunlar antistafilokokal penisilinler, aminopenisilinler ve antipsödomonal penisilinleri içerir.
Adlandırma[değiştir | kaynağı değiştir]
"Penisilin" terimi, Penicillium küfünün antimikrobiyal aktiviteye sahip doğal ürünü olarak tanımlanmaktadır.[7] Alexander Fleming tarafından 7 Mart 1929 tarihinde Penicillium rubens'in antibakteriyel özelliğini keşfettiğinde ortaya atılmıştır.[8] Fleming, 1929 yılında British Journal of Experimental Pathology'de yayınlanan makalesinde "oldukça külfetli olan 'Küf suyu süzüntüsü' ifadesinin tekrarından kaçınmak için 'penisilin' adının kullanılacağını" açıklamıştır.[9] Dolayısıyla bu isim, Fleming'in 1945'teki Nobel konferansında tanımladığı şekliyle küfün bilimsel ismine atıfta bulunmaktadır:
Bana sık sık "Penisilin" ismini neden icat ettiğim soruluyor. Ben sadece tamamen ortodoks çizgiyi takip ettim ve penisilin maddesinin Penicillium cinsi bir bitkiden türetildiğini açıklayan bir kelime icat ettim, tıpkı yıllar önce Digitalis bitkisinden türetilen bir madde için "Digitalin" kelimesinin icat edildiği gibi.[10]
Modern kullanımda penisilin terimi, β-laktam çekirdeğine kaynaşmış bir tiyazolidin halkası içeren ve doğal bir ürün olabilen veya olamayan herhangi bir β-laktam antimikrobiyalini ifade etmek için daha geniş bir şekilde kullanılmaktadır.[11] Çoğu doğal ürün gibi penisilin de Penicillium küflerinde aktif bileşenlerin bir karışımı olarak bulunur (gentamisin, aktif bileşenlerin tanımlanmamış bir karışımı olan doğal ürünlere bir başka örnektir).[7] Penicillium'un başlıca aktif bileşenleri aşağıdaki tabloda listelenmiştir:[12][13]
| Kimyasal adı | Birleşik Krallık adlandırması | ABD adlandırması | Penisilin G'ye göre potens[14] |
|---|---|---|---|
| 2-Pentenilpenisilin | Penisilin I | Penisilin F[15] | %70-82 |
| Benzilpenisilin | Penisilin II | Penisilin G[16] | %100 |
| p-Hidroksibenzilpenisilin | Penisilin III | Penisilin X[17] | %130-140 |
| n-Heptilpenisilin | Penisilin IV | Penisilin K[18] | %110-120 |
Penicillium'un diğer minör aktif bileşenleri arasında penisilin O,[19][20] penisilin U1 ve penisilin U6 bulunur. Penisilin A gibi doğal Penicillium'un diğer adlandırılmış bileşenlerinin daha sonra antibiyotik aktiviteye sahip olmadığı ve antibiyotik penisilinlerle kimyasal olarak ilişkili olmadığı bulunmuştur.[7]
Elde edilen penisilinin kesin yapısı, kullanılan Penicillium küfü türüne ve küfü kültürlemek için kullanılan besleyici ortama bağlıdır.[7] Fleming'in orijinal Penicillium rubens türü, esas olarak Fleming'in adıyla anılan penisilin F'yi üretir. Ancak penisilin F kararsızdır, izole edilmesi zordur ve küf tarafından küçük miktarlarda üretilir.[7]
Penicillium chrysogenum'un başlıca ticari suşu (Peoria suşu), kültür ortamı olarak mısır dik likörü kullanıldığında ana bileşen olarak penisilin G üretir.[7] Kültür ortamına fenoksietanol veya fenoksiasetik asit eklendiğinde, küf bunun yerine ana penisilin olarak penisilin V üretir.[7]
6-Aminopenicillanic acid (6-APA), penisilin G'den türetilen bir bileşiktir. 6-APA, penisilin G'nin beta-laktam çekirdeğini içerir, ancak yan zincirleri çıkarılmıştır; 6-APA, diğer penisilinlerin üretimi için yararlı bir öncüdür. 6-APA'dan türetilen birçok yarı sentetik penisilin vardır ve bunlar üç grupta toplanır: antistafilokokal penisilinler, geniş spektrumlu penisilinler ve antipseudomonal penisilinler. Yarı sentetik penisilinlerin hepsi penisilin olarak adlandırılır çünkü hepsi sonuçta penisilin G'den türetilmiştir.
Penisilin birimleri[değiştir | kaynağı değiştir]
- Bir birim penisilin G sodyum 0,600 mikrogram olarak tanımlanır. Bu nedenle, 2 milyon ünite (2 megaünite) penisilin G 1,2 g'dır.[21]
- Bir birim penisilin V potasyum 0,625 mikrogram olarak tanımlanır. Bu nedenle 400.000 ünite penisilin V 250 mg'dır.[22]
Penisilin reçetelemek için birimlerin kullanılması tarihsel bir kazadır ve ABD dışında büyük ölçüde geçerliliğini yitirmiştir. Orijinal penisilin, aktif bileşiklerin iyi tanımlanmamış bir karışımı (amorf sarı bir toz) olduğundan, her bir penisilin partisinin gücü partiden partiye değişmekteydi. Bu nedenle 1 g penisilin reçete etmek imkansızdı çünkü bir partiden alınan 1 g penisilinin aktivitesi başka bir partinin aktivitesinden farklı olacaktı. Üretimden sonra, her bir penisilin partisinin bilinen bir penisilin birimine göre standardize edilmesi gerekiyordu: her bir cam şişe daha sonra gerekli birim sayısı ile dolduruluyordu. 1940'larda 5.000 Oxford birimlik bir şişe standarttı,[23] ancak partiye bağlı olarak 15 mg ila 20 mg penisilin içerebilirdi. Daha sonra, 1.000.000 uluslararası ünitelik bir flakon standart hale geldi ve bu 2,5 g ila 3 g doğal penisilin (penisilin I, II, III ve IV ile doğal safsızlıkların bir karışımı) içerebiliyordu. Saf penisilin G preparatlarının (beyaz kristal toz) ortaya çıkmasıyla, penisilini ünite olarak reçete etmek için çok az neden kalmıştır.
Penisilin "birimi" daha önce üç kez tanımlanmış ve her bir tanım bir öncekine kabaca eşdeğer olarak seçilmiştir.
- Oxford veya Florey birimi (1941). Bu başlangıçta, standart bir Staphylococcus aureus suşunun (Oxford Staphylococcus) büyümesini engelleyecek 50 ml et özütünde çözünmüş minimum penisilin miktarı olarak tanımlanmıştır. Referans standart, Oxford'da tutulan büyük bir saf olmayan penisilin partisiydi.[24] Tahlil daha sonra Florey'in grubu tarafından daha tekrarlanabilir bir "kap tahlili" olarak değiştirildi: bu tahlilde, bir katı agar plakası üzerindeki bir "kap" içine yerleştirilen 339 mikrolitre çözelti Oxford Staphylococcus'un büyümesini 24 milimetrelik bir inhibisyon bölgesi oluşturduğunda, bir penisilin çözeltisinin bir birim/ml penisilin içerdiği tanımlandı.[25]:107[26][27]
- İlk Uluslararası Standart (1944). 8 gramlık tek bir saf kristal penisilin G sodyum partisi Londra'daki Mill Hill'de bulunan Ulusal Tıbbi Araştırma Enstitüsünde (Uluslararası Standart) depolanmıştır. Bir penisilin birimi, Uluslararası Standart'ın 0,6 mikrogramı olarak tanımlanmıştır. Saf olmayan bir "çalışma standardı" da tanımlandı ve dünya çapında dağıtılan çok daha büyük miktarlarda mevcuttu: çalışma standardının bir birimi 2,7 mikrogramdı (safsızlık nedeniyle birim başına miktar çok daha büyüktü). Aynı zamanda, 24 mm'lik bir zon çapı belirtmek yerine, potens hakkında bir okuma sağlamak için zon boyutunun bir referans eğrisine karşı çizildiği kap tahlili rafine edildi.[12][27][28]
- İkinci Uluslararası Standart (1953). Tek bir 30 gramlık saf kristal penisilin G sodyum partisi elde edilmiştir: bu da Mill Hill'de depolanmıştır. Bir penisilin birimi, İkinci Uluslararası Standardın 0,5988 mikrogramı olarak tanımlanmıştır.[29]
Penisilin V için mevcut penisilin V birimine eşdeğer olmayan eski bir birim vardır. Bunun nedeni, ABD FDA'nın yanlışlıkla penisilin V'nin gücünün penisilin G ile aynı mol-mol olduğunu varsaymasıdır. Aslında penisilin V, penisilin G'den daha az güçlüdür ve mevcut penisilin V birimi bu gerçeği yansıtmaktadır.
- İlk uluslararası penisilin V birimi (1959). Bir birim penisilin V, Londra'daki Mill Hill'de tutulan bir referans standardının 0,590 mikrogramı olarak tanımlanmıştır.[30] Bu birim artık kullanılmamaktadır.
Benzer bir standart penisilin K için de oluşturulmuştur.[31]
Türler[değiştir | kaynağı değiştir]
Doğal penisilinler[değiştir | kaynağı değiştir]
Penisilin G (benzilpenisilin) ilk olarak doğada bulunan bir penicillium mantarından üretilmiştir. Günümüzde penisilin G üretimi için kullanılan mantar türü, üretim sürecindeki verimi artırmak için genetik mühendisliği ile oluşturulmuştur. Diğer doğal penisilinlerin (F, K, N, X, O, U1 veya U6) hiçbiri şu anda klinik kullanımda değildir.
Yarı sentetik penisilin[değiştir | kaynağı değiştir]
Penisilin V (fenoksimetilpenisilin), penicillium mantarının genetik olarak değiştirilmiş bir suşunun kültürlendiği ortama öncül fenoksiasetik asit eklenerek üretilir.
6-APA'dan oluşturulan antibiyotikler[değiştir | kaynağı değiştir]
Penisilinlerle ilişkili diğer yarı sentetik antibiyotiklerin üç ana grubu vardır. Bunlar penisilin G'den izole edilen 6-APA öncülüne çeşitli yan zincirler eklenerek sentezlenir. Bunlar antistafilokokal antibiyotikler, geniş spektrumlu antibiyotikler ve antipseudomonal antibiyotiklerdir.
Antistafilokokal antibiyotikler[değiştir | kaynağı değiştir]
- Kloksasilin (ağızdan veya enjeksiyon yoluyla)
- Dikloksasilin (ağızdan veya enjeksiyon yoluyla)
- Flukloksasilin (ağızdan veya enjeksiyon yoluyla)
- Metisilin (sadece enjeksiyon)
- Nafsilin (sadece enjeksiyon)
- Oksasilin (ağızdan veya enjeksiyon yoluyla)
Antistafilokokal antibiyotikler, stafilokokal penisilinaz tarafından parçalanmaya dirençli oldukları için böyle adlandırılırlar. Bu nedenle penisilinaza dirençli olarak da adlandırılırlar.
Geniş spektrumlu antibiyotikler[değiştir | kaynağı değiştir]
Bu antibiyotik grubu, penisilinin uygun olmadığı Escherichia coli ve Salmonella typhi gibi çok çeşitli Gram-negatif bakterilere karşı aktif oldukları için "geniş spektrumlu" olarak adlandırılır. Ancak, bu organizmalarda direnç artık yaygındır.
Var olan birçok ampisilin öncüsü vardır. Bunlar, ampisilini serbest bırakmak için bağırsakta parçalanan inaktif bileşiklerdir. Bu ampisilin ön ilaçlarının hiçbiri şu anda kullanımda değildir:
- Pivampisilin (ampisilinin pivaloyloksimetil esteri)
- Bakampisilin
- Metampisilin (ampisilinin formaldehit esteri)
- Talampisilin
- Hetasilin (asetona konjuge ampisilin)
Episilin, hiçbir zaman yaygın klinik kullanım görmemiş bir aminopenisilindir.
Antipsödomonal antibiyotikler[değiştir | kaynağı değiştir]
Gram-negatif bir tür olan Pseudomonas aeruginosa, birçok antibiyotik sınıfına karşı doğal olarak dirençlidir. 1960'larda ve 1970'lerde Pseudomonas türlerine karşı aktif olan antibiyotikler geliştirmek için birçok çaba sarf edilmiştir. Grup içinde iki kimyasal sınıf vardır: karboksipenisilinler ve üreidopenisilinler. Hepsi enjeksiyon yoluyla verilir: hiçbiri ağız yoluyla verilemez.
Karboksipenisilinler[değiştir | kaynağı değiştir]
Üreidopenisilinler[değiştir | kaynağı değiştir]
β-laktamaz inhibitörleri[değiştir | kaynağı değiştir]
Tıbbi kullanım[değiştir | kaynağı değiştir]
"Penisilin" terimi tek başına kullanıldığında, penisilin G veya penisilin V olmak üzere iki kimyasal bileşikten birini ifade edebilir.
| Yaygın ad | Kimyasal ad | Uygulama yöntemi |
|---|---|---|
| Penisilin V | fenoksimetilpenisilin | oral |
| Penisilin G | benzilpenisilin | intravenöz, intramüsküler |
Penisilin G[değiştir | kaynağı değiştir]
Penisilin G mide asidi tarafından yok edilir, bu nedenle ağızdan alınamaz, ancak 2,4 g'a kadar yüksek dozlar verilebilir (penisilin V'den çok daha yüksek). İntravenöz veya intramüsküler enjeksiyon yoluyla verilir. Çözünmeyen bir tuz olarak formüle edilebilir ve şu anda kullanımda olan bu tür iki formülasyon vardır: prokain penisilin ve benzatin benzilpenisilin. Kandaki yüksek konsantrasyonun korunması gerektiğinde, penisilin G nispeten sık aralıklarla uygulanmalıdır, çünkü böbrek tarafından kan dolaşımından oldukça hızlı bir şekilde elimine edilir.
Penisilin G, duyarlı stafilokok ve streptokok suşlarının neden olduğu septisemi, empiyem, pnömoni, perikardit, endokardit ve menenjit tedavisinde kullanılmak üzere ruhsatlandırılmıştır. Ayrıca şarbon, aktinomikoz, servikofasiyal hastalıklar, torasik ve abdominal hastalıklar, klostridiyal enfeksiyonlar, botulizm, gazlı kangren (endike olduğu şekilde debridman ve/veya cerrahi ile birlikte), tetanos (insan tetanoz immün globülinine ek tedavi olarak) tedavisinde ruhsatlıdır, difteri (antitoksine ek tedavi olarak ve taşıyıcı durumun önlenmesi için), erizipelotriks endokarditi, fusospiroketoz (orofarenks, alt solunum yolu ve genital bölgenin ciddi enfeksiyonları), Listeria enfeksiyonları, menenjit, endokardit, bakteriyemi ve menenjit dahil Pasteurella enfeksiyonları, Haverhill ateşi; fare ısırığı ateşi ve yaygın gonokok enfeksiyonları, penisiline duyarlı organizmaların neden olduğu meningokok menenjiti ve/veya septisemi ve sifiliz.[32]
Penisilin V[değiştir | kaynağı değiştir]
Penisilin V mide asidine nispeten dirençli olduğu için ağız yoluyla alınabilir. Zayıf emilim nedeniyle 500 mg'dan yüksek dozlar tam olarak etkili değildir. Penisilin G ile aynı bakteriyel enfeksiyonlar için kullanılır ve penisilinin en yaygın kullanılan formudur.[33] Bununla birlikte, endokardit gibi yüksek kan penisilin seviyelerinin gerekli olduğu hastalıklarda kullanılmaz.
Bakteriyel duyarlılık[değiştir | kaynağı değiştir]
Penisilin direnci artık çok yaygın olduğundan, diğer antibiyotikler artık tedavilerde tercih edilen seçeneklerdir. Örneğin, penisilin eskiden Neisseria gonorrhoeae ve Neisseria meningitidis enfeksiyonları için ilk basamak tedaviydi, ancak artık bu enfeksiyonların tedavisi için önerilmemektedir. Staphylococcus aureus'ta penisilin direnci artık çok yaygındır, bu da enfekte eden türün duyarlı olduğu bilinmedikçe penisilinin S. aureus enfeksiyonunun neden olduğu enfeksiyonları tedavi etmek için kullanılmaması gerektiği anlamına gelir.
| Bakteri | Duyarlı (S) | Orta düzey (I) | Dayanıklı (R) |
|---|---|---|---|
| Staphylococcus aureus | ≤0,12 mcg/ml | - | ≥0,25 mcg/ml |
| Streptococcus pneumoniae menenjiti | ≤0,06 mcg/ml | - | ≥0,12 mcg/ml |
| Streptococcus pneumoniae (menenjit değil) | ≤2 mcg/ml | ≥8 mcg/ml | |
| Streptococcus Viridans grubu | 0,12 mcg/ml | 0,25–2 mcg/ml | 4 mcg/ml |
| Listeria monocytogenes | ≤2 mcg/ml | - | - |
| Bacillus anthracis | ≤0,12 mcg/ml | - | ≥0,25 mcg/ml |
Yan etkiler[değiştir | kaynağı değiştir]
Penisilinlerin kullanımıyla ilişkili yaygın (insanların ≥ %1'i) advers ilaç reaksiyonları arasında ishal, aşırı duyarlılık, bulantı, döküntü, nörotoksisite, ürtiker ve süperenfeksiyon (kandidiyaz dahil) yer almaktadır. Seyrek görülen yan etkiler (insanların %0,1-1'i) ateş, kusma, eritem, dermatit, anjiyoödem, nöbetler (özellikle epilepsisi olan kişilerde) ve psödomembranöz kolittir.[34] Penisilin ayrıca bazı kişilerde serum hastalığına veya serum hastalığı benzeri bir reaksiyona neden olabilir. Serum hastalığı, penisilin dahil ilaçlara maruz kaldıktan bir ila üç hafta sonra ortaya çıkan tip III aşırı duyarlılık reaksiyonudur. Gerçek bir ilaç alerjisi değildir, çünkü alerjiler tip I aşırı duyarlılık reaksiyonlarıdır, ancak rahatsız edici maddeye tekrar tekrar maruz kalmak anafilaktik reaksiyona neden olabilir.[35][36] Alerji, insanların %1-10'unda görülür ve maruziyet sonrası deri döküntüsü şeklinde ortaya çıkar. Hastaların yaklaşık %0,01'inde IgE aracılı anafilaksi meydana gelecektir.[34][37]
Enjeksiyon bölgesinde ağrı ve iltihaplanma parenteral olarak uygulanan benzatin benzilpenisilin, benzilpenisilin ve daha az oranda prokain benzilpenisilin için de yaygındır. Bu durum livedoid dermatit veya Nicolau sendromu olarak bilinir.[38][39]
Yapı[değiştir | kaynağı değiştir]
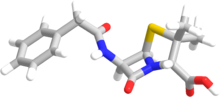
"Penam" terimi, penisilinlerin bir üyesinin ortak çekirdek iskeletini tanımlamak için kullanılır. Bu çekirdek R-C9H11N2O4S moleküler formülüne sahiptir, burada R penisilinleri birbirinden ayıran değişken yan zincirdir. Penam çekirdeğinin molar kütlesi 243 g/mol olup, daha büyük penisilinler 450'ye yakın molar kütleye sahiptir - örneğin kloksasilinin molar kütlesi 436 g/mol'dür. 6-APA (C8H12N2O3S) penisilinlerin temel yapısını oluşturur. L-sistein ve D-valinin kondensasyonu ile oluşan kapalı bir dipeptitten oluşur. Bu, β-laktam ve tiyazolidinik halkaların oluşumuyla sonuçlanır.[40]
Penisilinlerin temel yapısal özelliği dört üyeli β-laktam halkasıdır; bu yapısal parça penisilinin antibakteriyel aktivitesi için gereklidir. β-laktam halkasının kendisi beş üyeli bir tiyazolidin halkasına kaynaşmıştır. Bu iki halkanın kaynaşması β-laktam halkasının monosiklik β-laktamlardan daha reaktif olmasına neden olur çünkü iki kaynaşmış halka β-laktam amid bağını bozar ve bu nedenle normalde bu kimyasal bağlarda bulunan rezonans stabilizasyonunu ortadan kaldırır.[41] β-laktam halkasına bir açil yan zinciri bağlanır.[42]
Çeşitli β-laktam antibiyotikler, sentez sırasında 6-APA yapısından kimyasal modifikasyonun ardından, özellikle açil yan zincirinde kimyasal sübstitüsyonlar yapılarak üretilmiştir. Örneğin, kimyasal olarak değiştirilmiş ilk penisilin olan metisilin, penisilin G'den 6-APA benzen halkasının 2' ve 6' pozisyonlarında metoksi grupları ile yer değiştirmiştir.[40] Bu farklılık, metisilini, birçok bakterinin penisilinlere doğal olarak duyarlı olmadığı bir enzim olan β-laktamaz aktivitesine karşı dirençli hale getirir.[43]
Farmakoloji[değiştir | kaynağı değiştir]
Bakteri içine giriş[değiştir | kaynağı değiştir]
Penisilin, Gram pozitif türler söz konusu olduğunda bakteri hücrelerine kolayca girebilir. Bunun nedeni Gram pozitif bakterilerin bir dış hücre zarına sahip olmaması ve sadece kalın bir hücre duvarı ile çevrili olmasıdır.[44] Penisilin molekülleri hücre duvarındaki glikoproteinlerin boşluklarından geçebilecek kadar küçüktür. Bu nedenle Gram pozitif bakteriler penisiline karşı çok hassastır (ilk olarak 1928'de penisilinin keşfiyle kanıtlandığı gibi[45]).[46]
Penisilin ya da başka herhangi bir molekül Gram negatif bakterilere farklı bir yolla girer. Bakterilerin hücre duvarları daha incedir ancak dış yüzeyleri dış zar adı verilen ek bir hücre zarı ile kaplıdır. Dış zar, penisilin gibi suda çözünen (hidrofilik) moleküllerin geçişini engelleyen bir lipid tabakasıdır (lipopolisakkarit zinciri). Bu nedenle, herhangi bir toksik maddeye karşı ilk savunma hattı görevi görür ve Gram pozitif türlere kıyasla antibiyotiklere karşı göreceli direncin nedeni budur.[47] Ancak penisilin, yağ molekülleri arasında dağılmış olan ve bakterilere besin ve antibiyotik taşıyabilen porinler (dış zar proteinleri) adı verilen sulu kanallardan difüzyon yoluyla Gram negatif türlere hala girebilir.[48] Porinler çoğu penisilinin difüzyonuna izin verecek kadar büyüktür, ancak içlerinden difüzyon oranı ilaç moleküllerinin spesifik boyutuna göre belirlenir. Örneğin, penisilin G büyüktür ve porinlerden yavaş geçer; daha küçük olan ampisilin ve amoksisilin ise çok daha hızlı yayılır.[49] Buna karşılık, büyük vankomisin porinlerden geçemez ve bu nedenle Gram-negatif bakteriler için etkisizdir.[50] Porinlerin boyutu ve sayısı farklı bakterilerde farklıdır. Bu iki faktörün (penisilin ve porin) bir sonucu olarak Gram-negatif bakteriler spesifik penisiline karşı duyarsız olabilir ya da değişen derecelerde duyarlılık gösterebilir.[51]
Etki mekanizması[değiştir | kaynağı değiştir]


Penisilin, bakteriyel hücre duvarının yapısal bileşeni olan peptidoglikanların sentezinin tamamlanmasını engelleyerek bakterileri öldürür. Özellikle hücre duvarı biyosentezindeki son adım sırasında peptidoglikanların çapraz bağlanması için gerekli olan enzimlerin aktivitesini inhibe eder. Bunu, penisilin moleküllerinde bulunan bir yapı olan β-laktam halkası ile penisilin bağlayıcı proteinlere bağlanarak yapar.[53][54] Bu, daha az çapraz bağ nedeniyle hücre duvarının zayıflamasına neden olur ve doğru ozmotik gradyanı koruyamadığı için suyun kontrolsüz bir şekilde hücre içine akması anlamına gelir. Bu da hücrenin parçalanması ve ölümüyle sonuçlanır.
Bakteriler peptidoglikan hücre duvarlarını sürekli olarak yeniden şekillendirir, büyüdükçe ve bölündükçe eş zamanlı olarak hücre duvarının bölümlerini inşa eder ve yıkarlar. Peptidoglikan biyosentezinin son aşamalarında, dördüncü ve beşinci amino asitlerin her ikisinin de D-alanil-D-alanin olduğu üridin difosfat-N-asetilmuramik asit pentapeptit (UDP-MurNAc) oluşur. D-alanin transferi DD-transpeptidaz enzimi (penisilin bağlayıcı proteinler bu türdendir) tarafından yapılır (katalize edilir).[49] Bakteri hücre duvarının yapısal bütünlüğü UDP-MurNAc ve N-asetil glukozaminin çapraz bağlanmasına bağlıdır.[55] Penisilin ve diğer β-laktam antibiyotikler, konformasyonel benzerlikler nedeniyle UDP-MurNAc'da D-alanin-D-alanin (dipeptit) analoğu olarak hareket eder. DD-transpeptidaz daha sonra UDP-MurNAc yerine penisilinin dört üyeli β-laktam halkasını bağlar.[49] Sonuç olarak, DD-transpeptidaz inaktive olur, UDP-MurNAc ve N-asetil glukozamin arasındaki çapraz bağların oluşumu engellenir, böylece hücre duvarı üretimi ve yıkımı arasında bir dengesizlik gelişerek hücrenin hızla ölmesine neden olur.[56]
Peptidoglikan çapraz bağları hidrolize eden enzimler çalışmaya devam ederken, bu tür çapraz bağları oluşturanlar çalışmaz. Bu durum bakterinin hücre duvarını zayıflatır ve ozmotik basınç giderek dengelenemez hale gelir ve sonuçta hücre ölümüne (sitoliz) neden olur. Buna ek olarak, peptidoglikan öncüllerinin birikmesi, hücre duvarının peptidoglikanlarını daha da sindiren bakteriyel hücre duvarı hidrolazlarının ve otolizinlerin aktivasyonunu tetikler. Penisilinlerin küçük boyutları, hücre duvarının tüm derinliğine nüfuz etmelerini sağlayarak etkilerini arttırır. Bu durum, her ikisi de penisilinlerden çok daha büyük olan glikopeptit antibiyotikler vankomisin ve teikoplanin ile tezat oluşturmaktadır.[57]
Gram-pozitif bakteriler hücre duvarlarını kaybettiklerinde protoplast olarak adlandırılırlar. Gram negatif bakteriler hücre duvarlarını tamamen kaybetmezler ve penisilin ile tedavi edildikten sonra sferoplast olarak adlandırılırlar.[52]
Penisilin, aminoglikozitlerle sinerjik bir etki gösterir, çünkü peptidoglikan sentezinin inhibisyonu, aminoglikozidlerin bakteri hücre duvarına daha kolay nüfuz etmesine ve hücre içindeki bakteriyel protein sentezini bozmasına izin verir. Bu da duyarlı organizmalar için MBK'nin düşmesine neden olur.[58]
Penisilinler, diğer β-laktam antibiyotikler gibi, sadece siyanobakteriler de dahil olmak üzere bakterilerin bölünmesini değil, aynı zamanda glokofitlerin fotosentetik organelleri olan siyanellerin bölünmesini ve briyofitlerin kloroplastlarının bölünmesini de engeller. Buna karşılık, oldukça gelişmiş damarlı bitkilerin plastitleri üzerinde hiçbir etkileri yoktur. Bu da kara bitkilerinde plastid bölünmesinin evrimine ilişkin endosimbiyotik teoriyi desteklemektedir.[59]
Bazı bakteriler β-laktam halkasını parçalayan ve β-laktamaz adı verilen enzimler üreterek bakterileri penisiline dirençli hale getirir. Bu nedenle, bazı penisilinler antibiyotiğe dirençli bakterilere karşı veya bağışıklık sistemi baskılanmış hastalarda kullanılmak üzere modifiye edilir veya diğer ilaçlarla birlikte verilir. Penisilinin yanında β-laktamaz inhibitörleri olan klavulanik asit veya tazobaktam kullanımı β-laktamaz üreten bakterilere karşı penisilin aktivitesi sağlar. β-Laktamaz inhibitörleri β-laktamaza geri dönüşümsüz olarak bağlanarak antibiyotik molekülü üzerindeki beta-laktam halkalarını parçalamasını engeller. Alternatif olarak flukloksasilin, beta-laktam halkasını β-laktamazdan koruyan bir açil yan zinciri nedeniyle β-laktamaz üreten bakterilere karşı aktiviteye sahip modifiye bir penisilindir.[37]
Farmakokinetik[değiştir | kaynağı değiştir]
Penisilinin plazmada proteine bağlanma oranı düşüktür. Penisilinin biyoyararlanımı türüne bağlıdır: penisilin G'nin biyoyararlanımı %30'un altında düşükken, penisilin V'nin biyoyararlanımı %60 ila 70 arasında daha yüksektir.[60]
Penisilinin kısa bir yarılanma ömrü vardır ve böbrekler yoluyla atılır.[60] Bu, kanda yeterli penisilin seviyesini korumak için günde en az dört kez dozlanması gerektiği anlamına gelir. Bu nedenle penisilin kullanımına ilişkin ilk el kitaplarında penisilinin üç saatte bir gibi sık aralıklarla enjekte edilmesi önerilmiş ve penisilin dozajı, tıpası dışarıda olan bir banyoyu doldurmaya çalışmaya benzetilmiştir.[7] Çok daha büyük dozlarda penisilin ucuz ve kolay bir şekilde temin edilebildiğinden bu artık gerekli değildir; ancak bazı otoriteler bu nedenle sürekli penisilin infüzyonlarının kullanılmasını önermektedir.[61]
Direnç[değiştir | kaynağı değiştir]
Alexander Fleming 1928 yılında ham penisilini keşfettiğinde yaptığı önemli bir gözlem, birçok bakterinin penisilinden etkilenmediğiydi.[45] Bu olgu, Ernst Chain ve Edward Abraham tarafından penisilini tam olarak tanımlamaya çalışırken fark edildi. 1940 yılında, Escherichia coli gibi duyarlı olmayan bakterilerin penisilin moleküllerini parçalayabilen spesifik enzimler ürettiğini ve böylece antibiyotiğe dirençli hale geldiklerini keşfettiler. Bu enzime penisilinaz adını verdiler.[62] Penisilinaz artık β-laktamaz adı verilen enzimlerin bir üyesi olarak sınıflandırılmaktadır. Bu β-laktamazlar diğer birçok bakteride doğal olarak bulunur ve birçok bakteri sürekli antibiyotiğe maruz kaldığında bunları üretir. Çoğu bakteride direnç üç farklı mekanizma yoluyla olabilir - bakterilerde geçirgenliğin azalması, penisilin bağlayıcı proteinlerin (PBP'ler) bağlanma afinitesinin azalması veya β-laktamaz ekspresyonu yoluyla antibiyotiğin yok edilmesi.[63] Bunlardan herhangi birini kullanan bakteriler genellikle farklı antibiyotiklere karşı direnç geliştirir, bu olguya çoklu ilaç direnci denir.
Direnç mekanizmasının gerçek süreci çok karmaşık olabilir. Bakterilerde geçirgenliğin azalması durumunda, mekanizmalar Gram pozitif ve Gram negatif bakteriler arasında farklıdır. Gram pozitif bakterilerde penisilinin bloke olması hücre duvarındaki değişikliklerden kaynaklanmaktadır. Örneğin, S. aureus'ta vankomisine karşı direnç, hücre duvarını etkili penisilin girişini önleyen çok daha kalın hale getiren ek peptidoglikan sentezinden kaynaklanmaktadır.[46] Gram negatif bakterilerde direnç, porinlerin yapısı ve sayısındaki mutasyonel varyasyonlardan kaynaklanmaktadır.[51] Pseudomonas aeruginosa gibi bakterilerde porin sayısı azalmıştır; Enterobacter türleri, Escherichia coli ve Klebsiella pneumoniae gibi bakterilerde ise penisilini taşıyamayan spesifik olmayan porinler (OmpC ve OmpF grupları gibi) gibi modifiye porinler vardır.[64]
PBP değişikliklerine bağlı direnç oldukça çeşitlidir. Yaygın bir vaka, PBP geninde mutasyon olan Streptococcus pneumoniae'de bulunur ve mutant PBP'lerin penisilinlere bağlanma afinitesi azalmıştır.[65] S. pneumoniae'de altı mutant PBP vardır ve bunlardan PBP1a, PBP2b, PBP2x ve bazen PBP2a azalmış bağlanma afinitesinden sorumludur.[66] S. aureus, penisilinler için düşük bağlanma afinitesine sahip farklı bir PBP olan PBD2'yi üreten gizli bir geni aktive edebilir.[67] S. aureus'un metisiline dirençli S. aureus (MRSA) olarak adlandırılan ve sadece penisilin ve diğer β-laktamlara değil aynı zamanda çoğu antibiyotiğe dirençli olan farklı bir türü bulunmaktadır. Bu bakteri türü 1959 yılında metisilinin kullanılmaya başlanmasından sonra gelişmiştir.[43] MRSA'da PBP genlerindeki (mec sistemi) mutasyonlar, dört normal PBP üretirken PBP2a (PBP2' olarak da adlandırılır)[68] adı verilen bir varyant protein üretir. PBP2a penisilin için zayıf bağlanma afinitesine sahiptir ve ayrıca tam peptidoglikan sentezi için gerekli olan glikoziltransferaz aktivitesinden yoksundur (bu dört normal PBP tarafından gerçekleştirilir).[66] Helicobacter cinaedi'de, farklı genlerde PBP varyantları oluşturan çok sayıda mutasyon vardır.[69]
β-laktamazlar tarafından gerçekleştirilen enzimatik yıkım, penisilin direncinin en önemli mekanizmasıdır[70] ve "[penisilinlerin] kullanımına yönelik en büyük tehdit" olarak tanımlanmaktadır.[71] Penisilin direncinin ilk keşfedilen mekanizmasıdır. Penisilinin saflaştırılması ve biyolojik aktivite testlerinin 1940 yılında yapıldığı deneyler sırasında E. coli'nin dirençsiz olduğu görülmüştür.[72] Bunun nedeni, E. coli'de penisilini kolayca parçalayan bir penisilinaz enziminin (dolayısıyla bilinen ilk β-laktamaz) üretilmesi olarak keşfedildi.[62] Her biri benzersiz amino asit dizisine ve dolayısıyla enzimatik aktiviteye sahip 2.000'den fazla β-laktamaz türü vardır.[71] Hepsi β-laktam halkalarını hidrolize edebilir ancak tam hedef bölgeleri farklıdır.[73] Gram pozitif bakterilerde bakteri yüzeyinde büyük miktarlarda salgılanırken, Gram negatif türlerde daha az salgılanırlar. Bu nedenle, karışık bir bakteriyel enfeksiyonda, Gram-pozitif bakteriler penisiline duyarlı Gram-negatif hücreleri koruyabilir.[49]
P. aeruginosa'da biyofilm aracılı direncin ve çoklu ilaca toleranslı persister hücrelerin oluşumunun söz konusu olabildiği alışılmadık mekanizmalar mevcuttur.[74]
Tarihçe[değiştir | kaynağı değiştir]
Keşif[değiştir | kaynağı değiştir]

19. yüzyılın sonlarından itibaren Penicillium küfünün antibakteriyel özelliklerine dair raporlar vardı, ancak bilim insanları bu etkiye hangi sürecin neden olduğunu anlayamıyordu.[75] Penicillium rubens'in antibakteriyel özelliklere sahip olduğunu gösteren ilk kişi Londra'daki St Mary's Hastanesi'nde (şu anda Imperial College'ın bir parçası) çalışan İskoç doktor Alexander Fleming oldu.[76] 3 Eylül 1928'de bir bakteri kültürüne (Staphylococcus aureus) mantar bulaşmasının bakteriyi öldürdüğünü tesadüfen gözlemledi. Bu gözlemini 28 Eylül 1928'de yeni bir deneyle doğruladı.[77][78] Deneyini 1929 yılında yayınladı ve antibakteriyel maddeye (mantar özü) penisilin adını verdi.[45]
C. J. La Touche mantarı Penicillium rubrum olarak tanımladı (daha sonra Charles Thom tarafından P. notatum ve P. chrysogenum olarak yeniden sınıflandırıldı, ancak daha sonra P. rubens olarak düzeltildi).[79] Fleming, günün diğer antiseptiklerine kıyasla yüksek etki gücü ve minimal toksisitesi nedeniyle penisilinin yararlı bir antiseptik olacağına dair ilk iyimserliğini dile getirdi ve Bacillus influenzae'nin (şimdiki adı Haemophilus influenzae) izolasyonundaki laboratuvar değerine dikkat çekti.[80][81]
Fleming, keşfinin önemli olduğu konusunda kimseyi ikna edemedi.[80] Bunun nedeni büyük ölçüde penisilinin izole edilmesinin çok zor olması ve bir ilaç olarak geliştirilmesinin imkansız görünmesiydi. Fleming, diğer bilim insanlarının onun çalışmalarına ilgi duymasını sağlamakta daha başarılı olsaydı penisilinin muhtemelen yıllar önce geliştirilebileceği tahmin edilmektedir.[80]
Çalışmalarının önemi, 19 Kasım 1999'da Londra'daki Alexander Fleming Laboratuvar Müzesine Uluslararası Tarihi Kimya Simgesi yerleştirilmesiyle tanınmıştır.[82]
Geliştirme ve tıbbi uygulama[değiştir | kaynağı değiştir]

1930 yılında Sheffield Kraliyet Revirinde patolog olan Cecil George Paine, 25 Kasım 1930'da bebeklerde gonokok enfeksiyonu olan oftalmia neonatorumu penisilin (mantar özü) ile başarılı bir şekilde tedavi etti.[83][84][85]
1940 yılında Avustralyalı bilim adamı Howard Florey (daha sonra Baron Florey) ve Oxford Üniversitesi Sir William Dunn Patoloji Okulundaki bir grup araştırmacı (Ernst Chain, Edward Abraham, Arthur Duncan Gardner, Norman Heatley, Margaret Jennings, Jean Orr-Ewing ve Arthur Gordon Sanders) mantar kültürü suyundan hem in vitro hem de in vivo bakterisidal etki gösteren konsantre penisilin yapımında ilerleme kaydetti.[86][87] 1941'de Albert Alexander adlı ciddi bir yüz enfeksiyonuna sahip bir polis memurunu tedavi ettiler; durumu düzeldi, ancak daha sonra penisilin stokları tükendi ve öldü. Daha sonra birkaç hasta daha başarıyla tedavi edildi.[88] Aralık 1942'de Boston'daki Cocoanut Grove yangınından kurtulanlar, penisilin ile başarılı bir şekilde tedavi edilen ilk yanık hastaları oldu.[89]
Saf penisilinin ilk başarılı kullanımı 1942'de Fleming'in Harry Lambert'i aksi takdirde ölümcül olabilecek bir sinir sistemi enfeksiyonundan (streptokok menenjiti) iyileştirmesiyle oldu. O zamana kadar Oxford ekibi sadece küçük bir miktar üretebiliyordu. Florey eldeki tek örneği kendi isteğiyle Fleming'e verdi. Lambert tedavinin hemen ertesi gününden itibaren iyileşme gösterdi ve bir hafta içinde tamamen iyileşti.[90][91] Fleming klinik deneyini 1943 yılında The Lancet dergisinde yayınladı.[6] Bu tıbbi buluşun ardından İngiliz Savaş Kabinesi 5 Nisan 1943'te "Penisilin Komitesi"ni kurarak seri üretim projelerini başlattı.[92][93]
Seri üretim[değiştir | kaynağı değiştir]
Tıbbi uygulama ortaya çıktıkça, Oxford ekibi laboratuvarlarında kullanılabilir miktarlarda üretim yapmanın imkansız olduğunu gördü.[88] İngiliz hükümetini ikna edemeyen Florey ve Heatley, büyük ölçekli üretim için ABD hükümetinin ilgisini çekmek amacıyla küf örnekleriyle birlikte Haziran 1941'de ABD'ye gitti.[94] Büyük ölçekli fermantasyonlar için tesislerin kurulduğu Illinois, Peoria'daki USDA Kuzey Bölgesel Araştırma Laboratuvarı'na (NRRL, şimdi Ulusal Tarımsal Kullanım Araştırmaları Merkezi) başvurdular.[95] Küfün kitlesel kültürü ve daha iyi küflerin araştırılması hemen ardından geldi.[94]
14 Mart 1942'de ilk hasta streptokok sepsisi nedeniyle Merck & Co. tarafından üretilen ABD yapımı penisilin ile tedavi edildi.[96] O dönemde üretilen toplam stokun yarısı Anne Miller adlı bu tek hastada kullanıldı.[97] Haziran 1942'ye gelindiğinde, on hastayı tedavi etmeye yetecek kadar ABD penisilini mevcuttu.[98] Temmuz 1943'te Savaş Üretim Kurulu, Avrupa'da savaşan Müttefik birliklerine penisilin stoklarının toplu dağıtımı için bir plan hazırladı.[99] NRRL'de mısır abartılı likör üzerinde yapılan fermantasyon araştırmasının sonuçları, ABD'nin 1944 baharında Normandiya'nın işgali için zamanında 2,3 milyon doz üretmesini sağladı. 1943'te dünya çapında yapılan bir araştırmanın ardından, Peoria, Illinois'deki bir markette bulunan küflü bir kavunun, mısır abartılı likör prosesi kullanılarak üretim için en iyi küf türünü içerdiği tespit edildi.[100] Pfizer bilim adamı Jasper H. Kane, büyük miktarlarda farmasötik sınıf penisilin üretmek için derin tank fermantasyon yönteminin kullanılmasını önerdi.[101][25]:109 Kimya mühendisi Margaret Hutchinson Rousseau tarafından derin tank fermantasyon tesisinin geliştirilmesiyle büyük ölçekli üretim sağlandı.[102] Savaşın ve Savaş Üretim Kurulunun doğrudan bir sonucu olarak, Haziran 1945 itibarıyla yılda 646 milyar üniteden fazla üretim yapılıyordu.[99]
G. Raymond Rettew, mantar yumurtası konusundaki bilgisini Sharples Krem Ayırıcı'nın işleviyle birleştirdiği ticari miktarlarda penisilin üretme teknikleriyle Amerikan savaş çabalarına önemli bir katkıda bulundu.[103] 1943 yılına gelindiğinde Rettew'in laboratuarı dünyadaki penisilinin çoğunu üretiyordu. İkinci Dünya Savaşı sırasında penisilin, Müttefik kuvvetler arasında enfekte yaraların neden olduğu ölüm ve ampütasyon sayısında büyük bir fark yarattı ve tahmini olarak hayatların %12-%15'ini kurtardı.[104] Bununla birlikte, büyük miktarlarda penisilin üretmenin zorluğu ve ilacın böbreklerden hızla atılması nedeniyle sık sık doz verilmesi gerektiğinden bulunabilirliği ciddi şekilde sınırlıydı. Penisilinin seri üretim yöntemleri 1945 yılında Andrew Jackson Moyer tarafından patentlendi.[105][106][107] Florey, Sir Henry Dale tarafından bunun etik olmayacağı konusunda uyarıldığı için penisilinin patentini almamıştı.[88]
Penisilin aktif olarak atılır ve bir penisilin dozunun yaklaşık %80'i uygulamadan sonraki üç ila dört saat içinde vücuttan temizlenir. Gerçekten de penisilinin ilk dönemlerinde ilaç o kadar az bulunuyordu ve o kadar değerliydi ki idrardaki penisilinin izole edilip yeniden kullanılabilmesi için tedavi edilen hastaların idrarının toplanması yaygın hale gelmişti.[108] Bu tatmin edici bir çözüm değildi, bu nedenle araştırmacılar penisilin atılımını yavaşlatmanın bir yolunu aradılar. Atılımdan sorumlu organik asit taşıyıcısı için penisilin ile rekabet edebilecek bir molekül bulmayı umuyorlardı, öyle ki taşıyıcı tercihen rakip molekülü atacak ve penisilin tutulacaktı. Ürikosürik ajan probenesidin uygun olduğu kanıtlanmıştır. Probenesid ve penisilin birlikte uygulandığında, probenesid penisilinin atılımını rekabetçi bir şekilde inhibe ederek penisilinin konsantrasyonunu artırır ve aktivitesini uzatır. Sonunda, seri üretim tekniklerinin ve yarı sentetik penisilinlerin ortaya çıkması tedarik sorunlarını çözdü, bu nedenle probenesidin bu kullanımı azaldı.[108] Bununla birlikte probenesid, özellikle yüksek konsantrasyonlarda penisilin gerektiren bazı enfeksiyonlar için hala yararlıdır.[109]
II. Dünya Savaşı'ndan sonra ilacı sivil kullanıma sunan ilk ülke Avustralya olmuştur. ABD'de penisilin 15 Mart 1945 tarihinde halkın kullanımına sunulmuştur.[110]
Fleming, Florey ve Chain penisilini geliştirdikleri için 1945 Nobel Fizyoloji veya Tıp Ödülü'nü paylaşmışlardır.
- 1943'te penisilin hazırlayan bir teknisyen
- Penisilin 1944 yılında seri üretime geçmişti
- İkinci Dünya Savaşı'nda penisilin kullanımını öven bir poster
Yapı belirleme ve toplam sentez[değiştir | kaynağı değiştir]

Penisilinin kimyasal yapısı ilk olarak 1942 yılında Edward Abraham tarafından ortaya atılmış[86] ve daha sonra 1945 yılında yine Oxford'da çalışan Dorothy Crowfoot Hodgkin tarafından X ışını kristalografisi kullanılarak doğrulanmıştır.[111] Daha sonra 1964 yılında bu ve diğer yapı belirleme çalışmaları için Nobel Kimya Ödülü'nü almıştır.
Massachusetts Teknoloji Enstitüsünden (MIT) kimyager John C. Sheehan, penisilinin ilk kimyasal sentezini 1957 yılında tamamladı.[112][113][114] Sheehan, penisilin sentezi çalışmalarına 1948 yılında başlamış ve bu araştırmalar sırasında peptitlerin sentezi için yeni yöntemler ve yeni koruyucu gruplar (belirli fonksiyonel grupların reaktivitesini maskeleyen gruplar) geliştirmişti.[114][115] Sheehan tarafından geliştirilen ilk sentez penisilinlerin seri üretimi için uygun olmasa da Sheehan'ın sentezindeki ara bileşiklerden biri penisilinin çekirdeği olan 6-aminopenicillanic acid (6-APA) idi.[112][113][114][116]
6-APA, 1957 yılında Surrey'deki Beecham Araştırma Laboratuvarlarındaki (daha sonra Beecham Group) araştırmacılar tarafından keşfedilmiştir (1959'da yayınlanmıştır).[117] Penisilinin 6-APA 'çekirdeğine' farklı grupların eklenmesi, daha çok yönlü ve daha iyi aktiviteye sahip yeni penisilin formlarının oluşturulmasını sağladı.[118]
Penisilinden gelen gelişmeler[değiştir | kaynağı değiştir]
Penisilinlerin dar tedavi edilebilir hastalık yelpazesi veya "aktivite spektrumu", oral olarak aktif fenoksimetilpenisilinin zayıf aktivitesi ile birlikte, daha geniş bir enfeksiyon yelpazesini tedavi edebilecek penisilin türevlerinin araştırılmasına yol açmıştır. Penisilinin çekirdeği olan 6-APA'nın izolasyonu, benzilpenisilin üzerinde çeşitli iyileştirmelerle (biyoyararlanım, spektrum, stabilite, tolerans) yarı sentetik penisilinlerin hazırlanmasına izin verdi.
İlk büyük gelişme 1961 yılında ampisilin olmuştur. Orijinal penisilinlerin her ikisinden de daha geniş bir aktivite spektrumu sunuyordu. Daha sonraki gelişmeler flukloksasilin, dikloksasilin ve metisilin dahil olmak üzere β-laktamaza dirençli penisilinler ortaya çıkardı. Bunlar β-laktamaz üreten bakteri türlerine karşı aktiviteleri açısından önemliydi, ancak daha sonra ortaya çıkan metisiline dirençli Staphylococcus aureus (MRSA) suşlarına karşı etkisizdi.[119]
Gerçek penisilinler serisindeki bir diğer gelişme de Gram negatif bakterilere karşı aktiviteleri nedeniyle yararlı olan karbenisilin, tikarsilin ve piperasilin gibi antipsödomonal penisilinler olmuştur. Bununla birlikte, β-laktam halkasının kullanışlılığı, mesilinamlar, karbapenemler ve en önemlisi sefalosporinler de dahil olmak üzere ilgili antibiyotiklerin yapılarının merkezinde hala bu halkayı muhafaza etmelerini sağlamıştır.[120]
Üretim[değiştir | kaynağı değiştir]

Penisilin, Penicillium rubens mantarı tarafından çeşitli şeker türlerinin fermantasyonu ile üretilir.[121] Fermantasyon süreci, mantarın büyümesi stres tarafından engellendiğinde ikincil bir metabolit olarak penisilin üretir.[121] Aşağıda özetlenen biyosentetik yol, homositrat sentaz enzimini inhibe eden yan ürün l-lizini içeren geri besleme inhibisyonu yaşar.[122]
Penicillium hücreleri, hücrelerin penisilin üretiminin indüksiyonu için gerekli olan strese sürekli maruz bırakıldığı beslemeli kesikli kültür adı verilen bir teknik kullanılarak yetiştirilmektedir. Karbon kaynağı olarak glukoz kullanımı penisilin biyosentez enzimlerini baskılarken, laktoz herhangi bir etki göstermez ve alkali pH seviyeleri bu düzenlemeyi geçersiz kılar. Aşırı fosfat, mevcut oksijen ve azot kaynağı olarak amonyum kullanımı penisilin üretimini baskılarken, metiyonin uyarıcı etkilere sahip tek bir azot/kükürt kaynağı olarak hareket edebilir.[123]
Yönlendirilmiş evrimin biyoteknolojik yöntemi, mutasyon yoluyla çok sayıda Penicillium suşu üretmek için uygulanmıştır. Bu teknikler arasında hataya eğilimli PCR, DNA karıştırma, ITCHY ve iplikçik örtüşmeli PCR yer almaktadır.
Yarı sentetik penisilinler, penisilin çekirdeği 6-APA'dan başlamak üzere hazırlanır.
Biyosentez[değiştir | kaynağı değiştir]

Genel olarak penisilin G'nin (benzilpenisilin) biyosentezinde üç ana ve önemli adım vardır.
- İlk adım, üç amino asidin-L-α-aminoadipik asit, L-sistein, L-valinin bir tripeptide yoğunlaşmasıdır.[124][125][126] Tripeptide yoğunlaşmadan önce, L-valin amino asidi D-valine dönüşmek için epimerizasyona uğramalıdır.[127][128] Yoğunlaşmış tripeptit δ-(L-α-aminoadipil)-L-sistein-D-valin (ACV) olarak adlandırılır. Yoğunlaşma reaksiyonu ve epimerizasyonun her ikisi de bir nonribozomal peptit sentetaz veya NRPS olan δ-(L-α-aminoadipil)-L-sistein-D-valin sentetaz (ACVS) enzimi tarafından katalize edilir.
- Penisilin G biyosentezindeki ikinci adım, pcbC geni tarafından kodlanan izopenisilin N sentaz (IPNS) tarafından lineer ACV'nin bisiklik ara ürün izopenisilin N'ye oksidatif dönüşümüdür.[124][125] İzopenisilin N çok zayıf bir ara üründür, çünkü güçlü antibiyotik aktivitesi göstermez.[127]
- Son adım, izopenisilin N'nin α-aminoadipil yan zincirinin çıkarıldığı ve bir fenilasetil yan zinciri ile değiştirildiği izopenisilin N N-asiltransferaz tarafından gerçekleştirilen bir transamidasyondur. Bu reaksiyon, penisilinlerin elde edilmesi sürecinde benzersiz olan penDE geni tarafından kodlanır.[124]
Ayrıca bakınız[değiştir | kaynağı değiştir]
Kaynakça[değiştir | kaynağı değiştir]
- ^ "American Chemical Society National Historic Chemical Landmarks. Penicillin Production through Deep-tank Fermentation". American Chemical Society. 2008-06-12. 2020-10-24 tarihinde kaynağından arşivlendi. Erişim tarihi: 2022-06-15.
- ^ Barreiro C, García-Estrada C (April 2019). "Proteomics and Penicillium chrysogenum: Unveiling the secrets behind penicillin production". Journal of Proteomics. Elsevier. 198: 119–131. doi:10.1016/j.jprot.2018.11.006. PMID 30414515.
- ^ Meštrović T (2018-08-29). "Penicillin Production". News Medical Life Sciences. 2023-04-04 tarihinde kaynağından arşivlendi. Erişim tarihi: 2022-06-15.
- ^ Wanat M, Anthierens S, Butler CC, Savic L, Savic S, Pavitt SH, ve diğerleri. (June 2021). "Management of penicillin allergy in primary care: a qualitative study with patients and primary care physicians". BMC Family Practice. 22 (1): 112. doi:10.1186/s12875-021-01465-1. PMC 8194168 $2. PMID 34116641.
- ^ Lalchhandama K (2020). "Reappraising Fleming's snot and mould". Science Vision. 20 (1): 29–42. doi:10.33493/scivis.20.01.03.
- ^ a b Fleming A (1943). "Streptococcal Meningitis treated With Penicillin". The Lancet (İngilizce). 242 (6267): 434–438. doi:10.1016/S0140-6736(00)87452-8.
- ^ a b c d e f g h Robinson FA (July 1947). "Chemistry of penicillin". The Analyst. 72 (856): 274–6. Bibcode:1947Ana....72..274R. doi:10.1039/an9477200274. PMID 20259048.
- ^ Diggins FW (1999). "The true history of the discovery of penicillin, with refutation of the misinformation in the literature". British Journal of Biomedical Science. 56 (2): 83–93. PMID 10695047.
- ^ Krylov AK (1929). "[Gastroenterologic aspects of the clinical picture of internal diseases]". Terapevticheskii Arkhiv. 63 (2): 139–41. PMC 2041430 $2. PMID 2048009.; Reprinted as Fleming A (1979). "On the antibacterial action of cultures of a Penicillium, with special reference to their use in the isolation of B. influenzae". British Journal of Experimental Pathology. 60 (1): 3–13. JSTOR 4452419. PMC 2041430 $2.
- ^ Fleming A (1945). "Nobel Lecture" (PDF). www.nobelprize.org. 31 March 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 19 July 2020.
- ^ Patrick GL (2017). Medicinal Chemistry (6th bas.). Oxford, UK: Oxford University Press. s. 425. ISBN 978-0198749691.
- ^ a b "Recommendations of the International Conference on Penicillin". Science. 101 (2611): 42–43. 1945-01-12. Bibcode:1945Sci...101...42.. doi:10.1126/science.101.2611.42. PMID 17758593.
- ^ Committee on Medical Research; The Medical Research Council (1945). "Chemistry of Penicillin". Science. American Association for the Advancement of Science. 102 (2660): 627–629. Bibcode:1945Sci...102..627M. doi:10.1126/science.102.2660.627. ISSN 0036-8075. JSTOR 1673446. PMID 17788243. 9 May 2022 tarihinde kaynağından arşivlendi. Erişim tarihi: 9 May 2022.
- ^ "The Relative Activity of Penicillins F, G, K, and X Against Spirochetes and Streptococci in Vitro". Journal of Bacteriology. 52 (1): 81–8. July 1946. doi:10.1128/JB.52.1.81-88.1946. PMC 518141 $2. PMID 16561156.
- ^ "Penicillin F". PubChem. National Center for Biotechnology Information, National Library of Medicine. 2021-05-07 tarihinde kaynağından arşivlendi. Erişim tarihi: 2020-12-26.
- ^ "Penicillin G". PubChem. National Center for Biotechnology Information, National Library of Medicine. 2020-12-25 tarihinde kaynağından arşivlendi. Erişim tarihi: 2020-12-26.
- ^ "Penicillin X". PubChem. National Center for Biotechnology Information, National Library of Medicine. 2021-05-05 tarihinde kaynağından arşivlendi. Erişim tarihi: 2020-12-26.
- ^ "Penicillin K". PubChem. National Center for Biotechnology Information, National Library of Medicine. 2021-05-06 tarihinde kaynağından arşivlendi. Erişim tarihi: 2020-12-26.
- ^ "Penicillin O". PubChem. National Center for Biotechnology Information, National Library of Medicine. 2021-05-05 tarihinde kaynağından arşivlendi. Erişim tarihi: 2020-12-26.
- ^ Fishman LS, Hewitt WL (September 1970). "The natural penicillins". The Medical Clinics of North America. 54 (5): 1081–99. doi:10.1016/S0025-7125(16)32579-2. PMID 4248661.
- ^ Genus Pharmaceuticals (2020-11-30). "Benzylpenicillin sodium 1200mg Powder for Injection". Electronic medicines compendium. Datapharm Ltd. 2021-01-15 tarihinde kaynağından arşivlendi. Erişim tarihi: 2020-12-28.
- ^ Sandoz GmbH. "Penicillin-VK" (PDF). US FDA. 2021-01-21 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 2020-12-28.
- ^ "Penicillin, 5,000 Oxford Units". National Museum of American History. Behring Center, Washington, D. C. 2021-05-06 tarihinde kaynağından arşivlendi. Erişim tarihi: 2020-12-28.
- ^ Robinson GL (February 1947). "Penicillin in general practice". Postgraduate Medical Journal. 23 (256): 86–92. doi:10.1136/pgmj.23.256.86. PMC 2529492 $2. PMID 20284177.
- ^ a b Greenwood D (2008). Antimicrobial Drugs: A Chronicle of a Twentieth Century Medical Triumph. Oxford, UK: Oxford University Press. s. 107. ISBN 978-0-19-953484-5.
- ^ Abraham EP, Chain E, Fletcher CM, Gardner AD, Heatley NG, Jennings MA, Florey HW (1941). "Further observations on penicillin". Lancet. 238 (6155): 177–189. doi:10.1016/S0140-6736(00)72122-2.
- ^ a b Foster JW, Woodruff HB (August 1943). "Microbiological Aspects of Penicillin: I. Methods of Assay". Journal of Bacteriology. 46 (2): 187–202. doi:10.1128/JB.46.2.187-202.1943. PMC 373803 $2. PMID 16560688.
- ^ Hartley P (June 1945). "World Standard and Unit for Penicillin". Science. 101 (2634): 637–8. Bibcode:1945Sci...101..637H. doi:10.1126/science.101.2634.637. PMID 17844083.
- ^ Humphrey JH, Musset MV, Perry WL (1953). "The second international standard for penicillin". Bulletin of the World Health Organization. 9 (1): 15–28. PMC 2542105 $2. PMID 13082387.
- ^ Humphrey JH, Lightbown JW, Mussett MV (1959). "International Standard for phenoxymethylpenicillin". Bulletin of the World Health Organization. 20 (6): 1221–7. PMC 2537888 $2. PMID 14405369.
- ^ Humphrey JH, Lightbown JW (1954). "The international reference preparation of penicillin K". Bulletin of the World Health Organization. 10 (6): 895–9. PMC 2542178 $2. PMID 13199652.
- ^ "Penicillin G Potassium Injection, USP" (PDF). US FDA. July 2016. 2021-04-01 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 2020-12-28.
- ^ Pandey N, Cascella M (2020), "Beta Lactam Antibiotics", StatPearls, Treasure Island (FL): StatPearls Publishing, PMID 31424895, 2020-12-15 tarihinde kaynağından arşivlendi, erişim tarihi: 2021-01-05
- ^ a b Rossi S, (Ed.) (2006). Australian Medicines Handbook. Adelaide: Australian Medicines Handbook. ISBN 978-0-9757919-2-9.
- ^ Bhattacharya S (January 2010). "The facts about penicillin allergy: a review". Journal of Advanced Pharmaceutical Technology & Research. 1 (1): 11–7. PMC 3255391 $2. PMID 22247826.
- ^ Blumenthal KG, Peter JG, Trubiano JA, Phillips EJ (January 2019). "Antibiotic allergy". Lancet. 393 (10167): 183–198. doi:10.1016/S0140-6736(18)32218-9. PMC 6563335 $2. PMID 30558872.
- ^ a b Hitchings A, Lonsdale D, Burrage D, Baker E (2015). Top 100 drugs: clinical pharmacology and practical prescribing. Churchill Livingstone. ss. 174–181. ISBN 978-0-7020-5516-4.
- ^ Kim KK, Chae DS (2015). "Nicolau syndrome: A literature review". World Journal of Dermatology. 4 (2): 103. doi:10.5314/wjd.v4.i2.103.
- ^ Saputo V, Bruni G (1998). "[Nicolau syndrome caused by penicillin preparations: review of the literature in search for potential risk factors]". La Pediatria Medica e Chirurgica. 20 (2): 105–23. PMID 9706633.
- ^ a b Fernandes R, Amador P, Prudêncio C (2013). "β-Lactams: chemical structure, mode of action and mechanisms of resistance". Reviews in Medical Microbiology (İngilizce). 24 (1): 7–17. doi:10.1097/MRM.0b013e3283587727. hdl:10400.22/7041.
- ^ Nicolaou (1996), pg. 43.
- ^ Fisher JF, Mobashery S (October 2009). "Three decades of the class A beta-lactamase acyl-enzyme". Current Protein & Peptide Science. 10 (5): 401–7. doi:10.2174/138920309789351967. PMC 6902449 $2. PMID 19538154.
- ^ a b Morell EA, Balkin DM (December 2010). "Methicillin-resistant Staphylococcus aureus: a pervasive pathogen highlights the need for new antimicrobial development". The Yale Journal of Biology and Medicine. 83 (4): 223–33. PMC 3002151 $2. PMID 21165342.
- ^ Silhavy TJ, Kahne D, Walker S (May 2010). "The bacterial cell envelope". Cold Spring Harbor Perspectives in Biology. 2 (5): a000414. doi:10.1101/cshperspect.a000414. PMC 2857177 $2. PMID 20452953.
- ^ a b c Fleming A (1929). "On the Antibacterial Action of Cultures of a Penicillium, with Special Reference to their Use in the Isolation of B. influenzæ". British Journal of Experimental Pathology. 10 (3): 226–236. PMC 2048009 $2. Reprinted as Fleming A (1980). "Classics in infectious diseases: on the antibacterial action of cultures of a penicillium, with special reference to their use in the isolation of B. influenzae by Alexander Fleming, Reprinted from the British Journal of Experimental Pathology 10:226–236, 1929". Reviews of Infectious Diseases. 2 (1): 129–39. doi:10.1093/clinids/2.1.129. PMC 2041430 $2. PMID 6994200.
- ^ a b Lambert PA (2002). "Cellular impermeability and uptake of biocides and antibiotics in Gram-positive bacteria and mycobacteria". Journal of Applied Microbiology. 92 (Suppl): 46S–54S. doi:10.1046/j.1365-2672.92.5s1.7.x. PMID 12000612.
- ^ Vergalli J, Bodrenko IV, Masi M, Moynié L, Acosta-Gutiérrez S, Naismith JH, ve diğerleri. (March 2020). "Porins and small-molecule translocation across the outer membrane of Gram-negative bacteria" (PDF). Nature Reviews. Microbiology. 18 (3): 164–176. doi:10.1038/s41579-019-0294-2. PMID 31792365. 2021-10-22 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 2021-07-30.
- ^ Masi M, Winterhalter M, Pagès JM (2019). "Outer Membrane Porins". Bacterial Cell Walls and Membranes. Subcellular Biochemistry. 92. ss. 79–123. doi:10.1007/978-3-030-18768-2_4. ISBN 978-3-030-18767-5. PMID 31214985.
- ^ a b c d Soares GM, Figueiredo LC, Faveri M, Cortelli SC, Duarte PM, Feres M (2012). "Mechanisms of action of systemic antibiotics used in periodontal treatment and mechanisms of bacterial resistance to these drugs". Journal of Applied Oral Science. 20 (3): 295–309. doi:10.1590/s1678-77572012000300002. PMC 3881775 $2. PMID 22858695.
- ^ Antonoplis A, Zang X, Wegner T, Wender PA, Cegelski L (September 2019). "Vancomycin-Arginine Conjugate Inhibits Growth of Carbapenem-Resistant E. coli and Targets Cell-Wall Synthesis". ACS Chemical Biology. 14 (9): 2065–2070. doi:10.1021/acschembio.9b00565. PMC 6793997 $2. PMID 31479234.
- ^ a b Breijyeh Z, Jubeh B, Karaman R (March 2020). "Resistance of Gram-Negative Bacteria to Current Antibacterial Agents and Approaches to Resolve It". Molecules. 25 (6): 1340. doi:10.3390/molecules25061340. PMC 7144564 $2. PMID 32187986.
- ^ a b Cushnie TP, O'Driscoll NH, Lamb AJ (December 2016). "Morphological and ultrastructural changes in bacterial cells as an indicator of antibacterial mechanism of action". Cellular and Molecular Life Sciences. 73 (23): 4471–4492. doi:10.1007/s00018-016-2302-2. hdl:10059/2129. PMID 27392605. 2017-10-07 tarihinde kaynağından arşivlendi. Erişim tarihi: 2019-10-10.
- ^ Yocum RR, Rasmussen JR, Strominger JL (May 1980). "The mechanism of action of penicillin. Penicillin acylates the active site of Bacillus stearothermophilus D-alanine carboxypeptidase". The Journal of Biological Chemistry. 255 (9): 3977–86. doi:10.1016/S0021-9258(19)85621-1. PMID 7372662.
- ^ "Benzylpenicillin". www.drugbank.ca. 23 January 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 22 January 2019.
- ^ DeMeester KE, Liang H, Jensen MR, Jones ZS, D'Ambrosio EA, Scinto SL, ve diğerleri. (August 2018). "Synthesis of Functionalized N-Acetyl Muramic Acids To Probe Bacterial Cell Wall Recycling and Biosynthesis". Journal of the American Chemical Society. 140 (30): 9458–9465. doi:10.1021/jacs.8b03304. PMC 6112571 $2. PMID 29986130.
- ^ Gordon E, Mouz N, Duée E, Dideberg O (June 2000). "The crystal structure of the penicillin-binding protein 2x from Streptococcus pneumoniae and its acyl-enzyme form: implication in drug resistance". Journal of Molecular Biology. 299 (2): 477–85. doi:10.1006/jmbi.2000.3740. PMID 10860753.
- ^ Van Bambeke F, Lambert D, Mingeot-Leclercq MP, Tulkens P (1999). Mechanism of Action (PDF). 2022-01-25 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 2014-03-13.
- ^ Winstanley TG, Hastings JG (February 1989). "Penicillin-aminoglycoside synergy and post-antibiotic effect for enterococci". The Journal of Antimicrobial Chemotherapy. 23 (2): 189–99. doi:10.1093/jac/23.2.189. PMID 2708179.
- ^ Kasten B, Reski R (March 30, 1997). "β-lactam antibiotics inhibit chloroplast division in a moss (Physcomitrella patens) but not in tomato (Lycopersicon esculentum)". Journal of Plant Physiology. 150 (1–2): 137–140. doi:10.1016/S0176-1617(97)80193-9. July 21, 2011 tarihinde kaynağından arşivlendi. Erişim tarihi: March 30, 2009.
- ^ a b Levison ME, Levison JH (December 2009). "Pharmacokinetics and pharmacodynamics of antibacterial agents". Infectious Disease Clinics of North America. 23 (4): 791–815, vii. doi:10.1016/j.idc.2009.06.008. PMC 3675903 $2. PMID 19909885.
- ^ Walton AL, Howden BP, Grayson LM, Korman TM (May 2007). "Continuous-infusion penicillin home-based therapy for serious infections due to penicillin-susceptible pathogens". International Journal of Antimicrobial Agents. 29 (5): 544–8. doi:10.1016/j.ijantimicag.2006.10.018. PMID 17398076.
- ^ a b Abraham EP, Chain E (1940). "An enzyme from bacteria able to destroy penicillin. 1940". Reviews of Infectious Diseases. 10 (4): 677–8. Bibcode:1940Natur.146..837A. doi:10.1038/146837a0. PMID 3055168.
- ^ Rice LB (February 2012). "Mechanisms of resistance and clinical relevance of resistance to β-lactams, glycopeptides, and fluoroquinolones". Mayo Clinic Proceedings. 87 (2): 198–208. doi:10.1016/j.mayocp.2011.12.003. PMC 3498059 $2. PMID 22305032.
- ^ Pagès JM, James CE, Winterhalter M (December 2008). "The porin and the permeating antibiotic: a selective diffusion barrier in Gram-negative bacteria" (PDF). Nature Reviews. Microbiology. 6 (12): 893–903. doi:10.1038/nrmicro1994. PMID 18997824. 2018-11-23 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 2021-07-30.
- ^ Jacobs MR (May 1999). "Drug-resistant Streptococcus pneumoniae: rational antibiotic choices". The American Journal of Medicine. 106 (5A): 19S-25S; discussion 48S-52S. doi:10.1016/s0002-9343(98)00351-9. PMID 10348060.
- ^ a b Zapun A, Contreras-Martel C, Vernet T (March 2008). "Penicillin-binding proteins and beta-lactam resistance". FEMS Microbiology Reviews. 32 (2): 361–85. doi:10.1111/j.1574-6976.2007.00095.x. PMID 18248419.
- ^ Peacock SJ, Paterson GK (2015). "Mechanisms of Methicillin Resistance in Staphylococcus aureus" (PDF). Annual Review of Biochemistry. 84: 577–601. doi:10.1146/annurev-biochem-060614-034516. PMID 26034890.
- ^ Reygaert W (2009). "Methicillin-resistant Staphylococcus aureus (MRSA): molecular aspects of antimicrobial resistance and virulence". Clinical Laboratory Science. 22 (2): 115–9. PMID 19534446. 2021-01-12 tarihinde kaynağından arşivlendi. Erişim tarihi: 2021-01-08.
- ^ Rimbara E, Mori S, Kim H, Suzuki M, Shibayama K (February 2018). "Mutations in Genes Encoding Penicillin-Binding Proteins and Efflux Pumps Play a Role in β-Lactam Resistance in Helicobacter cinaedi". Antimicrobial Agents and Chemotherapy. 62 (2): e02036-17. doi:10.1128/AAC.02036-17. PMC 5786776 $2. PMID 29203490.
- ^ Tooke CL, Hinchliffe P, Bragginton EC, Colenso CK, Hirvonen VH, Takebayashi Y, Spencer J (August 2019). "β-Lactamases and β-Lactamase Inhibitors in the 21st Century". Journal of Molecular Biology. 431 (18): 3472–3500. doi:10.1016/j.jmb.2019.04.002. PMC 6723624 $2. PMID 30959050.
- ^ a b Bonomo RA (January 2017). "β-Lactamases: A Focus on Current Challenges". Cold Spring Harbor Perspectives in Medicine. 7 (1): a025239. doi:10.1101/cshperspect.a025239. PMC 5204326 $2. PMID 27742735.
- ^ Davies J, Davies D (September 2010). "Origins and evolution of antibiotic resistance". Microbiology and Molecular Biology Reviews. 74 (3): 417–33. doi:10.1128/MMBR.00016-10. PMC 2937522 $2. PMID 20805405.
- ^ Bush K (October 2018). "Past and Present Perspectives on β-Lactamases". Antimicrobial Agents and Chemotherapy. 62 (10): e01076-18. doi:10.1128/AAC.01076-18. PMC 6153792 $2. PMID 30061284.
- ^ Pang Z, Raudonis R, Glick BR, Lin TJ, Cheng Z (2019). "Antibiotic resistance in Pseudomonas aeruginosa: mechanisms and alternative therapeutic strategies". Biotechnology Advances. 37 (1): 177–192. doi:10.1016/j.biotechadv.2018.11.013. PMID 30500353.
- ^ Dougherty TJ, Pucci MJ (2011). Antibiotic Discovery and Development. Springer Science & Business Media. ss. 79–80.
- ^ Landau R, Achilladelis B, Scriabine A (1999). Pharmaceutical Innovation: Revolutionizing Human Health. Chemical Heritage Foundation. s. 162.
- ^ Haven KF (1994). Marvels of Science: 50 Fascinating 5-Minute Reads. Littleton, CO: Libraries Unlimited. s. 182. ISBN 978-1-56308-159-0.
- ^ Gaynes, R. (2017). "The Discovery of Penicillin—New Insights After More Than 75 Years of Clinical Use". Emerging Infectious Diseases. 23 (5): 849–853. doi:10.3201/eid2305.161556. PMC 5403050 $2.
- ^ Houbraken J, Frisvad JC, Samson RA (June 2011). "Fleming's penicillin producing strain is not Penicillium chrysogenum but P. rubens". IMA Fungus. 2 (1): 87–95. doi:10.5598/imafungus.2011.02.01.12. PMC 3317369 $2. PMID 22679592.
- ^ a b c Lax E (2004). The Mold in Dr. Florey's Coat: The Story of the Penicillin Miracle. Holt Paperbacks. ISBN 978-0-8050-7778-0.
- ^ Krylov AK (1991). "[Gastroenterologic aspects of the clinical picture of internal diseases]". Terapevticheskii Arkhiv. 63 (2): 139–41. PMID 2048009.
- ^ "Discovery and Development of Penicillin". International Historic Chemical Landmarks. American Chemical Society. June 28, 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: August 21, 2018.
- ^ Wainwright M, Swan HT (January 1986). "C.G. Paine and the earliest surviving clinical records of penicillin therapy". Medical History. 30 (1): 42–56. doi:10.1017/S0025727300045026. PMC 1139580 $2. PMID 3511336.
- ^ Howie J (July 1986). "Penicillin: 1929-40". British Medical Journal. 293 (6540): 158–9. doi:10.1136/bmj.293.6540.158. PMC 1340901 $2. PMID 3089435.
- ^ Wainwright M (January 1987). "The history of the therapeutic use of crude penicillin". Medical History. 31 (1): 41–50. doi:10.1017/s0025727300046305. PMC 1139683 $2. PMID 3543562.
- ^ a b Jones DS, Jones JH (2014-12-01). "Sir Edward Penley Abraham CBE. 10 June 1913 – 9 May 1999". Biographical Memoirs of Fellows of the Royal Society. 60: 5–22. doi:10.1098/rsbm.2014.0002. ISSN 0080-4606. 26 November 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 10 May 2017.
- ^ "Ernst B. Chain – Nobel Lecture: The Chemical Structure of the Penicillins". www.nobelprize.org. 2017-04-30 tarihinde kaynağından arşivlendi. Erişim tarihi: 2017-05-10.
- ^ a b c "Making Penicillin Possible: Norman Heatley Remembers". ScienceWatch. Thomson Scientific. 2007. February 21, 2007 tarihinde kaynağından arşivlendi. Erişim tarihi: 2007-02-13.
- ^ Levy SB (2002). The Antibiotic Paradox: How the Misuse of Antibiotics Destroys Their Curative Powers. Da Capo Press. ss. 5–7. ISBN 978-0-7382-0440-6.
- ^ Bennett JW, Chung KT (2001). "Alexander Fleming and the discovery of penicillin". Advances in Applied Microbiology. Elsevier. 49: 163–84. doi:10.1016/s0065-2164(01)49013-7. ISBN 978-0-12-002649-4. PMID 11757350.
- ^ Cairns H, Lewin WS, Duthie ES, Smith H (1944). "Pneumococcal Meningitis Treated with Penicillin". The Lancet (İngilizce). 243 (6299): 655–659. doi:10.1016/S0140-6736(00)77085-1.
- ^ Mathews JA (2008). "The Birth of the Biotechnology Era: Penicillin in Australia, 1943–80". Prometheus. 26 (4): 317–333. doi:10.1080/08109020802459306.
- ^ Baldry P (1976). The Battle Against Bacteria: A Fresh Look (İngilizce). CUP Archive. s. 115. ISBN 978-0-521-21268-7. 2021-05-05 tarihinde kaynağından arşivlendi. Erişim tarihi: 2020-12-31.
- ^ a b Boucher HW, Talbot GH, Benjamin DK, Bradley J, Guidos RJ, Jones RN, ve diğerleri. (June 2013). "10 x '20 Progress--development of new drugs active against gram-negative bacilli: an update from the Infectious Diseases Society of America". Clinical Infectious Diseases. 56 (12): 1685–94. doi:10.1093/cid/cit152. PMC 3707426 $2. PMID 23599308.
- ^ Carroll A (2014-06-02). "Here is Where: Penicillin Comes to Peoria". HistoryNet (İngilizce). 2021-01-07 tarihinde kaynağından arşivlendi. Erişim tarihi: 2021-01-04.
- ^ Grossman CM (July 2008). "The first use of penicillin in the United States". Annals of Internal Medicine. 149 (2): 135–6. doi:10.7326/0003-4819-149-2-200807150-00009. PMID 18626052.
- ^ Rothman L (14 March 2016). "Penicillin history: what happened to first American patient". Time. 17 March 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 12 March 2019.
- ^ Mailer JS, Mason B. "Penicillin : Medicine's Wartime Wonder Drug and Its Production at Peoria, Illinois". lib.niu.edu. October 7, 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: February 11, 2008.
- ^ a b Parascandola J (1980). The History of antibiotics: a symposium. American Institute of the History of Pharmacy No. 5. ISBN 978-0-931292-08-8.
- ^ "The History of Penicillin and Antibiotics". ThoughtCo (İngilizce). 8 Nisan 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 2024-06-09.
- ^ Lehrer S (2006). Explorers of the Body: Dramatic Breakthroughs in Medicine from Ancient Times to Modern Science (2nd bas.). New York: iUniverse. ss. 329–330. ISBN 978-0-595-40731-6.
- ^ Madhavan G (Aug 20, 2015). Think Like an Engineer. Oneworld Publications. ss. 83–85, 91–93. ISBN 978-1-78074-637-1. 23 March 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 20 November 2016.
- ^ "G. Raymond Rettew Historical Marker". ExplorePAhistory.com. January 5, 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: June 27, 2019.
- ^ Goyotte D (2017). "The Surgical Legacy of World War II. Part II: The age of antibiotics" (PDF). The Surgical Technologist. 109: 257–264. 2021-05-05 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 2021-01-08.
- ^ US 2442141, Moyer AJ, "Method for Production of Penicillin", 25 March 1948 tarihinde verildi, assigned to US Agriculture
- ^ US 2443989, Moyer AJ, "Method for Production of Penicillin", 22 June 1948 tarihinde verildi, assigned to US Agriculture
- ^ US 2476107, Moyer AJ, "Method for Production of Penicillin", 12 July 1949 tarihinde verildi, assigned to US Agriculture
- ^ a b Silverthorn DU (2004). Human physiology: an integrated approach (3rd bas.). Upper Saddle River (NJ): Pearson Education. ISBN 978-0-8053-5957-2.
- ^ Luque Paz D, Lakbar I, Tattevin P (March 2021). "A review of current treatment strategies for infective endocarditis". Expert Review of Anti-Infective Therapy. 19 (3): 297–307. doi:10.1080/14787210.2020.1822165. PMID 32901532.
- ^ "Discovery and development of penicillin". American Chemical Society. 1999. 2015-01-03 tarihinde kaynağından arşivlendi. Erişim tarihi: 2015-01-04.
- ^ "The Nobel Prize in Chemistry 1964". NobelPrize.org. 2017-07-16 tarihinde kaynağından arşivlendi. Erişim tarihi: 9 May 2022.
- ^ a b Sheehan JC, Henery-Logan KR (March 5, 1957). "The Total Synthesis of Penicillin V". Journal of the American Chemical Society. 79 (5): 1262–1263. doi:10.1021/ja01562a063.
- ^ a b Sheehan JC, Henery-Loganm KR (June 20, 1959). "The Total Synthesis of Penicillin V". Journal of the American Chemical Society. 81 (12): 3089–3094. doi:10.1021/ja01521a044.
- ^ a b c Corey EJ, Roberts JD. "Biographical Memoirs: John Clark Sheehan". The National Academy Press. March 3, 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: January 28, 2013.
- ^ Nicolaou KC, Vourloumis D, Winssinger N, Baran PS (January 2000). "The Art and Science of Total Synthesis at the Dawn of the Twenty-First Century". Angewandte Chemie. 39 (1): 44–122. doi:10.1002/(SICI)1521-3773(20000103)39:1<44::AID-ANIE44>3.0.CO;2-L. PMID 10649349.
- ^ "Professor John C. Sheehan Dies at 76". MIT News. April 1, 1992. June 30, 2008 tarihinde kaynağından arşivlendi. Erişim tarihi: January 28, 2013.
- ^ Batchelor FR, Doyle FP, Nayler JH, Rolinson GN (January 1959). "Synthesis of penicillin: 6-aminopenicillanic acid in penicillin fermentations". Nature. 183 (4656): 257–8. Bibcode:1959Natur.183..257B. doi:10.1038/183257b0. PMID 13622762.
- ^ Rolinson GN, Geddes AM (January 2007). "The 50th anniversary of the discovery of 6-aminopenicillanic acid (6-APA)". International Journal of Antimicrobial Agents. 29 (1): 3–8. doi:10.1016/j.ijantimicag.2006.09.003. PMID 17137753.
- ^ Colley EW, Mcnicol MW, Bracken PM (March 1965). "Methicillin-Resistant Staphylococci in a General Hospital". Lancet. 1 (7385): 595–7. doi:10.1016/S0140-6736(65)91165-7. PMID 14250094.
- ^ James CW, Gurk-Turner C (January 2001). "Cross-reactivity of beta-lactam antibiotics". Proceedings. 14 (1): 106–7. doi:10.1080/08998280.2001.11927741. PMC 1291320 $2. PMID 16369597.
- ^ a b Kosalková K, Sánchez-Orejas IC, Cueto L, García-Estrada C (2021). "Penicillium chrysogenum Fermentation and Analysis of Benzylpenicillin by Bioassay and HPLC". Barreiro C, Barredo JL (Ed.). Antimicrobial Therapies. Methods in Molecular Biology (İngilizce). 2296. New York, NY: Springer US. ss. 195–207. doi:10.1007/978-1-0716-1358-0_11. ISBN 978-1-0716-1357-3. PMID 33977449.
- ^ Luengo JM, Revilla G, López MJ, Villanueva JR, Martín JF (December 1980). "Inhibition and repression of homocitrate synthase by lysine in Penicillium chrysogenum". Journal of Bacteriology. 144 (3): 869–876. doi:10.1128/jb.144.3.869-876.1980. PMC 294747 $2. PMID 6777369.
- ^ Ozcengiz G, Demain AL (2013-03-01). "Recent advances in the biosynthesis of penicillins, cephalosporins and clavams and its regulation". Biotechnology Advances. 31 (2): 287–311. doi:10.1016/j.biotechadv.2012.12.001. PMID 23228980.
- ^ a b c Al-Abdallah Q, Brakhage AA, Gehrke A, Plattner H, Sprote P, Tuncher A (2004). "Regulation of Penicillin Biosynthesis in Filamentous Fungi". Brakhage AA (Ed.). Molecular Biotechnology of Fungal beta-Lactam Antibiotics and Related Peptide Synthetases. Advances in Biochemical Engineering/Biotechnology. 88. ss. 45–90. doi:10.1007/b99257. ISBN 978-3-540-22032-9. PMID 15719552.
- ^ a b Brakhage AA (September 1998). "Molecular regulation of beta-lactam biosynthesis in filamentous fungi". Microbiology and Molecular Biology Reviews. 62 (3): 547–85. doi:10.1128/MMBR.62.3.547-585.1998. PMC 98925 $2. PMID 9729600.
- ^ Schofield CJ, Baldwin JE, Byford MF, Clifton I, Hajdu J, Hensgens C, Roach P (December 1997). "Proteins of the penicillin biosynthesis pathway". Current Opinion in Structural Biology. 7 (6): 857–64. doi:10.1016/s0959-440x(97)80158-3. PMID 9434907.
- ^ a b Martín JF, Gutiérrez S, Fernández FJ, Velasco J, Fierro F, Marcos AT, Kosalkova K (September 1994). "Expression of genes and processing of enzymes for the biosynthesis of penicillins and cephalosporins". Antonie van Leeuwenhoek. 65 (3): 227–43. doi:10.1007/BF00871951. PMID 7847890.
- ^ Baker WL, Lonergan GT (December 2002). "Chemistry of some fluorescamine–amine derivatives with relevance to the biosynthesis of benzylpenicillin by fermentation". Journal of Chemical Technology & Biotechnology. 77 (12): 1283–8. Bibcode:2002JCTB...77.1283B. doi:10.1002/jctb.706.


 French
French Deutsch
Deutsch

