溴化亚铁 - 维基百科,自由的百科全书
| 溴化亚铁 | |
|---|---|
 | |
| IUPAC名 溴化铁(II) | |
| 识别 | |
| CAS号 | 7789-46-0 |
| ChemSpider | 74218 |
| InChI |
|
| InChIKey | GYCHYNMREWYSKH-NUQVWONBAN |
| 性质 | |
| 化学式 | FeBr2 |
| 摩尔质量 | 215.65 g·mol⁻¹ |
| 外观 | 棕黄色固体 米白色固体(二水) 浅绿蓝色晶体(四水) 浅蓝绿色晶体(六水)[1] |
| 密度 | 4.63 g/cm3(固态) |
| 熔点 | 684 °C(957 K) |
| 沸点 | 934 °C(1207 K) |
| 溶解性(水) | 可溶于水 |
| 危险性 | |
| 警示术语 | R:R20, R36/37/38 |
| 安全术语 | S:S26, S36 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
溴化亚铁,化学式FeBr2,棕黄色潮解固体,可溶于水。在室温下从水溶液中结晶出淡绿色的六水合物。温度升高时,也可结晶出四水合物和二水合物。400 °C时,在溴化氢气流中加热含水的溴化亚铁,可以得到无水盐。
结构
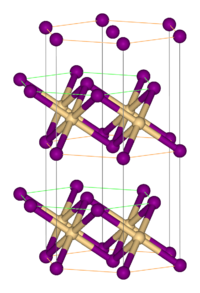
[编辑]FeBr2为碘化镉型层状晶格结构,Br−成紧密堆积的层,Fe2+填充在八面体空隙中。[2]
同族的碘形成的碘化亚铁也采取这种结构,但在另外两个卤化亚铁中,氯化亚铁为氯化镉型结构,氟化亚铁则为金红石型结构。
无水溴化亚铁可溶于乙醚、乙醇和乙腈中,表明该化合物具有一定的共价性。
制备
[编辑]此外,赤热的铁与溴或溴化氢反应也可以生成溴化亚铁。高温时溴化铁会分解为溴化亚铁。
参见
[编辑]参考资料
[编辑]- ^ C. D. Burbridge, D. M. L. Goodgame. Electronic and Mössbauer spectra of some iron( II ) halide hydrates. J. Chem. Soc. A. 1968, 0 (0): 1410–1413 [2023-03-16]. ISSN 0022-4944. doi:10.1039/J19680001410 (英语).
- ^ Haberecht, J.; Borrmann, H.; Kniep, R. "Refinement of the Crystal Structure of Iron Dibromide, FeBr2 Zeitschrift für Kristallographie - New Crystal Structures (2001), volume 216, page 510.


 French
French Deutsch
Deutsch