Alternative Periodensysteme – Wikipedia
Alternative Periodensysteme unterscheiden sich in Darstellung und Zuordnung der chemischen Elemente vom traditionellen Periodensystem. Seit ein systematischer Zusammenhang zwischen Atommasse und chemischen Eigenschaften der Elemente entdeckt wurde, gab es mehrere alternative Vorschläge zu der von Dimitri Iwanowitsch Mendelejew (1834–1907) und Lothar Meyer (1830–1895) aufgestellten Ordnung der Elemente. Jedoch blieb dieses Periodensystem das allgemein übliche Periodensystem in der Chemie.[1] Graphische Darstellungen mit inneren Beziehungen der Elemente mittels Vektoren und Klammern nennt man Periodensysteme in Form geordneter Hypergraphen.
Janet-Periodensystem
[Bearbeiten | Quelltext bearbeiten]Charles Janet erstellte ein Periodensystem, bei welchem die Elemente nach Blöcken angeordnet wurden. In einem Block werden die chemischen Elemente nach den energiereichsten Orbitalen ihrer Elektronenhülle zusammengefasst. Dieses Periodensystem ist heute noch manchmal in der Physik gebräuchlich.[2]
| f-Block | d-Block | p-Block | s-Block | ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 H | 2 He | ||||||||||||||||||||||||||||||
| 3 Li | 4 Be | ||||||||||||||||||||||||||||||
| 5 B | 6 C | 7 N | 8 O | 9 F | 10 Ne | 11 Na | 12 Mg | ||||||||||||||||||||||||
| 13 Al | 14 Si | 15 P | 16 S | 17 Cl | 18 Ar | 19 K | 20 Ca | ||||||||||||||||||||||||
| 21 Sc | 22 Ti | 23 V | 24 Cr | 25 Mn | 26 Fe | 27 Co | 28 Ni | 29 Cu | 30 Zn | 31 Ga | 33 As | 35 Br | 36 Kr | 37 Rb | 38 Sr | ||||||||||||||||
| 39 Y | 40 Zr | 41 Nb | 42 Mo | 43 Tc | 44 Ru | 45 Rh | 46 Pd | 47 Ag | 48 Cd | 49 In | 50 Sn | 52 Te | 53 I | 54 Xe | 55 Cs | 56 Ba | |||||||||||||||
| 57 La | 58 Ce | 59 Pr | 60 Nd | 61 Pm | 62 Sm | 63 Eu | 64 Gd | 65 Tb | 66 Dy | 67 Ho | 68 Er | 69 Tm | 70 Yb | 71 Lu | 72 Hf | 73 Ta | 74 W | 75 Re | 76 Os | 77 Ir | 78 Pt | 79 Au | 80 Hg | 81 Tl | 82 Pb | 83 Bi | 86 Rn | 87 Fr | 88 Ra | ||
| 89 Ac | 90 Th | 91 Pa | 92 U | 93 Np | 94 Pu | 95 Am | 96 Cm | 97 Bk | 98 Cf | 99 Es | 100 Fm | 101 Md | 102 No | 103 Lr | 104 Rf | 105 Db | 106 Sg | 107 Bh | 108 Hs | 109 Mt | 110 Ds | 111 Rg | 112 Cn | 113 Nh | 114 Fl | 115 Mc | 116 Lv | 117 Ts | 118 Og | ||
Elemente-Spirale
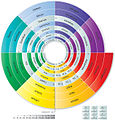
[Bearbeiten | Quelltext bearbeiten]Theodor Benfey entwickelte eine Systematik, bei welcher die chemischen Elemente spiralförmig angeordnet sind. Wasserstoff ist der Mittelpunkt der Spirale. Um den Mittelpunkt sind die Elemente mit größer werdender Masse angeordnet.
- Das von Theodor Benfey entwickelte Periodensystem
Weitere ähnliche Konzepte
[Bearbeiten | Quelltext bearbeiten]- Von Jan Scholten
- Von Robert W Harrison
- Kreisförmiges Periodensystem
- Pyramidenförmig angeordnet.
- Vom kanadischen Künstler Alexander Braun
- Spiralförmiges Schema des PSE
Blumen-Periodensystem
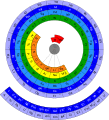
[Bearbeiten | Quelltext bearbeiten]Das Blumen-Periodensystem ist räumlich. Die Elemente sind nach aufsteigender Ordnungszahl als aufgewickeltes Band dargestellt. Die Nebengruppenelemente sowie die Actinoide und die Lanthanoide bilden jeweils eine Schleife neben den Hauptgruppenelementen.[3]
- Blumen-Periodensystem von Dmitri Mendelejew
Das Periodensystem von Stowe
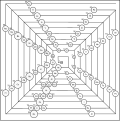
[Bearbeiten | Quelltext bearbeiten]Auch dieses Periodensystem ist dreidimensional. Das Periodensystem hat drei Achsen, welche die Hauptquantenzahl, die Nebenquantenzahl, und die Magnetische Quantenzahl darstellen. Das Periodensystem ist nach seinem Erfinder Timothy Stowe benannt.
Das Periodensystem von Bettermann
[Bearbeiten | Quelltext bearbeiten]Das Bettermannsche Periodensystem wird aus den isoelektronischen Reihen der Elemente abgeleitet. Eugenie Lisitzin zeigte 1936, dass diese Reihe als Polynom dargestellt werden kann. Auch die Valenzelektronen der Atome zeigen ein ähnliches Verhalten.[4]
- Die Isoelektronischen Reihen der Elemente
- Die Elemente geordnet nach den Parametern der Polynome
- Die Elemente nach ihren Valenzelektronen geordnet.
Periodensystem nach Allahyari und Oganov
[Bearbeiten | Quelltext bearbeiten]Die zwei russischen Wissenschaftler Zahed Allahyari und Artem R. Oganov vom Skolkowo-Institut für Wissenschaft und Technologie in Moskau veröffentlichten im Journal of Physical Chemistry 2020 ein eindimensionales Ordnungsschema. In diesem werden die chemischen Elemente gemäß ihrer „Ähnlichkeit“ in Bezug auf den Atomradius und der Elektronegativität nacheinander aufgereiht, welche als Mendelejew-Zahl bezeichnet wird. Diese Bezeichnung wurde in Anlehnung an einen der Mitbegründer des klassischen Periodensystems, Dmitri Mendelejew, gewählt. Die Forscher definierten den Wert für den Atomradius (da variabel) für eine ganz bestimmte Elementkonfiguration, und zwar für die sogenannte primitive kubische Struktur, bei der sich an den Ecken der würfelförmigen Elementarzelle jeweils ein Atom des Elements befindet. Die universale Sequenz der Elemente ergibt sich daraus aus ihrer Reihenfolge auf einer Regressionsgeraden in einem Liniendiagramm, wo Elektronegativität gegen Atomradius aufgetragen ist. Wasserstoff findet sich in dieser Liste beispielsweise relativ weit hinten in der Liste auf Position 90 vor Neon (91) und Helium (92). Das Ordnungskonzept auf Grundlage einer Mendelejew-Zahl ist nicht neu. Vorgeschlagen hatte es bereits der englische Chemiker David Pettifor im Jahr 1984. Die Forscher vermuten, dass sich auf Grundlage dieser Systematik neue Materialien mit nützlichen Eigenschaften wie Härte oder magnetischem Verhalten viel einfacher identifizieren lassen.[5][6]
Sonstige
[Bearbeiten | Quelltext bearbeiten]- Von Zmaczynski und Bayley.
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Volker Mrasek: Darstellung von Elementen – Wasserstoff in alternativen Periodensystemen. In: Deutschlandfunk-Sendung „Wissenschaft im Brennpunkt“. 3. März 2019.
- Janosch Deeg: Elemente anders ordnen – Konkurrenz für das Periodensystem. In: Frankfurter Allgemeine Zeitung. 3. Januar 2021.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Hans-Jürgen Quadbeck-Seeger Die Welt der Elemente – Die Elemente der Welt. Wiley-VCH Verlag, 2006, ISBN 3-527-31789-9, S. 107.
- ↑ Albert Tarantola: Periodic Table of the Elements (Janet form). In: ipgp.fr. 23. September 2002, abgerufen am 2. Januar 2013 (englisch).
- ↑ Periodensystem einmal anders. In: welsch.com. 2002, archiviert vom am 14. Oktober 2016; abgerufen am 6. März 2019.
- ↑ Das andere Periodensystem. In: per-table.com. Archiviert vom am 18. November 2013; abgerufen am 3. Mai 2013.
- ↑ Elemente anders ordnen: Konkurrenz für das Periodensystem: Elemente anders ordnen: Konkurrenz für das Periodensystem, abgerufen am 28. März 2021
- ↑ Zahed Allahyari, Artem R. Oganov: Nonempirical Definition of the Mendeleev Numbers: Organizing the Chemical Space. In: The Journal of Physical Chemistry C. Band 124, Nr. 43, 2020, ISSN 1932-7447, S. 23867–23878, doi:10.1021/acs.jpcc.0c07857.


 French
French Deutsch
Deutsch