Хлорметин — Википедия
| Хлорметин | |
|---|---|
| Chlormethinum | |
 | |
| Химическое соединение | |
| ИЮПАК | 2-хлоро-N-(2-хлорэтил)-N-метил-этанамин |
| Брутто-формула | C5H11Cl2N |
| Молярная масса | 156,055 г/моль |
| CAS | 51-75-2 |
| PubChem | 4033 |
| DrugBank | APRD00249 |
| Состав | |
| Классификация | |
| АТХ | L01AA05 |
| Фармакокинетика | |
| Биодоступн. | 100 % |
| Метаболизм | Быстро гидролизуется и деметилируется в плазме крови |
| Период полувывед. | менее 1 минуты |
| Экскреция | почечная, в основном в виде метаболитов, менее 0,01 % введённой дозы экскретируется в неизменённом виде |
| Другие названия | |
| Mustargen, Embichin | |
Хлорметин (лат. Chlormethinum, англ. chlormethine, BAN chlormethine) — исторически первый цитостатический препарат алкилирующего типа, производное бис-β-хлорэтиламина, азотистый аналог иприта.
В США хлорметин также известен как мехлоретамин (mechlorethamine), что, однако, не является зарегистрированным USAN именем, и мустин (mustine), газ HN2, азотистый иприт HN2 (nitrogen mustard HN2) или просто HN2, а также под торговой маркой Мустарген (Mustargen), в странах бывшего СССР известен также как эмбихин
История открытия хлорметина
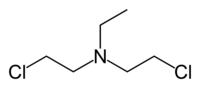
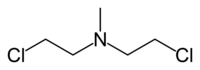
[править | править код]Изначально азотистые иприты, или азотистые аналоги иприта, азотистые аналоги горчичного газа были известны как группа органических веществ общей формулы R-N-(СН2-СН2-Сl)2, где R = либо СН3-, либо С2Н5-, либо -СН2-СН2-Сl. Интерес к этим веществам изначально был обусловлен возможностью их военного применения в качестве потенциального химического оружия. По общеядовитому и сильному кожно-нарывному действию эти соединения аналогичны "обычному" иприту (сернистому иприту). Однако впоследствии некоторые из азотистых аналогов иприта (азотистых ипритов) нашли совершенно иное применение — в качестве противоопухолевых цитостатических препаратов.
Американские фармакологи Луис Гудман и Альфред Гилман исследовали три различных азотистых аналога иприта в качестве потенциальных лечебных агентов — так называемые «газ HN1», «газ HN2» и «газ HN3». Показавший наилучшее соотношение эффективность / токсичность «газ HN2» в итоге и стал лекарством, ныне известным как хлорметин, мехлоретамин, мустин или мустарген.
 |  |  |
До начала использования алкилирующих агентов в химиотерапии злокачественных опухолей, многие из них были уже известны в качестве «горчичного газа» (иприта и его аналогов), использовавшихся в качестве химического оружия кожно-нарывного типа во время Первой Мировой войны. Азотистые аналоги иприта были исторически первыми алкилирующими агентами, использовавшимися в медицине, и первыми примерами современной химиотерапии злокачественных опухолей. Гудман, Гилман и их коллеги в Йельском университете начали изучать азотистые аналоги иприта в 1942 году. И вскоре после обнаружения того факта, что введение этих агентов иногда приводит к значительному уменьшению и даже полному исчезновению экспериментальных злокачественных опухолей у лабораторных мышей, эти химиотерапевтические агенты были впервые протестированы на людях в конце этого же года. Использование «газа HN2» — метил-бис-(β-хлорэтил)-амина гидрохлорида (позже ставшего известным как хлорметин, он же мехлоретамин, или мустин, мустарген, эмбихин) и «газа HN3» — трис-(β-хлорэтил)-амина гидрохлорида для химиотерапевтического лечения запущенных случаев лимфогранулематоза, лимфомы и лимфосаркомы, лейкозов и других злокачественных опухолей, особенно гематологических у пациентов-добровольцев часто приводило к быстрому уменьшению или даже временному полному исчезновению опухолевых масс. Однако потом с неизбежностью возникали рецидивы, причём уже с устойчивостью к хлорметину («газу HN2») и к «газу HN3». Ввиду высокой степени секретности, окружавшей эти разработки, как и всё, связанное с исследованиями в области боевых отравляющих веществ, результаты исследований Гудмана и Гилмана о противоопухолевой активности мехлоретамина и «газа HN3» не были опубликованы вплоть до 1946 года.[1] Эти публикации вызвали взрыв энтузиазма в среде онкологов и резкий рост интереса к прежде не существовавшей области химиотерапевтического лечения злокачественных опухолей человека.
В последующие 25 лет после публикации Гудмана и Гилмана о противоопухолевой активности хлорметина («газа HN2») и «газа HN3» были синтезированы десятки новых алкилирующих химиопрепаратов, обладавших заметно меньшей токсичностью (в частности, меньшей гематологической токсичностью, меньшей способностью вызывать выраженную миелосупрессию) и более широким спектром противоопухолевого действия. В частности, многие из вновь синтезированных алкилирующих агентов оказались применимы не только при гемобластозах, но и при различных солидных злокачественных опухолях. К таким удачным разработкам относятся, например, мелфалан и циклофосфамид, сохранившие своё значение и широко применяемые в химиотерапии злокачественных новообразований и по сей день.[2]
Распространённый миф утверждает, что якобы Гудману и Гилману пришло в голову (или было предложено их начальством из Йельского университета) изучить потенциальную пригодность азотистых аналогов иприта в качестве возможных средств для химиотерапии злокачественных новообразований после того, как в 1943 году случился инцидент в Италии, в городе Бари, где выжившие после воздействия «горчичного газа» солдаты и мирные жители длительное время страдали от выраженной лейкопении. Однако на самом деле эксперименты по химиотерапевтическому лечению злокачественных опухолей с помощью азотистых аналогов иприта, сначала на животных, а затем и на добровольцах-людях, начались за год до события в Бари, в 1942 году. Гилман не упоминает об эпизоде в Бари как об имевшем какое-либо значение или оказавшем какое-либо влияние на их с Гудманом научные изыскания по противоопухолевой активности азотистых аналогов иприта, хотя он, несомненно, знал об этом эпизоде.[3] А способность иприта вызывать выраженную лейкопению, миелосупрессию и иммуносупрессию была известна задолго до опытов Гудмана и Гилмана, ещё с 1919 года, со времён окончания Первой Мировой войны.[2]
Фармакологическое действие
[править | править код]Высокотоксичный и высокоактивный цитостатический препарат алкилирующего типа, с преимущественной активностью в отношении лейкозных клеток и сравнительно малой активностью в отношении клеток солидных опухолей.
Показания
[править | править код]Препарат бывает эффективен при остром и хроническом миело- и лимфолейкозе, лимфо- и ретикулосаркоме, лимфогранулематозе, грибовидном микозе, отчасти при мелкоклеточном раке лёгкого.
В настоящее время его применяют в основном при лечении лимфогранулематоза в системе комплексной терапии. В терапии других опухолей и гемобластозов практически не применяется, так как не имеет преимуществ перед более современными, более эффективными и менее токсичными цитостатиками. В России в качестве лекарственного средства на данный момент не зарегистрирован.
Способ применения и дозы
[править | править код]Вводят мехлоретамин внутривенно. При ударной методике вводят в течение 4 дней в общей дозе 0,4 мг/кг (по 0,1 мг/кг в день) или 0,4 мг/кг однократно. Иногда пользуются дробнопротяжной методикой: препарат вводят в дозе 5 — 6 мг три раза в неделю; общая доза (за 8 — 20 введений) составляет 40 — 120 мг.
Лечение прекращают при снижении содержания лейкоцитов в крови до 2,5 — 3 х 10^9/л.
Мехлоретамин можно вводить также в серозные полости (0,2 мг/кг в 10 — 50 мл изотонического раствора натрия хлорида) при наличии в них выпота, содержащего опухолевые клетки.
Лечение мехлоретамином должно проводиться под тщательным врачебным наблюдением.
При применении препарата могут возникнуть осложнения и побочные явления, связанные с его местными раздражающими свойствами и общим токсическим действием, особенно влиянием на гемопоэз.
При внутривенном введении мехлоретамина следует тщательно следить за тем, чтобы раствор не попал под кожу, так как возможно появление инфильтрата и некроза ткани. Рекомендуется капельное введение сильно разбавленных растворов мехлоретамина через венозный катетер большого диаметра, установленный в центральной вене (например, подключичной). Струйное введение также лучше производить в центральную, а не периферические вены.
В случае попадания раствора в подкожную жировую клетчатку следует немедленно ввести в это место большое количество изотонического раствора натрия хлорида. При возникновении инфильтрата применяют компрессы.
Следует очень остерегаться попадания растворов препарата на слизистые оболочки и кожу больного и медицинского персонала. Если это произошло, необходимо немедленно тщательно смыть препарат большим количеством воды.
Перед введением мехлоретамина обязательна противорвотная премедикация одним из препаратов группы сетронов, дексаметазоном и метоклопрамидом.
В процессе лечения мехлоретамином необходимо следить за изменениями картины крови. Серьёзным осложнением при передозировке препарата может быть глубокое угнетение функции костного мозга с резким подавлением гемопоэза, вплоть до явлений аплазии кроветворной ткани (с летальным исходом).
При лечении дробными дозами мехлоретамина влияние на лейко- и тромбоцитопоэз выражено в меньшей степени.
Примечания
[править | править код]- ↑ Goodman L.S., Wintrobe M.M., Dameshek W., Goodman M.J., Gilman A.Z., McLennan M.T. Nitrogen mustard therapy (англ.) // JAMA. — 1946. — Vol. 132, no. 3. — P. 126—132. — doi:10.1001/jama.1946.02870380008004.
- ↑ 1 2 Scott R.B. Cancer chemotherapy--the first twenty-five years (англ.) // Br Med J. : journal. — 1970. — Vol. 4, no. 5730. — P. 259—265. — doi:10.1136/bmj.4.5730.259. — PMID 4319950. — PMC 1819834.
- ↑ Gilman A. The initial clinical trial of nitrogen mustard (неопр.) // Am J Surg.. — 1963. — Т. 105, № 5. — С. 574—578. — doi:10.1016/0002-9610(63)90232-0. — PMID 13947966.
Для улучшения этой статьи желательно:
|


 French
French Deutsch
Deutsch