Оксид марганца(IV) — Википедия
| Оксид марганца(IV) | |||
|---|---|---|---|
| |||
 | |||
| Общие | |||
| Систематическое наименование | Диоксид марганца | ||
| Хим. формула | |||
| Физические свойства | |||
| Состояние | черные тетрагональные кристаллы | ||
| Молярная масса | 86,9368 г/моль | ||
| Плотность | 5,026 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • разложения | 535 °C | ||
| Энтальпия | |||
| • образования | -521,5 кДж/моль | ||
| Химические свойства | |||
| Растворимость | |||
| • в воде | нерастворим | ||
| Классификация | |||
| Рег. номер CAS | [1313-13-9] | ||
| PubChem | 14801 | ||
| Рег. номер EINECS | 215-202-6 | ||
| SMILES | |||
| InChI | |||
| RTECS | OP0350000 | ||
| ChEBI | 136511 | ||
| Номер ООН | 1479 | ||
| ChemSpider | 14117 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Окси́д ма́рганца(IV) (диокси́д марганца) — порошок тёмно-коричневого цвета, нерастворимый в воде. Наиболее устойчивое соединение марганца, широко распространённое в земной коре (минерал пиролюзит).
Химические свойства
[править | править код]При обычных условиях диоксид марганца ведет себя довольно инертно. При нагревании с кислотами проявляет окислительные свойства, например, окисляет концентрированную соляную кислоту до хлора:
- .
С серной и азотной кислотами разлагается с выделением кислорода:
- .
При взаимодействии с сильными окислителями диоксид марганца окисляется до соединений и :
- .
Диоксид марганца проявляет амфотерные свойства. Так, в концентрированных сернокислых растворах образует сульфат марганца(IV):
- .
А при сплавлении с щелочами и основными оксидами MnO2 выступает в роли кислотного оксида, образуя соли — манганиты:
- .
Является катализатором разложения пероксида водорода:
- .
При нагревании выше 530 °C разлагается:
- .
Получение
[править | править код]В лабораторных условиях получают термическим разложением перманганата калия с образованием манганата калия и кислорода:
- .
Также можно получить реакцией перманганата калия с пероксидом водорода. На практике образовавшийся каталитически разлагает пероксид водорода, вследствие чего реакция до конца не протекает:
- .
При температуре выше 100 °C восстановлением перманганата калия водородом:
- .
Структура
[править | править код]Известны несколько полиморфных модификаций диоксида марганца и его гидратированных форм. Диоксид марганца, как и многие другие диоксиды, имеет кристаллическую структуру рутила (пиролюзит, или ), где атомы металла занимают центры октаэдров, а координационное число атомов кислорода равно трём. Для диоксида марганца характерен недостаток кислорода, его нестехиометричный состав достигается за счет вакансий в подрешетке кислорода. У α-модификации диоксида марганца очень открытая структура, содержащая «каналы», в которых могут размещаться атомы некоторых металлов, например, серебра или бария. , вслед за структурно родственным минералом, часто называют голландитом.
Археология
[править | править код]- Красящие вещества, обнаруженные во время раскопок в пещере Ласко и образцы, взятые с некоторых наскальных изображений, соответствовали диоксиду марганца[1].
- Учёные определили, что кусочки чёрных камней из пещеры Пеш-де-Лазе на юге Франции, состоят из диоксида марганца. Возможно, неандертальцы использовали этот минерал в качестве окислителя и катализатора реакций окисления и горения[2].
Применение
[править | править код]- Применяется для промышленного производства марганца;
- Деполяризатор в марганец-цинковых элементах питания;
- Компонент минеральных пигментов;
- Осветлитель стекла.
Примечания
[править | править код]- ↑ Chalmin E., Menu M., Pomiès M.-P., Vignaud C., Aujoulat N. et Geneste J.-M. Les blasons de Lascaux // L’Anthropologie, 2004. T. 108. Р. 571—592.
- ↑ Неандертальская химия. Дата обращения: 7 марта 2016. Архивировано 7 марта 2016 года.
Литература
[править | править код]- Ахметов Н. С. «Общая и неорганическая химия» М.: Высшая школа, 2001
- Неорганическая химия под редакцией Ю. Д. Третьякова; Химия переходных элементов Кн. 1
- П. З. Пиролюзит // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1898. — Т. XXIIIA (46): Петропавловский — Поватажное. — С. 653—654.
- Полианит // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1906. — Т. доп. II. — С. 436.


 French
French Deutsch
Deutsch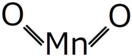










![{\displaystyle {\ce {2H2O2 ->[{\ce {MnO2}}] 2H2O + O2 ^}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d5749fd006a0947b039e50e20e2339e7ee3920a5)
![{\displaystyle {\ce {4MnO2->[530^{\circ }{\text{C}}]2Mn2O3\ +O2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4cc98b0e098d6602bedf8aeffdc1b4802c3e3d32)
![{\displaystyle {\ce {2KMnO4->[t] K2MnO4 \ + MnO2\ + O2 ^}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/71d25bdf5e2f21ee55cabe6ee974cb287b9a46da)

![{\displaystyle {\ce {2KMnO4 + 2H2 ->[t] K2MnO4 + MnO2 + 2H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b819e0305585cf3317d42c32e784309790ef2cce)

