Bendamustyna – Wikipedia, wolna encyklopedia
| |||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||
| Wzór sumaryczny | C16H21Cl2N3O2 | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa | 358,26 g/mol | ||||||||||||||||||||||||||||||||
| Wygląd | ciało stałe | ||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||
| DrugBank | |||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||
| Klasyfikacja medyczna | |||||||||||||||||||||||||||||||||
| ATC | |||||||||||||||||||||||||||||||||
| Stosowanie w ciąży | kategoria D[4] | ||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
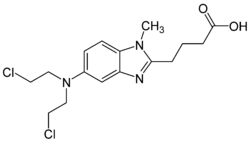
Bendamustyna (łac. bendamustinum) – wielofunkcyjny organiczny związek chemiczny, pochodna benzimidazolu zawierająca m.in. ugrupowanie typu iperytu azotowego. Stosowana jako lek cytostatyczny w leczeniu przewlekłej białaczki limfatycznej, szpiczaka mnogiego oraz chłoniaków nieziarniczych.
Mechanizm działania
[edytuj | edytuj kod]Bendamustyna poprzez alkilowanie uszkadza DNA, hamując podział komórek nowotworowych oraz prowadząc do ich apoptozy[6][7].
Zastosowanie
[edytuj | edytuj kod]- przewlekła białaczka limfocytowa (stadium choroby B lub C według klasyfikacji Bineta), jako leczenie pierwszego rzutu u chorych, u których chemioterapia skojarzona z fludarabiną jest niewskazana[5]
- chłoniaki nieziarnicze o powolnym przebiegu, jako monoterapia u pacjentów, u których progresja choroby nastąpiła w trakcie lub przed upływem 6 miesięcy od zakończenia leczenia rytuksymabem lub schematem zawierającym rytuksymab[5]
- szpiczak mnogi (stadium II z progresją lub stadium III według klasyfikacji Durie-Salmon, jako leczenie pierwszego rzutu) w skojarzeniu z prednizonem u pacjentów w wieku powyżej 65 lat, którzy nie spełniają kryteriów do zabiegu autologicznego przeszczepienia komórek macierzystych oraz którzy w momencie rozpoznania mają objawy istotnej klinicznie neuropatii, uniemożliwiającej zastosowanie leczenia zawierającego talidomid lub bortezomib[5]
Bendamustyna znajduje się na wzorcowej liście podstawowych leków Światowej Organizacji Zdrowia (WHO Model Lists of Essential Medicines) (2017)[8].
Bendamustyna jest dopuszczona do obrotu w Polsce (2018)[9].
Działania niepożądane
[edytuj | edytuj kod]Bendamustyna może powodować następujące działania niepożądane u ponad 10% pacjentów: zakażenie, leukopenia, małopłytkowość, nudności, wymioty, zapalenie błony śluzowej, osłabienie, gorączka, zmniejszenie poziomu hemoglobiny, zwiększenie stężenia kreatyniny oraz mocznika w osoczu[5].
Przypisy
[edytuj | edytuj kod]- ↑ W. Werner, G. Letsch, W. Ihn, Hydrolysis products of the cancerostatic drug Cytostasan® (Bendamustin), „Pharmazie”, 42 (4), 1987, s. 272–273.
- ↑ a b Bendamustine hydrochloride hydrate (nr B5437) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski. [dostęp 2018-07-12]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Bendamustine hydrochloride hydrate (nr B5437) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. [dostęp 2018-07-12]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Drugs and Supplements Bedaquiline (Oral Route) [online], Mayo Foundation for Medical Education and Research, 1 marca 2017 [dostęp 2018-07-12] [zarchiwizowane z adresu 2015-05-24] (ang.).
- ↑ a b c d e f g Lynetoril, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji – Charakterystyka Produktu Leczniczego [online], Centrum Systemów Informacyjnych Ochrony Zdrowia Rejestr Produktów Leczniczych [dostęp 2018-07-12].
- ↑ a b Jan K. Podlewski, Alicja Chwalibogowska-Podlewska, Leki współczesnej terapii online [online], Medical Tribune Polska [dostęp 2018-07-12].
- ↑ Jan K. Podlewski, Alicja Chwalibogowska-Podlewska, Leki współczesnej terapii, t. 1, Warszawa: Medical Tribune, 2010, s. 86, ISBN 978-83-60135-94-5.
- ↑ WHO Model List of Essential Medicines 20th List [online], Światowa Organizacja Zdrowia, 2017, s. 26 [dostęp 2018-07-12] (ang.).
- ↑ Obwieszczenie Prezesa Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych z dnia 16 kwietnia 2018 r. w sprawie ogłoszenia Urzędowego Wykazu Produktów Leczniczych Dopuszczonych do Obrotu na terytorium Rzeczypospolitej Polskiej [online], Dziennik Urzędowy Ministra Zdrowia, 16 kwietnia 2018 [dostęp 2018-07-12] [zarchiwizowane z adresu 2019-11-23].


 French
French Deutsch
Deutsch