Carbon
| Carbon | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Grafitul (stânga) și diamantul (dreapta), doi dintre cei mai cunoscuți alotropi ai carbonului | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Liniile spectrale ale carbonului | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Informații generale | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nume, Simbol, Număr | Carbon, C, 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serie chimică | nemetale | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupă, Perioadă, Bloc | 14, 2, p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densitate | 2267 kg/m³ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Culoare | negru | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Număr CAS | 7440-44-0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietăți atomice | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masă atomică | 12,0107 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rază atomică | 70 (67) pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rază de covalență | 77 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rază van der Waals | 150 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configurație electronică | [He] 2s2 2p2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electroni pe nivelul de energie | 2, 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Număr de oxidare | -4, 0, +2, +4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxid | acid slab | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Structură cristalină | hexagonală | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietăți fizice | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fază ordinară | solid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punct de topire | 3550°C; 3823.15 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punct de fierbere | 4827°C; 5100.15 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energie de fuziune | n/a kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energie de evaporare | 355,8 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volum molar | 5,29×10-6 m³/kmol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Presiune de vapori | ? | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Viteza sunetului | 18.350 m/s la 20 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Informații diverse | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegativitate (Pauling) | 2,55 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacitate termică masică | 710 J/(kg·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivitate electrică | 61×103 S/m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivitate termică | 129 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Prima energie de ionizare | 1086,5 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 2-a energie de ionizare | 2352,6 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 3-a energie de ionizare | 4620,5 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 4-a energie de ionizare | 6222,7 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 5-a energie de ionizare | 37.831,1 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 6-a energie de ionizare | 47.277,0 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 7-a energie de ionizare | {{{potențial_de_ionizare_7}}} kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 8-a energie de ionizare | {{{potențial_de_ionizare_8}}} kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 9-a energie de ionizare | {{{potențial_de_ionizare_9}}} kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A 10-a energie de ionizare | {{{potențial_de_ionizare_10}}} kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cei mai stabili izotopi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unitățile SI și condiții de temperatură și presiune normale dacă nu s-a specificat altfel. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modifică text | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Carbonul (din latină: carbo, „cărbune”) este un element chimic cu simbolul C și numărul atomic 6. Este un element nemetalic tetravalent, ceea ce înseamnă că poate forma legături covalente prin punerea în comun a patru electroni. În natură sunt răspândiți trei izotopi, 12C și 13C fiind stabili, iar 14C este un izotop radioactiv cu un timp de înjumătățire de aproximativ 5.730 de ani.[1] Carbonul este unul dintre puținele elemente cunoscute din antichitate.[2]
Carbonul este al 15-lea cel mai abundent element din scoarța terestră, și al patrulea cel mai răspândit element din univers după masă, primele fiind hidrogenul, heliul și oxigenul. Răspândirea naturală mare a carbonului, diversitatea specifică a compușilor săi organici și abilitatea sa unică de a forma polimeri la temperaturi terestre i-au permis carbonului să fie elementul chimic comun al lumii vii. Este al doilea cel mai abundent element din corpul uman, după oxigen, reprezentând aproximativ 18,5% în procente de masă.[3]
Atomii de carbon se pot lega între ei în diferite moduri, formând alotropii carbonului. Cele mai cunoscute exemple de alotropi sunt grafitul, diamantul și fulerenele.[4] Proprietățile fizice ale carbonului variază mult în funcție de aceste forme alotropice. De exemplu, grafitul este negru, moale și opac, în timp ce diamantul este transparent și extrem de dur (mai exact, cel mai dur material natural cunoscut). Grafitul este un bun conductor electric, în timp ce diamantul are o conductivitate electrică scăzută. În condiții normale de temperatură și presiune, diamantul, nanotuburile de carbon și grafenul sunt materialele cu cea mai mare stabilitate termodinamică cunoscută. În aceste condiții, toți alotropii carbonului sunt materiale solide, grafitul fiind cel mai stabil termodinamic. Sunt puțin reactivi, de aceea au nevoie de temperatură ridicată chiar și pentru a reacționa cu oxigenul.
Cel mai întâlnit număr de oxidare al carbonul este +4 și se regăsește în compușii anorganici, în timp ce +2 se regăsește în monoxidul de carbon și în complecșii carbonilici ai metalelor tranziționale. Cele mai mari surse naturale de carbon anorganic sunt calcarul, dolomitul și dioxidul de carbon, iar majoritatea carbonului se găsește în materiile organice, în depozitele de cărbune, turbă, petrol și clatrați de metan. Carbonul formează un număr mare de compuși chimici, mai mulți decât orice alt elemente, existând aproximativ zece milioane de compuși descriși până în prezent,[5] acest număr fiind mic în comparație cu numărul teoretic de compuși posibili pe care carbonul îi poate forma. Din acest motiv, carbonul a fost numit și „regele elementelor”.[6]
Istoric
[modificare | modificare sursă]
Carbonul a fost descoperit încă din Preistorie și a fost cunoscut în forma sa alotropică de cărbune încă din cele mai îndepărtate timpuri, anume la începutul civilizațiilor umane. O altă formă a sa, diamantul, a fost cel mai probabil cunoscut începând cu anii 2500 î.Hr. în China, în timp ce cărbunele era fabricat în perioada romană prin aceeași metodă folosită și în prezent.[7][8]
În 1722, René-Antoine Ferchault de Réaumur a demonstrat că fierul putea fi transformat în oțel prin absorbția unei anumite substanțe, iar ulterior s-a înțeles că aceasta era de fapt carbonul.[9] În 1772, Antoine Lavoisier a arătat că diamantele reprezintă o formă rară de carbon; acesta a ars bucăți de cărbune și de diamant și a ajuns la concluzia că niciuna dintre ele nu a eliminat apă (deci nu conțineau hidrogen), însă ambele au eliminat aceeași cantitate de dioxid de carbon per gram. În 1779,[10] Carl Wilhelm Scheele a demonstrat că grafitul, despre care se credea că este o formă de plumb, era de fapt identic din punct de vedere chimic cu cărbunele, dar cu o mică cantitate de fier, întrucât prin tratarea cu un amestec de acid azotic se obținea dioxid de carbon.[11] În 1786, savanții francezi Claude Louis Berthollet, Gaspard Monge și C. A. Vandermonde au confirmat faptul că grafitul era în majoritate alcătuit din carbon, oxidându-l cu oxigen prin aceeași metodă folosită mai devreme de Lavoisier pentru diamant.[12] De asemenea, în urma arderii a rămas un reziduu de fier, despre care savanții au crezut că era necesar pentru structura grafitului. În lucrarea publicată, aceștia au propus numele de carbon (latină carbonum) pentru elementul constituent al grafitului, care elimina gazul de dioxid de carbon prin încălzire. Ulterior, Antoine Lavoisier a introdus carbonul în lista de elemente chimice în cartea sa din 1789.[13] O formă alotropică relativ nouă a carbonului, fulerenele, a fost descoperită mai recent, în 1985[14], și include forme nanostructurale precum Buckminsterfullerenele și nanotuburile de carbon.[15] Savanții care au descoperit fulerenele, Robert Curl, Harold Kroto și Richard Smalley, au primit Premiul Nobel pentru Chimie în anul 1996.[16] Rezultatele au dus treptat la mărirea interesului legat de noile forme ale carbonului, iar recent au fost descoperiți alotropi „exotici”, precum carbonul sticlos sau grafenele.[17]
Etimologie
[modificare | modificare sursă]Denumirea de carbon provine din termenul francez charbone, care, la rândul său, provine din latinescul carbo, care înseamnă cărbune.[18] O adaptare interesantă pentru denumirea elementului este întâlnită în limba germană, daneză și olandeză, unde Kohlenstoff, kulstof și koolstof înseamnă, literal, „substanță de cărbune”.
Structură atomică
[modificare | modificare sursă]
Carbonul este cel de-al șaselea element chimic din Sistemul periodic al elementelor, și are în forma sa fundamentală următoarea configurație electronică: 1s22s22p2. Se poate remarca faptul că cei patru electroni din stratul 2 sunt electronii de valență ai elementului. Razele covalente ale carbonului sunt de obicei considerate a fi 77,2 pm (C–C), 66,7 pm (C=C) și respectiv 60,3 pm (C≡C), deși acestea pot varia în funcție de numărul de coordinare și de atomul de care se leagă carbonul. În general, raza covalentă descrește cu scăderea numărului de coordinare și cu creșterea ordinului de legătură.[19]
Prin apartenența sa la perioada a doua, carbonul este singurul element din grupa a 14-a care este capabil să fie hibridizat sp2 și sp, dând naștere la legături duble (sigma-pi) și la legături triple (sigma-2pi), spre deosebire de restul elementelor din grupă. În combinațiile carbonului cu numărul de coordinare 4, cei patru orbitali din configurația fundamentală hibridizează, formând patru orbitali echivalenți sp3.[20]
Carbonul formează aproape în totalitate patru legături chimice cu alți atomi, în special în compușii organici, conferindu-i geometria specifică tetraedrică,[21] totuși au fost întâlnite excepții. În 2016, a fost confirmat faptul că hexametilbenzenul conține un atom de carbon ce formează șase legături, față de numărul obișnuit de patru.[22]
Proprietăți fizice
[modificare | modificare sursă]
Printre formele alotropice diferite ale carbonului se numără una dintre cele mai moi substanțe cunoscute, anume grafitul, și cea mai dură substanță întâlnită în natură, anume diamantul. Carbonul este un element remarcabil din mai multe motive, unul dintre acesta fiind capacitatea deosebită de a forma legături chimice cu alți atomi mici, incluzând atomii de carbon, iar mărimea sa îl face capabil de a forma legături covalente multiple cu atomi multivalenți. Datorită acestor proprietăți, carbonul poate forma aproape zece milioane de compuși chimici diferiți, majoritatea compușilor care există.[5] De asemenea, carbonul are cel mai mare punct de sublimare dintre toate elementele. La presiunea atmosferică, nu are niciun punct de topire, iar punctul triplu este la 10,8 ± 0,2 MPa și 4.600 ± 300 K (~4,330 °C),[23][24] așadar sublimează la aproximativ 3.900 K.[25][26]
Carbonul sublimează într-un arc de carbon ce are o temperatură de aproximativ 5.530 °C. Astfel, el rămâne solid la temperaturi mai înalte decât cele mai mari puncte de topire ale metalelor, precum wolframul sau reniul, indiferent de forma sa alotropică. Deși are din punct de vedere termodinamic o tendință de oxidare, carbonul rezistă la oxidare mai bine decât elemente precum fierul sau cuprul, care sunt agenți reducători mai slabi la temperatura camerei.
Valorile pentru primele patru energii de ionizare ale carbonului, 1086,5 kJ/mol, 2352,6 kJ/mol, 4620,5 kJ/mol și 6222,7 kJ/mol, sunt cu mult mai mari decât în cazul celorlalte elemente mai grele din grupa a 14-a. Electronegativitatea carbonului este 2,5, cu mult mai mare decât a elementelor mai grele din aceeași grupă, a căror electronegativitate variază între 1,8 și 1,9, dar destul de apropiată de cea a nemetalelor vecine și de a unor metale tranziționale din perioadele 5 și 6.
Cele mai reprezentative proprietăți fizice extreme ale formelor alotropice ale carbonului au fost aranjate în tabelul de mai jos:
| Grafitul este unul dintre cele mai moi materiale cunoscute. | Diamantul nanocristalin sintetic este cel mai dur material cunoscut.[27] |
| Grafitul este un lubrifiant foarte bun, fiind un superlubrifiant.[28] | Diamantul este unul dintre cele mai bune abrazive. |
| Grafitul este un conductor al electricității.[29] | Diamantul este un izolator electric excelent.[30] |
| Unele forme de grafit sunt utilizate ca și izolator termic, dar unele sunt conductori termici buni. | Diamantul este cel mai bun conductor termic întâlnit în natură. |
| Grafitul este opac. | Diamantul este puternic transparent. |
| Grafitul cristalizează în sistemul hexagonal.[31] | Diamantul cristalizează în sistemul cubic. |
| Carbonul amorf este complet izotrop. | Nanotuburile de carbon sunt printre cele mai anizotrope materiale cunoscute. |
Forme alotropice
[modificare | modificare sursă]Carbonul atomic este o specie chimică cu o durată de viață foarte scurtă, de aceea carbonul, ca și element, se stabilizează prin intermediul unor structuri multi-atomice, cu diferite configurații moleculare, numite alotropi sau forme alotrope. Cele mai cunoscute trei forme alotrope ale carbonului sunt grafitul, diamantul și carbonul amorf. Deși în trecut erau considerate forme exotice, fulerenele sunt în prezent sintetizate în mod comun și utilizate în cercetare; din această clasă fac parte buckminsterfullerenele,[15][32] nanotuburile de carbon,[33], carbon nanobuds („nano-muguri”)[34] și nanofibrele de carbon.[35][36] Alți câțiva alotropi au fost descoperiți, precum lonsdaleitul,[37] carbonul sticlos,[17] nanospuma de carbon[38] și carbonul acetilenic liniar, numit și carbină.[39]
Din 2009, grafenele par a fi cele mai dure sau puternice materiale testate vreodată.[40] Procedeul de separare al grafenei din grafit necesită o viitoare dezvoltare tehnologică, pentru a fi potrivit economic pentru procedee industriale.[41] Dacă cercetările vor fi de succes, grafenele ar putea fi utilizate pentru eventuala construcție a unui lift spațial. De asemenea, o altă utilizare a lor ar putea fi cea de rezervor pentru hidrogen în automobilele care au motoare pe bază de hidrogen.[42]

Forma amorfă a carbonului reprezintă o aranjare a atomilor de carbon într-o stare non-cristalină, neregulată, asemănătoare sticlei, care nu este susținută de o macrostructură cristalină. Are aspectul unei pudre și este constituentul primar al unor substanțe precum: mangalul, funinginea și cărbunele activ. În condiții normale de presiune, carbonul ia forma grafitului, în a cărui structură sunt întâlniți atomi legați între ei prin trei legături, cu o geometrie trigonală, într-un plan compus din nuclee hexagonale fuzionate, asemănătoare ca formă cu nucleele aromatice.[43] Rețeaua atomică rezultată este bidimensională, iar straturile sunt atașate unul deasupra celuilalt prin intermediul forțelor van der Waals slabe. Această structură îi conferă grafitului proprietățile sale de a fi foarte moale și de a cliva ușor (adică straturile bidimensionale se pot despica paralel cu rețeaua structurii). Datorită delocalizării unuia dintre electronii externi la fiecare atom din structură, ceea ce duce la formarea unui nor electronic de tip π, grafitul conduce electricitatea, dar doar în planul fiecărui strat legat covalent. Ca și rezultat, conductivitatea electrică a carbonului va fi mai mică decât cea a majorității metalelor. Delocalizarea electronilor este de asemenea și motivul pentru stabilitatea energetică a grafitului, în comparație cu diamantul, la temperatura camerei.

a) diamant; b) grafit; c) lonsdaleit;
d–f) fulerenele (C60, C540, C70);
g) carbon amorf; h) nanotub de carbon.
La presiuni foarte mari, carbonul trece în forma sa alotropică mult mai compactă, diamantul, care are o densitate aproximativ de două ori mai mare decât grafitul. În cazul acestui alotrop, fiecare atom se leagă de alți patru atomi de carbon, ceea ce induce orientarea tetraedrică a legăturilor, formându-se astfel o rețea tridimensională de nuclee atomice cu șase membri. Diamantul are structura cristalină cubică, aceeași cu a siliciului și germaniului, iar datorită puterii legăturilor carbon-carbon, este cea mai dură substanță întâlnită în natură, având maximul pe scara de duritate Mohs. Deși se spune în popor că „diamantele sunt veșnice”, acestea sunt instabile termodinamic în condiții normale și se transformă astfel în grafit.[4] Datorită unei energii de activare mari, tranziția spre starea de grafit este atât de înceată la temperaturi normale, încât nu poate fi observată. Sub unele condiții, carbonul cristalizează hexagonal sub formă de lonsdaleit, în a cărui structură toți atomii sunt legați covalent, iar proprietățile sale sunt asemănătoare cu cele ale diamantului.[37]
Fulerenele sunt formațiuni cristaline sintetice cu o structură asemănătoare grafitului, dar în locul hexagonelor avem pentagoane, sau câteodată și heptagoane de atomi de carbon. Atomii care lipsesc, sau care sunt în plus față de structura specifică grafenului, sunt motivul pentru care straturile iau forme de sferă, elipsă sau chiar cilindru. Proprietățile fulerenelor nu au fost încă analizate în totalitate și reprezintă un domeniu de interes pentru cercetare în știința nanomaterialelor. Denumirile de „fulerenă” și de „buckminsterfulerenă” provin de la numele lui Richard Buckminster Fuller, savantul care a popularizat conceptul de dom geodezic, care din punct de vedere structural este similar fulerenelor. Buckminsterfulerenele au molecule relativ mari, formate în totalitate din atomi de carbon legați trigonal, cu formă de sferoid. Cel mai simplu exemplu este fulerena C60, cu formă de minge de fotbal).[15] Nanotuburile de carbon sunt similare din punct de vedere structural cu fulerenele, exceptând faptul că fiecare atom este legat trigonal în cadrul unui strat curbat, care formează un cilindru gol la interior.[32][33] Un alotrop nou, carbon nanobuds („nano-muguri”), a fost descoperit în 2007 și este un material hibrid între buckminsterfulenere și nanotuburile de carbon (fulerenele sunt legate covalent de partea externă a unui nanotub), care combină proprietățile ambilor alotropi într-o singură structură.[34]
Proprietăți chimice
[modificare | modificare sursă]
Grafitul este mult mai reactiv decât diamantul, în condiții standard, în ciuda faptului că este mai stabil din punct de vedere termodinamic. Însă acesta este alcătuit dintr-un sistem pi-delocalizat, cu atomii de carbon hibridizați sp2, ceea ce induce o anumită vulnerabilitate. De exemplu, grafitul poate fi oxidat de acidul azotic concentrat la încălzire (acid azotic fumans), cu obținerea acidului melitic, C6(CO2H)6, un acid hexacarboxilic în a cărui structură sunt păstrate unitățile hexagonale ale grafitului.[44][45]
Compușii de carbon reprezintă baza vieții pe Pământ și ciclul carbon - azot produce o parte din energia radiată de Soare și de alte stele. Deși formează o varietate extraordinară de compuși, majoritatea formelor de carbon sunt destul de nereactive în condiții normale. În condiții standard de temperatură și presiune, carbonul este rezistent la acțiunea agenților oxidanți, cu excepția oxidanților puternici. Carbonul nu reacționează cu acidul sulfuric, acidul clorhidric, clorul sau metalele alcaline.
Reacția cu nemetale și oxizi nemetalici
[modificare | modificare sursă]La temperaturi ridicate, carbonul reacționează cu oxigenul formând oxizii de carbon. Monoxidul de carbon se obține prin combinarea carbonului cu o cantitate insuficientă de oxigen, sau prin efectuarea reacției la o temperatură înaltă, la care dioxidul de carbon nu este stabil:[46]
- C(s) + O2(g) → 2 CO(g)
Carbonul reacționează cu sulful pentru a obține sulfură de carbon:
- C(s) + S(s) → CS2(l)
O reacție specifică este reacția de formare a gazului de apă, prin care se suflă aburi (apă în stare gazoasă) printr-un strat de cărbune incandescent, formându-se amestecul de oxizi de carbon și hidrogen gazos:[46]
- C(s) + H2O(g) → CO(g) + H2(g)
Reacția cu metale și oxizi metalici
[modificare | modificare sursă]Carbonul preia oxigenul din oxizii metalici, cu obținerea metalului elementar. Această reacție exotermă este folosită în industria fierului și oțelului pentru obținerea fierului și în vederea controlării conținutului de carbon din oțel:
- Fe
3O
4 + 4 C(s) → 3 Fe(s) + 4 CO(g)
Carbonul se combină cu unele metale și oxizi metalice la temperaturi înalte cu formare de carburi metalice. Un exemplu este carbura de wolfram, un compus utilizat pe larg ca și abraziv și pentru fabricarea unor unelte de tăiat.
Carbura de calciu, numită și carbid, un alt exemplu de carbură importantă din punct de vedere industrial, se obține la nivel industrial prin reducerea varului nestins (oxidul de calciu) cu cărbune de lemn sau cocs, la o temperatură de 2500°C:[47]
- CaO + 3 C → CaC2 + CO
Izotopi
[modificare | modificare sursă]
Izotopii carbonului sunt acele nuclee atomice care conțin șase protoni plus un anumit număr de neutroni (care variază de la 2 la 16). Carbonul are doi izotopi naturali stabili.[1] Izotopul carbon-12 (12C) reprezintă 98,93% din totalitatea carbonului de pe Pământ, iar izotopul carbon-13 (13C) reprezintă restul de 1,07%.[1] Concentrația de 12C este chiar mai mare în materialele biologice, întrucât în cadrul reacțiilor biochimice acest izotop are prioritate față de 13C.[48] În 1961, Uniunea Internațională de Chimie Pură și Aplicată (IUPAC) a adoptat izotopul carbon-12 ca fiind baza pentru masele atomice.[49] Experimentele de identificare a carbonului prin rezonanță magnetică nucleară (RMN) se realizează cu ajutorul izotopului13C.
Carbon-14 sau radiocarbonul (14C) este un radioizotop întâlnit în natură, care se formează în atmosfera superioară (partea inferioară a stratosferei și cea superioară a troposferei) în urma interacției dintre atomii de azot și radiațiile cosmice.[50] Pe Pământ, este întâlnit în cantități extrem de mici, aproximativ o parte la un trilion (0,0000000001%), fiind în majoritate prins în atmosferă și în depozitele de suprafață, în special în turbă și în alte materiale organice.[51] Acest izotop este instabil și se dezintegrează prin emisie β−. Datorită perioadei de înjumătățire relativ scurte, de aproximativ 5730 ani, 14C este absent în rocile antice. Cantitatea de izotop 14C din atmosferă și din organismele vii este oarecum constantă, dar scade în corpurile acestora după moarte. Acest principiu este folosit pentru datarea cu radiocarbon, o metodă inventată în 1949 și folosită pentru determinarea vârstei unor materiale pe bază de carbon, cu condiția ca aceasta să nu depășească aproximativ 40.000 ani.[52][53]
Există aproximativ 15 izotopi cunoscuți ai carbonului, iar cel cu cea mai scurtă durată de viață este 8C, care se dezintegrează prin emisie de protoni și dezintegrare alfa, și are un timp de înjumătățire de 1,98739x10−21 secunde.[54] Izotopul 19C prezintă proprietăți interesante, în sensul că raza sa este cu mult mai mare decât s-a prezis pentru situația în care nucleul său atomic ar fi o sferă cu densitate constantă.[55]
Compuși
[modificare | modificare sursă]Carbonul este elementul capabil să formeze cel mai mare număr de compuși: aproximativ zece milioane de compuși posibili. Întrucât chimia organică este adesea denumită „chimia carbonului”, deoarece aceasta studiază majoritatea compușilor carbonului (în combinație cu hidrogenul și alte elemente), sunt puțini compuși așa-zis anorganici ai carbonului, precum: oxizii de carbon, carbonații, cianurile, cianații, tiocianații, fulminații, precum și acizii corespunzători. De asemenea, mai sunt luate în considerare și carburile.
Compuși organici
[modificare | modificare sursă]

Carbonul are capacitatea de a forma lanțuri sau catene foarte lungi prin legături carbon-carbon. Această proprietate se numește concatenare, și este restrânsă doar la câteva elemente (în afară de carbon, siliciul, borul și azotul). Legăturile carbon-carbon sunt destul de puternice și anormal de stabile. Această caracteristică este importantă deoarece permite carbonului să formeze un număr extrem de mare de compuși; de fapt, există mai mulți compuși chimici care conțin carbon decât toți compușii celorlalte elemente chimice la un loc. [56][57]
Cea mai simplă formă de moleculă organică este hidrocarbura - o familie mare de molecule organice care sunt alcătuite din atomi de hidrogen legați de un lanț de atomi de carbon. Lungimea catenei, catenele laterale (ramificațiile) și grupele funcționale influențează proprietățile moleculelor organice. Cea mai simplă hidrocarbură și, respectiv, cel mai simplu compus organic este metanul.
După natura atomilor din compuși, există două clase majore de compuși organici: hidrocarburile, compuși formați prin saturarea cu hidrogen a catenelor saturate sau nesaturate de carbon și compușii organici cu funcțiuni, o categorie care conține extrem de multe clase de substanțe importante din punct de vedere industrial și biologic, după cum se poate vedea în continuare. Compușii cu funcțiuni simple, monovalente sunt compușii hidroxilici (alcoolii, enolii, fenolii), nitroderivații, derivații halogenați și aminele, compușii cu funcțiuni divalente sunt compușii carbonilici (aldehidele și cetonele), iar compușii cu funcțiuni trivalente sunt acizii carboxilici. De asemenea, există și derivați ai acestor categorii, precum esterii, anhidridele acide, amidele și biomoleculele (proteinele, polizaharidele, lipidele și acizii nucleici), toate acestea având ca element de bază carbonul.[58][59]
Carbonul este răspândit în toate viețuitoare și formele de viață, reprezentând elementul central al chimiei organice. Când se unește cu hidrogenul, se obțin forme variate de hidrocarburi importante din punct de vedere industrial, fiind agenți frigorifici, lubrifianți, solvenți și ca precursori în procesele de fabricație ale materialelor plastice, produselor petrochimice și a combustibililor fosil.
Când se combină cu hidrogenul și oxigenul, carbonul poate forma o mare varietate de categorii de compuși importanți din punct de vedere biologic, printre care se numără zaharidele, chitinele, alcoolii, grăsimile, esterii aromatici, carotenoizii și terpenele. Cu azotul formează alcaloizi, iar prin adăugarea de sulf se obțin antibioticele, aminoacizii și cauciucurile. Prin adăugarea de fosfor la aceste elemente, se obțin acizii nucleici, ADN-ul și ARN-ul, esențiali pentru codificarea informației genetice specifice fiecărei viețuitoare. De asemenea, ATP-ul (adenozintrifosfatul) este cea mai importantă moleculă de transfer și de stocare a energiei din celulele vii.
Compuși anorganici
[modificare | modificare sursă]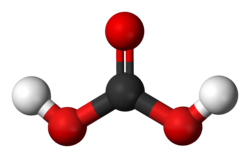
În categoria compușilor anorganici ai carbonului intră acei compuși care sunt asociați cu mineralele și nu conțin hidrogen sau fluor, însă această definiție lasă deschise anumite interpretări. Printre cei mai simpli compuși anorganici ai carbonului se numără oxizii de carbon. Cel mai cunoscut și important oxid al carbonului este dioxidul de carbon (CO2). Este un component minor al atmosferei Pământului, un compus volatil produs și folosit de toate ființele vii, și care era principalul component al paleoatmosferei.[60] Dizolvat în apă formează urme de acid carbonic (H2CO3), dar ca majoritatea compușilor cu mai mulți atomi de oxigen la un singur carbon, acesta este instabil.[61] Totuși, prin acest intermediar, sunt produși ioni carbonat, structuri stabilizate prin rezonanță. Unele minerale importante sunt carbonați, precum calcitul și azuritul. Disulfura de carbon (CS2) are o structură similară.[44]
Celălalt oxid comun al carbonului este monoxidul de carbon (CO), compus ce se formează prin combustia incompletă a carbonului și este un gaz incolor și inodor. Fiecare moleculă conține o legătură triplă, care este foarte puțin polară, rezultând tendința de a se atașa permanent de moleculele de hemoglobină, înlocuind oxigenul și formând carboxihemoglobina. Se poate concluziona astfel că gazul este foarte toxic.[62][63] Ionul cianură (CN-), are o structură similară și se comportă ca un ion halogenură. De exemplu, poate forma cianogenul ((CN)2, zis și dician), cu o structură similară halogenurilor diatomice. Printre ceilalți oxizi mai puțin comuni se numără suboxidul de carbon (C
3O
2),[64] monoxidul de dicarbon, instabil (C2O),[65][66] trioxidul de carbon (CO3),[67][68] ciclopentanpentona (C5O5),[69] ciclohexanhexona (C6O6),[69] și anhidrida melitică (C12O9).
Cu metalele reactive, precum wolframul, carbonul formează fie carburi metalice (C-), fie acetiluri metalice (C22-). De asemenea, formează aliaje cu puncte de topire foarte înalte. Acești anioni sunt astfel asociați cu metanul și acetilena, ambii fiind acizi foarte slabi. Cu o electronegativitate de 2,5,[70] carbonul are o preferință de a forma legături covalente. Unele carburi au matrice covalente, de exemplu carbura de siliciu sau carborundul (SiC), fiind asemănătoare cu diamantul. Totuși, chiar și cele mai polare și saline carburi nu sunt complet ionice.[71]
Compuși organometalici
[modificare | modificare sursă]Prin definiție, compușii organometalici conțin cel puțin o legătură de tipul carbon-metal. Există o varietate largă de astfel de compuși, iar printre principalele clase se numără: compuși simpli alchil-metal (de exemplu, tetraetilplumbul), compuși η2-alchene (de exemplu, sarea lui Zeise) și compuși η3-alil (de exemplu, dimerul clorurii de alilpaladiu); metalocenele sunt acei compuși care conțin liganzi de tip ciclopentadienil (de exemplu, ferocenul). Există mulți carbonilici metalici (de exemplu, tetracabonilul de nichel).
Deși se credea că carbonul formează exclusiv patru legături, a fost recent descoperit un compus complex organometalic ce conține un atom de carbon hexacoordinat, cu geometrie octaedrică. Cationul acestui compus este [(Ph3PAu)6C]2+, cu denumirea hexakis(trifenilfosfanaurio)metan. Se crede că acest fenomen este cauzat de aurofilicitatea pentru liganzii de aur.[72]
În natură
[modificare | modificare sursă]Formarea în stele
[modificare | modificare sursă]Carbonul nu a fost creat în timpul Big Bang-ului, deoarece are nevoie de producerea unei coliziuni triple de particule alfa (nuclee de heliu). Universul s-a extins inițial și apoi s-a răcit prea repede pentru ca acest lucru să fie posibil. Oricum, este produs în interiorul stelelor în ramura orizontală, unde un nucleu de heliu este transformat în carbon prin procesul triplu-alfa. A fost de asemenea creat în stări multi-atomice.
Răspândire
[modificare | modificare sursă]


Carbonul este al patrulea cel mai abundent element din univers după masă, situat în top după hidrogen, heliu și oxigen. Este răspândit în Soare, stele, comete și în atmosfera majorității planetelor.[73] Unii meteoriți conțin diamante microscopice, care s-au format în perioada în care sistemul solar era încă un disc protoplanetar.[74] De asemenea, este posibil ca diamantele microscopice să se fi putut forma datorită presiunii intense și a temperaturilor extrem de ridicate din timpul impacturilor dintre meteoriți.[75]
În 2014, NASA a anunțat publicarea unei baze de date folosită pentru urmărirea hidrocarburilor aromatice policiclice (HAP) din univers. Mai mult de 20% din carbonul din univers poate fi asociat cu aceste HAP, care sunt compuși complecși ai carbonului și hidrogenului, fără oxigen.[76] Acești compuși sunt notabili fiindcă este luată în considerare ipoteza că HAP au avut un rol în abiogeneză și în apariția vieții. Se pare că HAP s-au format la câteva miliarde de ani după Big Bang, fiind foarte răspândite în univers și asociate cu apariția stelelor și cu exoplanetele.[73]
S-a estimat că partea solidă a Pământului conține aproximativ 730 ppm (părți per milion) carbon, cu aproximativ 2000 ppm în nucleu și 120 ppm în manta și în scoarța terestră.[77] Din moment ce masa Pământului este aproximativ 5972×1024 kg, asta implică faptul că ar conține aproximativ 4360 milioane de gigatone de carbon.
În combinație cu oxigenul, mai exact în dioxidul de carbon, carbonul este răspândit în atmosfera terestră (aproximativ 810 gigatone de carbon) și dizolvat în toate elementele hidrologice (aproximativ 36.000 gigatone de carbon). Aproximativ 1.900 gigatone de carbon sunt prezente și în biosferă. De asemenea, și hidrocarburile (precum cărbunele, petrolul și gazele naturale) conțin carbon. Rezervele de cărbune sunt de aproximativ 900 gigatone, iar resursele probabil 18,000 Gt.[78] Rezervele petroliere sunt de aproximativ 150 gigatone. Sursele descoperite de gaze naturale sunt de aproximativ 175 1012 metri cubi (conținând aproximativ 105 gigatone de carbon), dar studiile au estimat alți 900 1012 metri cubi de depozite neconvenționale, precum de gaz de șist, care ar reprezenta aproximativ 540 gigatone de carbon.[79]
Carbonul este de asemenea întâlnit în hidrații de metan din regiunile polare și de pe fundul mărilor. Valorile estimate pentru carbonul din acești compuși este de 500 până la 2500 Gt,[80] sau chiar 3.000 Gt.[81]
În trecut, cantitatea de hidrocarburi la nivel mondial era mult mai mare. Conform unor surse, în perioada dintre anii 1751 și 2008 aproximativ 347 de gigatone de carbon au fost eliberate în atmosferă sub formă de dioxid de carbon, prin arderea combustibililor fosili.[82] Alte surse estimează totalul la 879 Gt, iar cantitatea care face referire la gazele ajunse în atmosferă, oceane și pe pământ (precum în turbării) ajunge la 2.000 Gt.[83]
Carbonul este un constituent a cantității extrem de mare de roci cu conținut de carbonat (aproximativ 12% în procente de masă , printre care se numără: calcarul, dolomitele și marmura. Cărbunele este foarte bogat în carbon (de exemplu, antracitul conține 92–98% carbon)[84] și este cea mai mare sursă comercială de carbon mineral, măsurând 4.000 gigatone și reprezentând 80% din totalul combustibililor fosili.[85]
În ceea ce privește alotropii carbonului, grafitul este întâlnit în cantități mari în Statele Unite (în majoritate în New York și Texas), Rusia, Mexic, Groenlanda și India. Diamantele naturale sunt întâlnite în roca numită kimberlit, din vulcani. Majoritatea depozitelor de diamante sunt răspândite în Africa, în special în Africa de Sud, Namibia, Botswana, Republica Congo și Sierra Leone. De asemenea, au fost întâlnite depozite de diamante și în Arkansas, Canada, zona arctică rusă, Brazilia și Australia de nord și de vest. În prezent, diamantele mai sunt extrase de pe fundul oceanului în zona Capului Bunei Speranțe.
Izotopul carbon-14 se formează în straturile superioare ale troposferei și în stratosferă, la altitudini cuprinse între 9–15 km, în urma unei reacții care este precipitată de radiațiile cosmice.[86] Neutronii termici sunt produșii care se unesc cu nucleul izotopului azot-14, formând carbon-14 și un proton. Astfel, 1,2 × 1010% din dioxidul de carbon atmosferic conține carbon-14.[19]
Asteroizii cu un conținut bogat de carbon sunt relativ răspândiți în părțile exterioare ale centurii de asteroizi și ale sistemului solar. Oamenii de știință încă nu au realizat teste pe eșantioane obținute direct de pe acești asteroizi, însă ei ar putea fi folosiți în viitor pentru mineritul în afara Pământului, o tehnologie care este încă indisponibilă.[87]
Rol biologic
[modificare | modificare sursă]
Carbonul este un element esențial pentru toate formele de viață cunoscute, fiind un micronutrient. Fiind atât de răspândit în aproape toți compușii cu importanță biologică majoră (exceptând sărurile, apa și restul compușilor bioanorganici), carbonul poate fi considerat cel mai important element pentru existența vieții așa cum este ea cunoscută. De la dioxidul de carbon expirat de animale și utilizat de plante și până la macromoleculele complexe, carbonul este elementul de bază, fără de care acești compuși nu ar exista.
Circuitul carbonului
[modificare | modificare sursă]În condițiile naturale de pe Pământ, conversia unui element într-altul este un fenomen foarte rar întâlnit. De aceea, cantitatea de carbon care se află pe Pământ este efectiv constantă. Astfel, procesele care utilizează carbon trebuie să procure de undeva elementul, iar apoi să-l depună într-un anumit loc. Totalitatea acestor schimburi ale carbonului sunt cunoscute sub numele de circuitul carbonului în natură. De exemplu, plantele fotosintetizatoare extrag dioxidul de carbon din atmosferă (sau din apa de mare) și îl folosesc pentru a construi biomasă printr-un proces numit fixarea carbonului. O parte din această biomasă este consumată de către animale ca parte a lanțului trofic, iar o altă cantitate de carbon este eliminată înapoi în atmosferă prin expirarea dioxidului de carbon de către acestea. Totuși, circuitul carbonului este mult mai complicat decât atât, deoarece în transportul acestui element sunt implicate și elementele abiotice. De exemplu, o parte din dioxidul de carbon se dizolvă în oceane, iar dacă bacteriile nu îl consumă, atunci plantele sau animalele moarte se pot transforma în timp în petrol sau cărbune, care eliberează carbonul prin ardere.[88][89]
Obținere
[modificare | modificare sursă]Preparare în laborator
[modificare | modificare sursă]Producția la scară industrială
[modificare | modificare sursă]Carbonul este răspândit în natură în stare elementară în cele două forme alotropice: grafitul și diamantul, fiind deci minat direct din zonele în care aceste minerale se găsesc, deci nu este nevoia neapărată a unor reacții chimice industriale pentru producerea acestuia. Se mai poate consideră, în anumite circumstanțe, și cărbunele ca o sursă importantă de carbon, deși procentul este mai mic decât în cazul celor două forme pure. Totuși, negrul de fum, o varietate tehnică de cărbune negru, sub formă de cenușă, se poate produce la nivel industrial prin arderea cu aer insuficient a unor gudroane de cărbuni, a unor fracțiuni grele de petrol, a acetilenei sau a metanului, după cum urmează:[90]

- C2H2 + O½ → 2 C + H2O
- CH4 + O2 → C + 2H2O
Grafitul
[modificare | modificare sursă]Depozite valoroase de grafit (numit și plombagină) se găsesc în multe zone ale lumii, însă cele mai importante din punct de vedere economic se situează în China, India, Brazilia și Coreea de Nord. Depozitele de grafit sunt de origine metamorfică, fiind întâlnite în asociație cu cuarțul, mica sau feldspații în șisturi, gnaisul și gresia și calcarul metamorfozat sub formă de lentile sau filoane în pegmatite, câteodată cu o grosime de un metru sau chiar mai mare. În rocile metamorfice bogate în surse de carbon, depozitele de grafit s-au format pe măsură ce materialul organic din calcar a fost alterat de căldură și presiune.[91][92] Depozitele de grafit din Borrowdale, Cumberland, Anglia erau în trecut de o puritate atât de ridicată și atât de mari încât, până în secolul al XIX-lea, creioanele erau realizate prin simpla atașare a lemnului asupra minelor de grafit, care erau direct tăiate din blocurile de grafit.[93]
Grafitul apare în natură sub diferite forme: poate fi cristalin (extrem de rar), amorf, granular, sau stratificat. Grafitul amorf este cel mai abundent și cel cu calitatea cea mai scăzută. Deși este denumit „amorf”, această denumire a grafitului face referire de fapt la o formă ce conține cristale foarte mici și este folosit pentru fabricarea unor produse cu valoare scăzută. Depozite mari de grafit amorf sunt situate în China, Europe, Mexic și Statele Unite.[93]
Conform USGS, producția la nivel mondial de grafit natural în anul 2010 era de 1,1 milioane de tone, dintre care China a contribuit cu 800.000 t, India cu 130.000 t, Brazilia cu 76.000 t, Coreea de Nord cu 30.000 t, iar Canada cu 25.000 t. În Statele Unite, în anul 2009 au fost sintetizate aproximativ 118,000 t de grafit sintetic, cu o valoare de 998 milioane de dolari.[93]
Diamantul
[modificare | modificare sursă]
Doar o mică fracție din așa-zisele „mine de diamante” reprezintă de fapt diamante. Zăcămintele sunt zdrobite, însă procedeul se face cu multă grijă pentru a evita distrugerea diamantelor de mărimi mai mari, iar ulterior particulele sunt sortate după densitate. În ziua de azi, diamantele sunt localizate în fracțiile cu conținut bogat de diamante cu ajutorul fluorescenței cu raze X, după care etapele finale de sortare sunt realizate manual. Înainte de folosirea acestei metode cu raze X, separarea se făcea cu ajutorul unor curele cu grăsime, întrucât diamantele au o tendință mai mare de a se lipi de grăsimi decât celelalte minerale componente ale zăcământului.[94]
Cărbunii
[modificare | modificare sursă]Cărbunele se obține pe cale artificială, deși există și în natură compuși cu o compoziție asemănătoare. Există mai multe tipuri de cărbuni, precum cărbunii fosili, care formează zăcăminte bogate în multe locuri de la suprafață. Unii cărbuni fosili conțin până la 99% carbon. Deci, aceștia conțin întotdeauna impurități care influențează proprietățile lor. Alte tipuri de cărbune sunt: cocsul, mangalul și cărbunii tehnici (negrul de fum, negrul de oase, etc.).[95]
Aplicații
[modificare | modificare sursă]





Carbonul este un element esențial pentru toate formele de viață cunoscute, iar fără acesta viața pe care o cunoaștem nu ar putea exista. Principala utilizare economică a carbonului, în afara industriei alimentare și a lemnului, se situează în domeniul hidrocarburilor, unde se remarcă produse importante precum: metanul gazos ca și combustibil fosil și petrolul sau țițeiul. Petrolul este distilat în rafinării prin intermediul industriei petrochimice, pentru a se obține benzina, kerosenul și alți produși. Celuloza este un polimer natural ce conține carbon, produs în corpul plantelor, și care poate fi prelucrat sub formă de lemn, bumbac sau pânză.[96] În corpul plantelor, principala sa utilizare este una mecanică, de a conferi suport și are astfel un rol structural. Printre polimerii de origine animală cu valoare comercială se numără lâna, cașmirul și mătasea. Materialele plastice sunt fabricate din polimeri sintetici de carbon, care mai conțin și atomi de oxigen și de azot în catena principală. Materialele de bază pentru multe din aceste substanțe sintetice provin din industria petrolieră. Diferite forme de carbon sunt adsorbante eficiente de gaze[97][98][99], materiale promițătoare pentru prepararea catalizatorilor[100][101][102] și electrocatalizatorilor[103][104][105].
Precum compușii carbonului sunt extrem de variați, astfel sunt și aplicațiile acestora. Carbonul poate forma diverse aliaje cu fierul, cel mai comun fiind oțelul. Grafitul se poate combina cu argilele pentru a forma uzualele mine de grafit care sunt folosite pentru scris și grafică. Este folosit ca și lubrifiant și pigment[106], ca material de turnare în procesul de fabricare al sticlei, ca și electrod în unele tipuri de baterii și ca moderator nuclear în reactoarele nucleare.
Cărbunele (și implicit mangalul) are multiple utilizări, printre care se numără aplicațiile în domeniul graficii (ca și material de desen), ca sursă de căldură pentru grătare, în metalurgie, etc. Lemnul, cărbunii și petrolul sunt folosiți ca și combustibili pentru producerea de energie și ca sursă de căldură. Diamantul cu calitățile necesare este utilizat pentru fabricarea bijuteriilor, iar diamantele industriale intră în componența instrumentelor folosite pentru forajul, tăierea și polizarea metalelor și a unor pietre prețioase. Materialele plastice sunt fabricate din hidrocarburile fosile, iar fibra de carbon, care este fabricată prin piroliza fibrelor sintetice de poliester, este utilizată pentru consolidarea materialelor plastice.
Negrul de fum este utilizat ca și pigment de culoare neagră, în anumite cerneli, vopsele pe bază de ulei și de apă, hârtia de carbon și în cauciucuri și materiale plastice, ca și aditiv. Cărbunele activ este un material cu proprietăți absorbante și adsorbante, fiind utilizat ca și medicament în tratamentul intoxicațiilor cauzate prin ingerare, în măștile de protecție contra gazelor și în sistemele de purificare a apei[107]. Carbonul este folosit, la temperaturi ridicate, în reacțiile chimice de reducere. Cocsul este folosit pentru reducerea minereului de fier, pentru obținerea acestui metal. Carburile de siliciu, wolfram[108], bor și titan sunt printre cele mai dure materiale cunoscute, fiind utilizate ca și abrazivi. De asemenea, trebuie menționată și implicarea izotopului carbon-14 în procesul de datare cu radioizotop, care are extrem de multe aplicații (în special în arheologie).[52]
Diamante
[modificare | modificare sursă]Măsuri de protecție
[modificare | modificare sursă]
Carbonul pur are o toxicitate extrem de mică asupra oamenilor și poate fi manipulat sau chiar ingerat fără probleme, în cazul grafitului și a unor cărbuni. Este rezistent la dizolvare sau la atacul agenților chimici, chiar și în mediul acid din interiorul tractului digestiv. Din acest motiv, odată ingerat sau ajuns în țesutul uman, este posibil să rămână acolo o perioadă nedefinită. Negrul de fum a fost probabil unul dintre primii pigmenți folosiți pentru tatuare, și se pare că mumia Ötzi avea tatuaje pe bază de carbon, care au supraviețuit timp de 5200 de ani după moartea sa.[109] Inhalarea în cantități mari a prafului de cărbune sau a funinginii poate fi periculoasă, având ca rezultat iritarea țesutului pulmonar și cauzarea unor probleme de respirație congestive care pot duce la pneumoconioză. Praful de diamant, utilizat pe larg ca și abraziv, poate fi toxic prin inhalare sau ingerare. Micropariculele de carbon, care sunt produse în gazele de eșapament ale motoarelor diesel, pot să se acumuleze în plămâni.[110] În toate exemplele date, toxicitatea provine mai degrabă de la contaminanți (de exemplu, compuși organici și metale grele) decât de la elementul în sine.
În cazul celorlalte viețuitoare de pe Pământ, carbonul este la fel de puțin toxic ca și pentru oameni. Conform unor cercetări, se pare că nanoparticulele de carbon sunt mortale pentru adulții speciilor din genul Drosophila.[111]
Carbonul poate lua foc și poate arde puternic la temperaturi înalte, în prezența aerului. Cantități mari acumulate de cărbune, care au fost izolate timp de sute de milioane de ani în absența oxigenului, pot să ardă spontan când sunt expuse aerului.[112][113]
În aplicațiile nucleare, unde grafitul este utilizat pe post de moderator nuclear, este posibilă să aibă loc un incendiu spontan ca urmare a acumulării energiei Wigner. Un exemplu de incident în care materialele din reactor (grafit solid) au început să ardă spontan este accidentul nuclear din Windscale din Marea Britanie, ce avut loc pe 10 octombrie 1957.
Marea varietate de compuși ai carbonului include atât substanțe toxice, precum tetrodotoxina, lectina ricină din semințele de ricin (Ricinus communis), cianurile (CN−) și monoxidul de carbon, cât și substanțe esențiale vieții, precum glucoza și proteinele.
Vezi și
[modificare | modificare sursă]- Cărbuni: antracit, cocs, huilă, lignit, mangal, turbă
- Diamant
- Fulerenă
- Grafen
- Grafit
- Nanotub de carbon
- Reacție Boudouard
- Stea de carbon
Referințe
[modificare | modificare sursă]- ^ a b c „Carbon – Naturally occurring isotopes”. WebElements Periodic Table. Accesat în .
- ^ „History of Carbon”. Arhivat din original la . Accesat în .
- ^ „Biological Abundance of Elements”. The Internet Encyclopedia of Science. Accesat în .
- ^ a b „World of Carbon – Interactive Nano-visulisation in Science & Engineering Education (IN-VSEE)”. Accesat în .
- ^ a b Chemistry Operations (). „Carbon”. Los Alamos National Laboratory. Arhivat din original la . Accesat în .
- ^ Deming, Anna (). „King of the elements?”. Nanotechnology. 21. doi:10.1088/0957-4484/21/30/300201. ISSN 0957-4484. Accesat în .
- ^ „Chinese made first use of diamond”. BBC News. . Accesat în .
- ^ van der Krogt, Peter. „Carbonium/Carbon at Elementymology & Elements Multidict”. Accesat în .
- ^ Ferchault de Réaumur, R.-A. (). L'art de convertir le fer forgé en acier, et l'art d'adoucir le fer fondu, ou de faire des ouvrages de fer fondu aussi finis que le fer forgé (English translation from 1956). Paris, Chicago.
- ^ „Carbon”. Canada Connects. Arhivat din original la . Accesat în .
- ^ Senese, Fred. „Who discovered carbon?”. Frostburg State University. Accesat în .
- ^ Giolitti, Federico (). The Cementation of Iron and Steel. McGraw-Hill Book Company, inc.
- ^ Senese, Fred (). „Who discovered carbon”. Frostburg State University. Accesat în .
- ^ Kroto, H. W.; Heath, J. R.; O'Brien, S. C.; Curl, R. F.; Smalley, R. E. (). „C60: Buckminsterfullerene”. Nature. 318 (6042): 162–163. Bibcode:1985Natur.318..162K. doi:10.1038/318162a0.
- ^ a b c Unwin, Peter. „Fullerenes(An Overview)”. Accesat în .
- ^ „The Nobel Prize in Chemistry 1996 "for their discovery of fullerenes"”. Accesat în .
- ^ a b Harris, PJF (). „Fullerene-related structure of commercial glassy carbons” (PDF). Philosophical Magazine. 84 (29): 3159–3167. Bibcode:2004PMag...84.3159H. doi:10.1080/14786430410001720363. Arhivat din original (PDF) la . Accesat în .
- ^ „Carbon” la DEX online - Etimologia cuvântului carbon; accesat la 13 august 2017
- ^ a b Greenwood and Earnshaw, pp. 276–8
- ^ Nenițescu, Chimie Generală, p. 786
- ^ Reid, Danielle. „The 4 Types of Bonds Carbon Can Form”. study.com.
- ^ Ritter, Stephen K. „Six bonds to carbon: Confirmed”. Chemical & Engineering News.
- ^ Haaland, D (). „Graphite-liquid-vapor triple point pressure and the density of liquid carbon”. Carbon. 14 (6): 357. doi:10.1016/0008-6223(76)90010-5.
- ^ Savvatimskiy, A (). „Measurements of the melting point of graphite and the properties of liquid carbon (a review for 1963–2003)”. Carbon. 43 (6): 1115. doi:10.1016/j.carbon.2004.12.027.
- ^ Greenville Whittaker, A. (). „The controversial carbon solid−liquid−vapour triple point”. Nature. 276 (5689): 695–696. Bibcode:1978Natur.276..695W. doi:10.1038/276695a0.
- ^ Zazula, J. M. (). „On Graphite Transformations at High Temperature and Pressure Induced by Absorption of the LHC Beam” (PDF). CERN. Arhivat din original (PDF) la . Accesat în .
- ^ Irifune, Tetsuo; Kurio, Ayako; Sakamoto, Shizue; Inoue, Toru; Sumiya, Hitoshi (). „Materials: Ultrahard polycrystalline diamond from graphite”. Nature. 421 (6923): 599–600. Bibcode:2003Natur.421..599I. doi:10.1038/421599b. PMID 12571587.
- ^ Dienwiebel, Martin; Verhoeven, Gertjan; Pradeep, Namboodiri; Frenken, Joost; Heimberg, Jennifer; Zandbergen, Henny (). „Superlubricity of Graphite” (PDF). Physical Review Letters. 92 (12). Bibcode:2004PhRvL..92l6101D. doi:10.1103/PhysRevLett.92.126101.
- ^ Deprez, N.; McLachan, D. S. (). „The analysis of the electrical conductivity of graphite conductivity of graphite powders during compaction”. Journal of Physics D: Applied Physics. Institute of Physics. 21 (1): 101–107. Bibcode:1988JPhD...21..101D. doi:10.1088/0022-3727/21/1/015.
- ^ Collins, A. T. (). „The Optical and Electronic Properties of Semiconducting Diamond”. Philosophical Transactions of the Royal Society A. 342 (1664): 233–244. Bibcode:1993RSPTA.342..233C. doi:10.1098/rsta.1993.0017.
- ^ Delhaes, P. (). Graphite and Precursors. CRC Press. ISBN 90-5699-228-7.
- ^ a b Ebbesen, T. W., ed. (). Carbon nanotubes—preparation and properties. Boca Raton, Florida: CRC Press. ISBN 0-8493-9602-6.
- ^ a b Dresselhaus, M. S.; Dresselhaus, G.; Avouris, Ph., ed. (). „Carbon nanotubes: synthesis, structures, properties and applications”. Topics in Applied Physics. Berlin: Springer. 80. ISBN 3-540-41086-4.
- ^ a b Nasibulin, Albert G.; Pikhitsa, P. V.; Jiang, H.; Brown, D. P.; Krasheninnikov, A. V.; Anisimov, A. S.; Queipo, P.; Moisala, A.; et al. (). „A novel hybrid carbon material”. Nature Nanotechnology. 2 (3): 156–161. Bibcode:2007NatNa...2..156N. doi:10.1038/nnano.2007.37. PMID 18654245.
- ^ Nasibulin, A.; Anisimov, Anton S.; Pikhitsa, Peter V.; Jiang, Hua; Brown, David P.; Choi, Mansoo; Kauppinen, Esko I. (). „Investigations of NanoBud formation”. Chemical Physics Letters. 446: 109–114. Bibcode:2007CPL...446..109N. doi:10.1016/j.cplett.2007.08.050.
- ^ Vieira, R; Ledoux, Marc-Jacques; Pham-Huu, Cuong (). „Synthesis and characterisation of carbon nanofibers with macroscopic shaping formed by catalytic decomposition of C2H6/H2 over nickel catalyst”. Applied Catalysis A: General. 274: 1–8. doi:10.1016/j.apcata.2004.04.008.
- ^ a b Clifford, Frondel; Marvin, Ursula B. (). „Lonsdaleite, a new hexagonal polymorph of diamond”. Nature. 214 (5088): 587–589. Bibcode:1967Natur.214..587F. doi:10.1038/214587a0.
- ^ Rode, A. V.; Hyde, S. T.; Gamaly, E. G.; Elliman, R. G.; McKenzie, D. R.; Bulcock, S. (). „Structural analysis of a carbon foam formed by high pulse-rate laser ablation”. Applied Physics A: Materials Science & Processing. 69 (7): S755–S758. doi:10.1007/s003390051522.
- ^ Heimann, Robert Bertram; Evsyukov, Sergey E.; Kavan, Ladislav (). Carbyne and carbynoid structures. Springer. pp. 1–. ISBN 978-0-7923-5323-2. Accesat în . Parametru necunoscut
|last-author-amp=ignorat (ajutor) - ^ Lee, C.; Wei, X.; Kysar, J. W.; Hone, J. (). „Measurement of the Elastic Properties and Intrinsic Strength of Monolayer Graphene”. Science. 321 (5887): 385–8. Bibcode:2008Sci...321..385L. doi:10.1126/science.1157996. PMID 18635798. Sumar pentru neinițiați.
- ^ Sanderson, Bill (). „Toughest Stuff Known to Man : Discovery Opens Door to Space Elevator”. nypost.com. Arhivat din original la . Accesat în .
- ^ Jin, Zhong; Lu, Wei; O’Neill, Kevin J.; Parilla, Philip A.; Simpson, Lin J.; Kittrell, Carter; Tour, James M. (). „Nano-Engineered Spacing in Graphene Sheets for Hydrogen Storage”. Chemistry of Materials. 23 (4): 923–925. doi:10.1021/cm1025188. ISSN 0897-4756.
- ^ Jenkins, Edgar (). The polymorphism of elements and compounds. Taylor & Francis. p. 30. ISBN 0-423-87500-0. Accesat în .
- ^ a b Greenwood and Earnshaw, pp. 289–292
- ^ Nenițescu, Chimie Generală, pp. 791-792
- ^ a b Nenițescu, Chimie Generală, pp. 806-820
- ^ Nenițescu, Chimie Generală, pp. 827-829
- ^ Gannes, Leonard Z.; Del Rio, Carlos Martı́nez; Koch, Paul (). „Natural Abundance Variations in Stable Isotopes and their Potential Uses in Animal Physiological Ecology”. Comparative Biochemistry and Physiology – Part A: Molecular & Integrative Physiology. 119 (3): 725–737. doi:10.1016/S1095-6433(98)01016-2.
- ^ „Official SI Unit definitions”. Accesat în .
- ^ Bowman, S. (). Interpreting the past: Radiocarbon dating. British Museum Press. ISBN 0-7141-2047-2.
- ^ Brown, Tom (). „Carbon Goes Full Circle in the Amazon”. Lawrence Livermore National Laboratory. Accesat în .
- ^ a b Libby, W. F. (). Radiocarbon dating. Chicago University Press and references therein.
- ^ Westgren, A. (). „The Nobel Prize in Chemistry 1960”. Nobel Foundation. Accesat în .
- ^ „Use query for carbon-8”. barwinski.net. Accesat în .
- ^ Watson, A. (). „Beaming Into the Dark Corners of the Nuclear Kitchen”. Science. 286 (5437): 28–31. doi:10.1126/science.286.5437.28.
- ^ Burrows, A.; Holman, J.; Parsons, A.; Pilling, G.; Price, G. (). Chemistry3: Introducing Inorganic, Organic and Physical Chemistry. Oxford University Press. p. 70. ISBN 978-0-19-873380-5. Accesat în .
- ^ Nenițescu, Costin D. (). Chimie organică (ed. VII). Editura Didactică și Pedagogică. p. 12.
- ^ „Functional Groups and Classes of Organic Compounds”, Chemistry LibreTexts, , accesat în
- ^ Arsene, Paraschiva; Popescu, Ștefan (). Chimie și probleme de chimie organică. București: Editura Tehnică. pp. 23–25.
- ^ Levine, Joel S.; Augustsson, Tommy R.; Natarajan, Murali (). „The prebiological paleoatmosphere: stability and composition”. Origins of Life and Evolution of Biospheres. 12 (3): 245–259. Bibcode:1982OrLi...12..245L. doi:10.1007/BF00926894.
- ^ Loerting, T.; et al. (). „On the Surprising Kinetic Stability of Carbonic Acid”. Angew. Chem. Int. Ed. 39 (5): 891–895. doi:10.1002/(SICI)1521-3773(20000303)39:5<891::AID-ANIE891>3.0.CO;2-E. PMID 10760883.
- ^ Haldane J. (). „The action of carbonic oxide on man”. Journal of Physiology. 18 (5–6): 430–462. doi:10.1113/jphysiol.1895.sp000578. PMC 1514663
 . PMID 16992272.
. PMID 16992272. - ^ Gorman, D.; Drewry, A.; Huang, Y. L.; Sames, C. (). „The clinical toxicology of carbon monoxide”. Toxicology. 187 (1): 25–38. doi:10.1016/S0300-483X(03)00005-2. PMID 12679050.
- ^ „Compounds of carbon: carbon suboxide”. Accesat în .
- ^ Bayes, K. (). „Photolysis of Carbon Suboxide”. Journal of the American Chemical Society. 83 (17): 3712–3713. doi:10.1021/ja01478a033.
- ^ Anderson D. J.; Rosenfeld, R. N. (). „Photodissociation of Carbon Suboxide”. Journal of Chemical Physics. 94 (12): 7852–7867. Bibcode:1991JChPh..94.7857A. doi:10.1063/1.460121.
- ^ Sabin, J. R.; Kim, H. (). „A theoretical study of the structure and properties of carbon trioxide”. Chemical Physics Letters. 11 (5): 593–597. Bibcode:1971CPL....11..593S. doi:10.1016/0009-2614(71)87010-0.
- ^ Moll N. G.; Clutter D. R.; Thompson W. E. (). „Carbon Trioxide: Its Production, Infrared Spectrum, and Structure Studied in a Matrix of Solid CO2”. Journal of Chemical Physics. 45 (12): 4469–4481. Bibcode:1966JChPh..45.4469M. doi:10.1063/1.1727526.
- ^ a b Fatiadi, Alexander J.; Isbell, Horace S.; Sager, William F. (). „Cyclic Polyhydroxy Ketones. I. Oxidation Products of Hexahydroxybenzene (Benzenehexol)” (PDF). Journal of Research of the National Bureau of Standards Section A. 67A: 153–162. doi:10.6028/jres.067A.015.
- ^ Pauling, L. (). The Nature of the Chemical Bond (ed. 3rd). Ithaca, NY: Cornell University Press. p. 93. ISBN 0-8014-0333-2.
- ^ Greenwood and Earnshaw, pp. 297–301
- ^ Scherbaum, Franz; et al. (). „"Aurophilicity" as a consequence of Relativistic Effects: The Hexakis(triphenylphosphaneaurio)methane Dication [(Ph3PAu)6C]2+”. Angew. Chem. Int. Ed. Engl. 27 (11): 1544–1546. doi:10.1002/anie.198815441.
- ^ a b Hoover, Rachel (). „Need to Track Organic Nano-Particles Across the Universe? NASA's Got an App for That”. NASA. Arhivat din original la . Accesat în .
- ^ Lauretta, D.S.; McSween, H.Y. (). Meteorites and the Early Solar System II. Space science series. University of Arizona Press. p. 199. ISBN 978-0-8165-2562-1. Accesat în .
- ^ Mark, Kathleen (). Meteorite Craters. University of Arizona Press. ISBN 0-8165-0902-6.
- ^ „Online Database Tracks Organic Nano-Particles Across the Universe”. Sci Tech Daily. . Accesat în .
- ^ William F McDonough The composition of the Earth Arhivat în , la Wayback Machine. in Earthquake Thermodynamics and Phase Transformation in the Earth's Interior. . ISBN 978-0126851854.
- ^ Fred Pearce (). „Fire in the hole: After fracking comes coal”. New Scientist: 36–41.
- ^ "Wonderfuel: Welcome to the age of unconventional gas" by Helen Knight, New Scientist, 12 June 2010, pp. 44–7.
- ^ Ocean methane stocks 'overstated', BBC, 17 Feb. 2004.
- ^ "Ice on fire: The next fossil fuel" by Fred Pearce, New Scientist, 27 June 2009, pp. 30–33.
- ^ Calcule realizate pe fișierul global.1751_2008.csv în [1] publicat de Carbon Dioxide Information Analysis Center.
- ^ Rachel Gross (). „Deep, and dank mysterious”. New Scientist: 40–43.
- ^ Stefanenko, R. (). Coal Mining Technology: Theory and Practice. Society for Mining Metallurgy. ISBN 0-89520-404-5.
- ^ Kasting, James (). „The Carbon Cycle, Climate, and the Long-Term Effects of Fossil Fuel Burning”. Consequences: the Nature and Implication of Environmental Change. 4 (1).
- ^ „Carbon-14 formation”. Accesat în .
- ^ Nichols, Charles R. „Voltatile Products from Carbonaceous Asteroids” (PDF). UAPress.Arizona.edu. Arhivat din original (PDF) la . Accesat în .
- ^ Falkowski, P.; Scholes, R. J.; Boyle, E.; Canadell, J.; Canfield, D.; Elser, J.; Gruber, N.; Hibbard, K.; et al. (). „The Global Carbon Cycle: A Test of Our Knowledge of Earth as a System”. Science. 290 (5490): 291–296. Bibcode:2000Sci...290..291F. doi:10.1126/science.290.5490.291. PMID 11030643.
- ^ Smith, T. M.; Cramer, W. P.; Dixon, R. K.; Leemans, R.; Neilson, R. P.; Solomon, A. M. (). „The global terrestrial carbon cycle”. Water, Air, & Soil Pollution. 70: 19–37. doi:10.1007/BF01104986.
- ^ Nenițescu, Chimie Generală, p. 794
- ^ John Farndon, Enciclopedia ilustrată a rocilor și mineralelor, trad. Ungureanu Adina, Editura Aquila, Oradea, 2008, pag. 144-145, ISBN 978-973-714-414-0
- ^ „Graphite: Graphite mineral information and data.”, Https://www.mindat.org, accesat în Legătură externa în
|newspaper=(ajutor) - ^ a b c USGS Minerals Yearbook: Graphite, 2009 and Graphite: Mineral Commodity Summaries 2011
- ^ Harlow, G. E. (). The nature of diamonds. Cambridge University Press. p. 223. ISBN 0-521-62935-7.
- ^ N.L. Glinka: Chimie generală, ediția a II-a (traducere după ediția a VIII-a rusă), Editura Tehnică, București, 1958; despre carbon și cărbuni: pag. 359-362
- ^ „Uses of Carbon”, Usesof.net, accesat în
- ^ „Activated carbon from lignocellulosics precursors: A review of the synthesis methods, characterization techniques and applications”. Renewable and Sustainable Energy Reviews. 82: 1393–1414. .
- ^ „Biochar-based adsorbents for carbon dioxide capture: A critical review”. Renewable and Sustainable Energy Reviews. .
- ^ „Surface modification of activated carbon for adsorption of SO2 and NOX: A review of existing and emerging technologies”. Renewable and Sustainable Energy Reviews. 94: 1067–1085. .
- ^ „Application of carbonized ion exchange resin beads as catalyst support for gas phase hydrogenation processes”. Reaction Kinetics, Mechanisms and Catalysis: 1–10. .
- ^ „Fine-tuning the catalytic activity by applying nitrogen-doped carbon nanotubes as catalyst supports for the hydrogenation of olefins”. .
- ^ Ptaszyńska, Karolina; Malaika, Anna; Kapska, Magdalena; Kozłowski, Mieczysław (), SO3H-functionalized carbon fibers for the catalytic transformation of glycerol to glycerol tert-butyl ethers (în engleză), 13 (1), Scientific Reports, doi:10.1038/s41598-023-27432-7, ISSN 2045-2322
- ^ Pangotra, Dhananjai; Csepei, Lénárd-István; Roth, Arne; Ponce de León, Carlos; Sieber, Volker; Vieira, Luciana (), Anodic production of hydrogen peroxide using commercial carbon materials (în engleză), 303, Applied Catalysis B: Environmental, doi:10.1016/j.apcatb.2021.120848, ISSN 0926-3373
- ^ Pangotra, Dhananjai; Csepei, Lénárd-István; Roth, Arne; Sieber, Volker; Vieira, Luciana (), Anodic generation of hydrogen peroxide in continuous flow (în engleză), 24 (20), Green Chemistry, doi:10.1039/D2GC02575B
- ^ „Electrochemical synthesis of hydrogen peroxide from water and oxygen”. Nature Reviews Chemistry. 3: 442–458. .
- ^ Chavan, Bhagyesh; Nagose, Swati; Rose, Elvina; Joshi, Amit (), „Surfactant screening techniques for effective dispersion of carbon black pigment”, Coloration Technology (în engleză), pp. cote.12667, doi:10.1111/cote.12667, ISSN 1472-3581, accesat în
- ^ Kalantzis, Demetrios; Daskaloudis, Ioannis; Lacoere, Tim; Stasinakis, Athanasios S.; Lekkas, Demetris F.; De Vrieze, Jo; Fountoulakis, Michail S. (), Granular activated carbon stimulates biogas production in pilot-scale anaerobic digester treating agro-industrial wastewater (în engleză), 376, Bioresource Technology, doi:10.1016/j.biortech.2023.128908, ISSN 0960-8524
- ^ SreeramaReddy, T. V.; Sornakumar, T.; VenkataramaReddy, M.; Venkatram, R. (), Machinability of C45 steel with deep cryogenic treated tungsten carbide cutting tool inserts (în engleză), 27 (1), International Journal of Refractory Metals and Hard Materials, doi:10.1016/j.ijrmhm.2008.04.007, ISSN 0263-4368
- ^ Dorfer, Leopold; Moser, M.; Spindler, K.; Bahr, F.; Egarter-Vigl, E.; Dohr, G. (). „5200-year old acupuncture in Central Europe?”. Science. 282 (5387): 242–243. Bibcode:1998Sci...282..239D. doi:10.1126/science.282.5387.239f. PMID 9841386.
- ^ Donaldson, K.; Stone, V.; Clouter, A.; Renwick, L.; MacNee, W. (). „Ultrafine particles”. Occupational and Environmental Medicine. 58 (3): 211–216. doi:10.1136/oem.58.3.211. PMC 1740105
 . PMID 11171936.
. PMID 11171936. - ^ Carbon Nanoparticles Toxic To Adult Fruit Flies But Benign To Young ScienceDaily (17 aug. 2009)
- ^ „Press Release – Titanic Disaster: New Theory Fingers Coal Fire”. www.geosociety.org. Arhivat din original la . Accesat în .
- ^ McSherry, Patrick. „Coal bunker Fire”. www.spanamwar.com. Accesat în .
Bibliografie
[modificare | modificare sursă]- Greenwood, Norman N.; Earnshaw, Alan (). Chemistry of the Elements (ed. 2nd). Oxford: Butterworth-Heinemann. ISBN 0080379419.
- Costin D. Nenițescu Chimie generală (ed. 1). București, Editura Didactică și Pedagogică.
Legături externe
[modificare | modificare sursă]| Puteți găsi mai multe informații despre Carbon prin căutarea în proiectele similare ale Wikipediei, grupate sub denumirea generică de „proiecte surori”: | |
| Definiții și traduceri în Wikționar | |
| Imagini și media la Commons | |
| Manuale la Wikimanuale | |
| Resurse de studiu la Wikiversitate | |
- Carbonul Arhivat în , la Wayback Machine. de la sistemul-periodic.go.ro
- Incredibila poveste a carbonului Arhivat în , la Wayback Machine., 3 august 2008, Diac. Dr. Adrian Sorin Mihalache, Ziarul Lumina
- Carbon pe In Our Time la BBC. (ascultă acum)
- Carbon de la The Periodic Table of Videos (Universitatea din Nottingham, engleză)
- Carbon de la Britannica (engleză)
- Pagina despre carbon de la asu.edu
- Electrochemical uses of carbon[nefuncțională] (engleză)
- Carbon—Super Stuff. Animation with sound and interactive 3D-models. Arhivat în , la Wayback Machine.


 French
French Deutsch
Deutsch